вания не изменяется.
Для идеального газа внутренняя энергия не зависит от объема, а в процессе дросселирования газ не совершает работы и не участвует в теплообмене, поэтому его внутренняя энергия остается постоянной:
du 0, dT 0, dh 0 .
Для реального газа внутренняя энергия зависит от объема, поэтому при дросселировании
du z 0, dT z 0, dh 0.
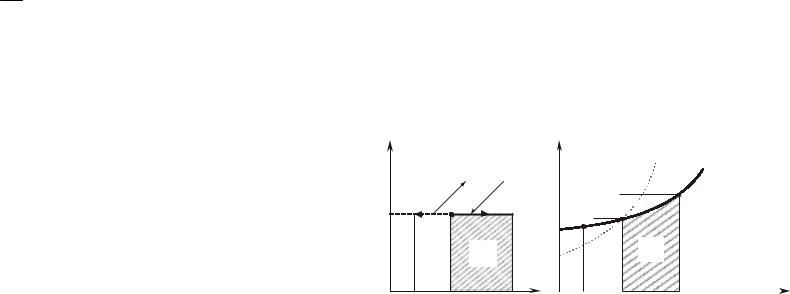
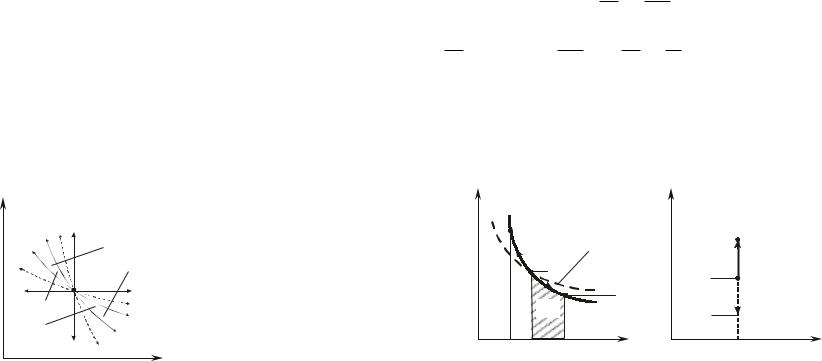
В зависимости от начальных параметров температура реальных газов в конце процесса дросселирования может быть выше, ниже или равна начальной температуре (температура инверсии).
Процесс дросселирования сопровождается трением и завихрениями и является необратимым процессом, поэтому не может быть изображен каким-либо графиком.
Для лучшего понимания физики процессов, происходящих в потоке при его дросселировании, обратимся к первому закону термодинамики для потока (при отсутствии трения) для любого обратимого и необратимого потока
|
|
|
|
|
|
|
|
|
w2 |
w2 |
|
|
|
|
|
q |
h |
|
h |
|
|
|
2 |
1 |
g z |
|
z |
l . |
2 |
1 |
|
|
|
2 |
âíåø |
|
|
|
|
|
|
2 |
|
|
1 |
|
òåõí |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Для случая q |
|
|
|
0, |
z |
|
z |
, |
l |
0, |
w | w |
, следует |
âíåø |
|
|
|
|
1 |
2 |
|
òåõí |
|
|
1 |
|
2 |
|
|
|
|
|
|
|
|
|
|
h1 |
h2 . |
|
|
|
|
|
Следовательно, постоянство энтальпий является свойством любого обратимого и необратимого адиабатного горизонтального потока малой скорости, не совершающего работы, а не «привилегией» дросселируемого потока.
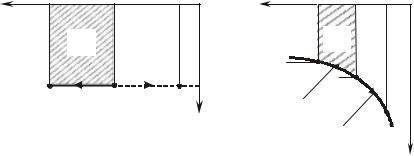
Здесь рассматривалось состояние дросселируемого вещества до дросселя и за дросселем. В самом же дросселе энтальпия может изменяться: проходя через сужение, поток ускоряется, его кинети- ческая энергия возрастает, а, следовательно, энтальпия уменьшается, за дросселем сечение потока снова возрастает, поток замедляется (тормозится), его кинетическая энергия уменьшается и энтальпия увеличивается до прежнего состояния (рис.6.6.2).
|
|
Таблица 6.5.1 |
|
|
|
Изменение внутренней энергии |
Расширение газа |
Сжатие газа |
|
|
|
U > 0 |
n < 1 |
n > 1 |
|
|
|
U = 0 |
n = 0 |
n = 0 |
|
|
|
U < 0 |
n > 1 |
n < 1 |
|
|
|
Знак теплоты |
Расширение газа |
Сжатие газа |
|
|
|
q > 0 |
n < k |
n > k |
|
|
|
q = 0 |
n = k |
n = k |
|
|
|
q < 0 |
n > k |
n < k |
|
|
|
мости, выведенные для адиабатного процесса, остаются справедливыми и для политропного процесса при замене показателя k показателем n. Таким образом, зависимости между основными терми- ческими параметрами имеют вид
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
§ v ·n 1 |
|
§ v |
|
·n |
|
§ P · |
n 1 |
|
T |
P |
|
T |
n |
|
|
1 |
¨ |
2 |
¸ |
; |
1 |
¨ |
|
2 |
¸ |
; |
1 |
¨ |
1 |
¸ . |
(6.5.2) |
|
|
|
|
|
|
|
|
|
|
T2 |
© v1 ¹ |
|
P2 |
© v1 ¹ |
|
T2 |
© |
P2 ¹ |
|
Величина работы вычисляется по формулам
l |
R |
T |
T |
, l |
1 |
Pv |
P v |
. |
(6.5.3) |
|
|
|
n 1 1 |
2 |
|
n 1 1 1 |
2 2 |
|
|
Согласно первому закону термодинамики для политропного процесса
q u |
|
u |
l Cv T |
T |
|
R |
|
T |
T |
|
§C |
|
|
R |
· |
T |
T |
. |
2 |
|
v |
|
|
¸ |
|
1 |
2 |
1 |
|
n 1 |
1 |
2 |
|
¨ |
|
n 1 |
2 |
1 |
|
|
|
|
|
|
|
|
|
|
© |
|
|
¹ |
|
|
|
Сравнивая полученное выражение с формулой q = C(T – T ), на-
2 1
ходим зависимость
C Cv |
|
R nCv Cv R nCv CP |
|
|
|
|
|
n 1 |
n 1 |
|
n 1 |
|
|
|
или, учитывая, что CP k,
Cv