Материал: Белозеров В.И. Учебное пособие по курсу Техническая термодинамика (оригинал)

11 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ютсяпроцессы,представляющиесобойнепрерывнуюпоследователь- |
|||||||||||||||||||||||||||||||||
норазделитьнаравновесныеи.неравновесныеРавновесныминазыва- |
|||||||||||||||||||||||||||||||||
Всепроцессы,происходящиевтермодинамическойсистеме,мож- |
|||||||||||||||||||||||||||||||||
|
стемыноситназваниетермодинамическогопроцесса. |
||||||||||||||||||||||||||||||||
Последовательностьизменениятермодинамическогосостоянияси- |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
.состояния |
|
(сжатие,расширение,теплообмен)происходитпроцессизмененияего |
|||||||||||||||||||||||||||||||||
Врезультатевоздействиянарабочеетело(газ,пар)внешнейсреды |
|||||||||||||||||||||||||||||||||
|
|
|
4..ПроцессЦикл |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
раметров.состояния |
|||||||
Эторавенствоиспользуетсяприустановлениизаконовизмененияпа- |
|||||||||||||||||||||||||||||||||
|
|
|
z |
©wy¹ |
y |
©wx¹ |
x |
©wz¹ |
|
|
|
|
|
|
|
|
|
||||||||||||||||
.(34) |
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
¸ |
|
|
|
|
¨ |
|
¸ |
|
|
|
¨ |
|
¸ |
|
|
|
¨ |
|
|
|
|
|
|
|
|
|
|||||
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
· |
|
x |
|
|
|
|
z· |
|
§ |
|
y· |
|
§ |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
§w |
|
|
|
|
w |
|
|
|
|
w |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
Несложныепреобразованиядают |
||||||||||||||||||||||
|
|
|
|
|
|
|
x |
©wy¹ |
|
|
|
|
y |
wx¹ |
© |
|
|
|
|
|
|
|
|
||||||||||
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
0 |
dy |
|
¸ |
|
|
|
¨ |
dx |
|
¸ |
|
|
|
|
¨ |
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
§wz· |
|
wz· |
§ |
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
Еслипараметрсостоянияdzнеизменяется,тоdz=0: |
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
x |
wy¹ |
© |
|
y |
©wx¹ |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dy. |
|
¸ |
|
|
|
|
¨ |
dx |
|
¸ |
|
|
¨ |
dz |
откуда |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
· |
|
z |
|
|
§ |
|
z· |
w |
§ |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
w |
|
|
|
|
|
|
|
|||||
.(33) |
|
|
|
|
, |
x,y |
f |
|
z |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
нымеждусобойуравнениемсостояния |
|||||||||||||||||||||||||
–параметрысостояния,тоонисвяза- |
z |
xy |
Сдругойстороны,если |
||||||||||||||||||||||||||||||
|
, |
, |
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
зуетсяприрассмотренииряда.вопросов |
||||||||||||||||||||||||||
обходимостиновыепараметры.состоянияЭтотприемширокоисполь- |
|||||||||||||||||||||||||||||||||
риватьвеличинуХкакновыйпараметрсостояния,.е.твводитьприне- |
|||||||||||||||||||||||||||||||||
междуначальнымиконечным.состояниямиЭтопозволяетрассмат- |
|||||||||||||||||||||||||||||||||
етсяизменениемсостояниятела,независимоотхарактерапроцесса |
|||||||||||||||||||||||||||||||||
Посколькуdx–полныйдифференциал,тоегоизменениеопределя- |
|||||||||||||||||||||||||||||||||
.(32) |
|
|
|
. |
|
|
|
|
|
|
f |
|
|
X |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
P,T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
.Ðèñ4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
1 |
|
|
|
|
|
|
1 |
|
|
1 |
|
1 |
|
|
|
|
,T |
P |
|
|
|
|
|
,T |
|
P |
|
|||
|
|
|
|
|
II |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
II |
|
|
|
|
|
|
|
|
|
|
|
I |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
|
|
|
|
|
|
1 |
|
|
2 |
|
|
|
|
2 |
|
,T |
P |
|
|
|
|
|
,T |
|
P |
|
|||
|
|
|
|
I |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ÿíèÿ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
обладает,очевидно,любаяоднозначнаяфункцияотпараметровсосто- |
||||||||||||||||
расостоянияявляетсяполным.дифференциаломНоэтимжесвойством |
||||||||||||||||
Сматематическихпозицийэтоозначает,чтодифференциалпарамет- |
||||||||||||||||
изменениемегосостоянияинезависитотхарактера.процесса |
||||||||||||||||
стояния,следовательно,изменениепараметрасостоянияопределяется |
||||||||||||||||
.ковоАналогичныерассужденияприменимыклюбомупараметрусо- |
||||||||||||||||
.ниеНовобоихслучаяхизменениеобъемарабочеготелабудетодина- |
||||||||||||||||
.телаВпроцессахII-II,сначаламеняетсятемпература,апотомдавле- |
||||||||||||||||
ратураостаетсяпостоянной,азатемменяетсятемпературарабочего |
||||||||||||||||
процессахI-Iсначаламеняетсядавлениерабочеготела,аеготемпе- |
||||||||||||||||
Нопереходизсостояния1в2возможноосуществитьпо-.разномуВ |
||||||||||||||||
|
1 |
1 |
2 |
2 |
|
1 |
|
2 |
v |
|||||||
|
P,T.) |
,T)M( |
M(P |
v |
|
|
||||||||||
|
|
|
|
|
Изуравнениясостоянияможносчитать |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ò=Ò. |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тело,совершаякакой-топроцесс,перешловсостояние2,гдеР=Ри |
||||||||||||||||
1 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
иТ=Т,рабочее |
Пустьизначальногосостояния1,вкоторомР=Р |
|||||||||||||||
.(31) |
|
|
|
|
MP,T. |
v |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
вычислитьудельныйобъем,тополучится |
|||||||||||
Еслиизуравнениясостоянияпростогохимическиоднородноготела |
||||||||||||||||
.3Общиесвойствапараметровсостояния |
||||||||||||||||
|
называетсякалорическимуравнением.состояния |
|||||||||||||||
.(27) |
|
|
|
fP,V |
|
U |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
гия(иликакой-либодругойкалорическийпараметр), |
|||||||||||||||
в.калориметреУравнениесостояния,вкотороевходитвнутренняяэнер- |
||||||||||||||||
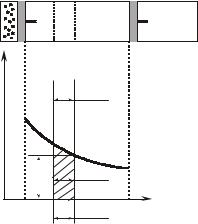
1.3. Работа изменения объема рабочего тела
Всякое изменение объема вещества сопровождается совершением работы. При расширении вещество совершает работу против внешних сил, при сжатии внешние силы совершают работу над веществом.
Положим, что 1 кг газа, расширяясь в цилиндре двигателя, перемещает поршень из положения А в положение В, причем процесс изменения состояния газа на Pv–диаграмме изображается линией 1–2 (рис. 1.3.1).
На элементарном отрезке пути поршня a–b, равном dS, изменением давления можно пренебречь, поэтому элементарная работа газа на этом участке составляет dl= PFdS, где F – площадь поршня и, следовательно, PF – сила, действующая на поршень. С другой стороны, FdS = dv, следовательно,
dl Pdv, |
Äæ |
|
|
. |
|||
|
|||
|
êã |
|
|
Очевидно, что суммарная работа, совершаемая газом в процессе 1–2, составляет
A |
a |
b |
B |
P
|
dS |
1 |
|
dl |
2 |
|
|
P |
|
4 |
3 |
|
|
dv |
v |
Ðèñ. 1.3.1 |
|
v2 |
|
|
l ³Pdv, |
Äæ |
|
êã |
. |
|
v1 |
|
|
При расширении газа dv>0 и l>0, т.е. работа расширения газа есть величина положительная; при сжатии dv<0 и l<0, т.е. работа сжатия газа есть величина отрицательная.
Из Pv–диаграммы видно, что элементарная работа dl графи- чески изображается площадью прямоугольника с основанием dv
и высотой P (заштрихованная на графике), следовательно, полная работа изменения объема в процессе 1–2 изображается площадью 1–2–3–4.
Глава 1
ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
1.1. Равновесные и неравновесные процессы
Любой процесс совершается под механическим (при расширении или сжатии рабочего тела) или термическим (при нагревании или охлаждении рабочего тела) воздействием на тело со стороны внешней среды, состояние которой при этом также меняется.
Чем медленнее изменяется состояние внешней среды, тем медленнее совершается процесс, тем больше успевают выравниваться температура и давление среды и рабочего тела, тем ближе находятся они к состоянию равновесия в каждый момент времени. При бесконечно малой скорости протекания такой процесс будет равновесным, т.к. внешняя среда и рабочее тело будут медленно переходить из одного состояния равновесия в другое. Таким образом, весь процесс можно представить как последовательный ряд равновесных состояний.
Действительные (реальные) процессы неравновесны, потому что протекают они с конечной скоростью, при значительной разности температур и давлений между внешней средой и рабочим телом.
После протекания равновесного процесса в одном направлении его можно провести в обратном направлении через ту же последовательность равновесных состояний. При этом, в результате протекания прямого и обратного равновесных процессов никаких изменений в окружающих телах не произойдет, а рабочее тело возвратится в первоначальное состояние, поэтому равновесный процесс называется также обратимым.
Все реальные процессы необратимы. Примерами необратимых процессов являются процессы горения топлива, передача тепла от горячих тел к менее нагретым, дросселирование жидкости или газа и т.д.
В термодинамике изучаются, главным образом, обратимые процессы. Изучение необратимых процессов, протекающих в тепловых двигателях, является весьма сложным. Кроме того, изучение обратимых процессов дает возможность наметить более выгодные условия для осуществления действительных процессов в тепловых двигателях. Перенесение результатов изучения обратимых процессов
16 |
13 |
15
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
=0,611.Äæ/êã |
/êã,h=Pv |
v=0,0010002ì |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
Ð=610,8Ïà, |
например,дляводыt=0,01С, |
отсчета,u=0,h=Pv, |
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
î |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Посколькуhиuвзаимосвязаны,товточке,принятойзаначало |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
наруживаетсяприанализеконкретных.явлений |
|||||||||||||||||||||||||||||||||||
которомупротекает.процессФизическийсмыслэтойфункцииоб- |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
1 |
|
1 |
|
|
|
|
|
2 |
2 |
|
|
|
2 |
|
|
1 |
|
|
2 |
|
|
' |
|
|||||
(u+Pv),независимоотпути,по |
|
=(u+Pv)– |
–h |
|
|
h=h |
цессов |
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
³dh |
|
|
'h |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
,адлянезамкнутыхпро- |
|
|
|
|
Ñ |
|
|
|
|
|
|
Такимобразом,дляцикла |
||||||||||||||||||||||||||||||||
.е.тдифференциалэнтальпииявляетсяполным.дифференциалом |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
wT¹ |
© |
|
|
|
T |
©wP¹ |
|
|
|
|
|||||||||
|
|
1 |
2 |
|
|
P |
|
|
1 |
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
'h |
|
|
|
|
|
|
¸ |
|
|
|
|
¨ |
|
|
|
|
¸ |
|
|
|
¨ |
|
|
|
|
||||||||
, |
t) |
|
(t |
|
c |
|
h |
h |
|
|
|
, |
dT |
|
|
|
|
|
dP |
|
|
|
dh |
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
wh· |
§ |
§wh· |
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
ния,например,еслизаданазависимостьh=f(P,V),то |
||||||||||||||||||||||||||||||||||||||||||
стоянияииграетрольодногоизкалорическихпараметровсостоя- |
||||||||||||||||||||||||||||||||||||||||||||
леннойизфункцийсостояния,энтальпиясамаявляетсяфункциейсо- |
||||||||||||||||||||||||||||||||||||||||||||
Будучисостав- |
|
=u+Pv,Дж/кг,называемаяэнтальпиейвещества. |
||||||||||||||||||||||||||||||||||||||||||
Нарядусвнутреннейэнергиейважнуюрольиграетвеличинаh= |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
житьпараметромсостояния.вещества |
||||||||||||||||||||||||||||
параметры(P,v,T),следовательно,ивнутренняяэнергияможетслу- |
||||||||||||||||||||||||||||||||||||||||||||
Аналогичнымисвойствамиобладаютвсерассмотренныевыше |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ñ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
0 |
|
³dU |
|
|
'U |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
равнонулю: |
|||
зываютсяциклами),тоизменениевнутреннейэнергиивнембудет |
||||||||||||||||||||||||||||||||||||||||||||
веществовозвращаетсявисходноесостояние(такиепроцессына- |
||||||||||||||||||||||||||||||||||||||||||||
Очевидно,чтоеслипроцессзамкнут,.е.теслипозавершенииего |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
©wV¹ |
|
|
V |
|
|
|
|
|
|
|
||||||
êã |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
©wP¹ |
|
|
|||||||||||||
|
|
1 |
|
2 |
|
|
|
v |
|
|
|
1 |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
¸ |
|
|
|
|
¨ |
|
|
¸ |
|
|
|
|
¨ |
|
|
||
. |
|
t, |
|
t |
|
c |
|
|
|
u |
|
u |
|
u |
' |
; |
dV |
|
|
|
|
|
|
dP |
|
|
|
|
|
dU |
||||||||||||||
Äæ |
|
|
|
|
|
|
|
|
|
|
|
§wU· |
· |
|
|
§wU |
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
равенством |
|||
f(P,V)иможетбытьпредставлен |
|
|
нымдифференциаломфункции |
|||||||||||||||||||||||||||||||||||||||||
Математическиэтоозначает,чтодифференциалdUявляетсяпол- |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
U |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
1 |
|
1 |
|
|
f |
|
|
2 |
|
2 |
|
|
f |
|
|
|
³dU |
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
P,V |
|
|
,V |
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
U |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
U |
2 |
U |
c |
'U |
|
b |
'U |
|
|
a |
'U |
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
14 |
энергииU=f(P,V): |
|
.Ðèñ1.2.1 |
|
|
|
будутиизменениязначениявнутренней |
|
|
яниявеществаодинаковы,одинаковыми |
v |
|
|
2 |
|
|
|
|
вкоторыхначальныеиконечныесосто- |
|
c |
Так,впроцессаха,bиc.(рис1),.2.1 |
|
|
нымиконечнымсостояниями.вещества |
|
b |
|
|
|
значноопределяетсязаданныминачаль- |
|
|
зависитотхарактерапроцесса,аодно- |
|
|
реннейэнергиивкаком-либопроцессене |
|
a |
|
|
1 |
это.состояниеПоэтомуизменениевнут- |
|
|
висимыхпараметров,определяющих |
|
P |
однозначнуюфункциюлюбыхдвухнеза- |
|
|
.энергииЭтоозначает,чтовнутренняяэнергияпредставляетсобой |
||
домусостояниювеществасоответствуетоднозначениевнутренней |
||
Изсамогоопределениявнутреннейэнергиивытекает,чтокаж- |
||
|
êã |
|
M |
|
|
|
, |
||
. |
|
|
u |
|
Äæ |
|
|||
|
|
U |
||
|
|
|
||
|
|
|
стваравнаМкг,то |
|
етсябуквойu.Такимобразом,еслимассарассматриваемоговеще- |
||||
относяткединицемассы(1.кг)Такаяудельнаяэнергияобознача- |
||||
шейопределенностивнутреннююэнергиюгаза(вещества)обычно |
||||
сящимотмассыиназываемыминтенсивными.)Поэтомудляболь- |
||||
.е.тзависитотегомассы(впротивоположностьсвойствам,незави- |
||||
ВнутренняяэнергияUявляетсяэкстенсивнымсвойствомгаза, |
||||
|
|
|
|
.энергии |
атомной(энергияэлектронныхоболочекатомов)ивнутриядерной |
||||
сцеплениямеждумолекулами,внутримолекулярнойэнергии,внутри- |
||||
энергиивнутримолекулярныхколебаний,потенциальнойэнергиисил |
||||
тельногоивращательногодвижениймолекул,составляющихтело, |
||||
|
|
|
|
U |
Внутренняяэнергия()теласкладываетсяизэнергийпоступа- |
||||
какфункциисостояния .2.1Внутренняяэнергияиэнтальпиярабочеготела
цессыот.необратимых тов,учитывающихвлияниефакторов,отличающихобратимыепронанеобратимыеосуществляетсяспомощьюопытныхкоэффициен-

1
2
P
1
S 
 P S
P S
1 |
|
2, |
2 |
z |
Q |
z |
|
1 |
|
2 |
|
Ðèñ. 1.5.1
'Eêèí |
§ w2 |
w2 |
· |
|
|||
G¨ |
2 |
|
1 |
¸ . |
(1.5.1) |
||
2 |
2 |
||||||
|
© |
|
¹ |
|
|||
Рассмотрим уравнение первого закона термодинамики |
|
||||||
Q12 |
U2 U1 L12 . |
|
|||||
Выясним, какие виды работ производит движущийся поток газа
(жидкости).
Между сечениями 1 и 2 может быть подведено некоторое коли-
чество тепла Q .
1-2
Площадь сечения и давление в сечении 1 обозначим через S и
1
P , в сечении 2 – S и P . Количество вещества, проходящего через
1 2 2
поперечное сечение потока в единицу времени (массовый расход), обозначим через G. В соответствии с уравнением неразрывности стационарного потока G одинаково для любого сечения канала (G = = const).
Обозначим через x длину пути, проходимого за единицу времени
1
через сечение S рассматриваемой порции газа (жидкости). Чтобы
1
переместить эту порцию на расстояние x , нужно совершить работу,
1
равную произведению силы (эта сила равна произведению давления на площадь сечения S ) на x :
11
L1 P1S1x1,
S1 x1 V1.
Очевидно, что
V1 v1G.
Таким образом,
20
Графическая интерпретация работы |
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
на Pv–диаграмме наглядно показывает, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
что ее величина зависит от того, каким |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
путем газ переходит из начального со- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
стояния в конечное. Поэтому можно |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
сказать, что работа является функци- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
l |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ей процесса и при одинаковых началь- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ных и конечных состояниях газа может |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
быть различной в зависимости от того, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
v |
|
по какому пути совершается этот про- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
цесс. Отсюда же вытекает, что работа |
Ðèñ. 1.3.2 |
|
|
|
|
||||||||||||||||||||
l не является функцией состояния, а ее
дифференциал dl не является полным дифференциалом.
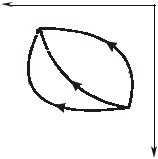
Работа газа за цикл в целом будет положительной (рис. 1.3.2), если линия расширения расположена выше линии сжатия (т.е. линия цикла направлена по часовой стрелке), ибо в этом случае положительная работа расширения по абсолютной величине больше отрицательной работы сжатия, и, наоборот, работа отрицательна, если линия расширения расположения ниже линии сжатия (т.е. линия цикла направлена против часовой стрелки). В первом случае цикл называется прямым, а во втором – обратным, причем в обоих случаях работа газа за цикл измеряется площадью, ограниченной линией цикла.
1.4. Первый закон термодинамики
По исторически сложившимся традициям первый закон термодинамики часто трактуют как приложение всеобщего закона сохранения и превращения энергии к тепломеханическим процессам. Фактически же никакого различия между этими двумя законами нет, ибо первый закон термодинамики применяется не только при анализе тепломеханических процессов, но и в других случаях, например, в термохимии, поэтому наиболее полно его сформулировать можно так:
энергия изолированной термодинамической системы остается неизменной, независимо от того, какие процессы в ней протекают.
Для тепломеханических процессов это означает, что если в тепловом двигателе совершается прямой цикл, то сообщенное в этом
17
19
каяэнергияпотокаизменяетсянавеличину |
|||
междусечениями1и2подлинеканала.(рис1),.5.1тоикинетичес- |
|||
потоке,аw–скорость.потокаПосколькускоростьпотокаменяется |
|||
гдеG–массанекоторогофиксированногоколичествавеществав |
|||
, |
|
2 |
êèí |
|
|
E |
|
|
Gw |
||
2 |
|
||
|
|
||
|
|
|
гиюпотока |
Длядвижущегосяпотокаследуетучитыватькинетическуюэнер- |
|||
|
|
|
.формы |
Рассмотримтечениежидкостиилигазавканалепроизвольной |
|||
ливдлялюбыхсистем–инеподвижных,и.движущихся |
|||
Первыйзаконтермодинамикиимеетобщийхарактерисправед- |
|||
|
потока |
|
|
|
|
|
|
|
|
|||
.5.1Уравнениепервогозаконатермодинамикидля |
||||||||||||
|
|
|
кающихвпотокерабочего.тела |
|||||||||
физическоесодержаниелишьприрассмотрениипроцессов,проте- |
||||||||||||
случаечистоматематическуювеличинуиприобретаетконкретное |
||||||||||||
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
какиэнтальпия,представляетсобойвобщем |
³vdP, |
Интеграл |
||||||||||
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
³vdP. |
|
1 |
2 |
q |
|
|
|
|
|
|
|
.4.(16) |
h |
h |
|
|
|
|
|
|
|
|||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
авконечномвиде |
|||
.4.(15) |
dhvdP, |
dq |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
èëè |
|
d(uPv)vdP |
|
dud(Pv)vdP |
dq |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
итогда |
|
d(Pv)vdP |
Pdv |
|
|
|
|
|
|
||||
|
vdP |
+ |
Pdv |
)= |
Pv |
d |
.Поскольку |
h |
энтальпия |
|||
|
,òî |
|
( |
|
|
|||||||
Вэтовыражениедлявнутреннейэнергииuможетбытьвведена |
||||||||||||
.4.(14) |
dl. |
du |
dq |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
18 |
|
|
|
|
|
|
|
|
|
|
|
|
èëè |
.4.(13) |
|
|
Pdv |
du |
|
dq |
|
|
|
|||
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
участкупроцесса, |
||
авдифференциальнойформе,соответствующейэлементарному |
||||||||||||
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
v |
|
|
|
|
|
|
|
|
.4.(12) |
|
³Pdv, |
1 |
|
2 |
u |
q |
|
|
|||
|
|
u |
|
|
|
|||||||
|
|
|
|
2 |
v |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
термодинамикидляпроцесса2–1принимаетвид |
||||||||||
Вразвернутойформеаналитическоевыражениепервогозакона |
||||||||||||
|
|
|
|
телу,тоq>0,впротивномслучаеq<.0 |
||||||||
етсяалгебраическойвеличиной:еслионоподводитсякрабочему |
||||||||||||
l<0,поэтомуитеплоq,находящеесявлевойчастиравенства,явля- |
||||||||||||
бочимтелом,тоl>0,еслионасовершаетсянадрабочимтелом,то |
||||||||||||
u<.0Равнымобразом,еслиработасовершаетсяра- |
|
номслучае |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
u>0,впротив- |
|
личины:есливнутренняяэнергияувеличивается,то |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
ражениемпервогозаконатермодинамики,входяталгебраическиеве- |
||||||||||||
Вправуючастьэтогоравенства,называемогоаналитическимвы- |
||||||||||||
.4.(11) |
|
. |
2 |
1 |
|
|
12 |
|
|
|
||
|
|
ul |
|
|
q |
|
|
|
||||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
нимаетвид |
случаеизисточникатепла,рабочеготелаиобъектаработы),при- |
||||||||||||
втермодинамическиизолированнойсистеме(состоящейвданном |
||||||||||||
ниебалансаэнергии,выражающеенеизменностьобщегозапасаее |
||||||||||||
12
0,поэтомууравне- |
ζ |
–u |
u=u |
|
общемслучаедляэтогопроцесса |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
Рассмотримтеперьпроизвольныйнезамкнутыйпроцесс.2–1В |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
еесчет.теплу |
||
ратномциклезатраченнаяработавточностиравнаполученномуза |
||||||||||||||
Спомощьюаналогичногорассужденияможнопоказать,чтовоб- |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
0 |
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
=l. |
случаеq |
|
первомузаконутермодинамики,аизэтогоследует,чтовданном |
||||||||||||||
следноеисчезновение.энергииОбапредположенияпротиворечат |
||||||||||||||
|
|
|
|
0 |
0 |
|
|
|
|
|
|
|
|
|
,тоимелобыместобес- |
ней.энергииРавнымобразом,еслиq>l |
|||||||||||||
вогорода,.е.тдвигатель,совершающийработубеззатратывнеш- |
||||||||||||||
томожнобылобысоздатьтакназываемыйвечныйдвигательпер- |
||||||||||||||
0 |
0 |
|
|
|
|
|
³dl |
0 |
l |
|
|
|||
|
q<l |
|
|
|
|
|
|
|
||||||
, |
.Еслибыоказалось,что |
|
Ñ |
|
|
|
носовершаемойимработе |
|||||||
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
Ñ |
0 |
|
|
|
|
|
должнобытьвточностирав- |
³dq |
q |
циклерабочемутелутепло |
|||||||||||
|
||||||||||||||
|
|
|
|
|
|
|||||||||