§ |
a |
· |
v b RT , |
|
¨P |
|
|
¸ |
(7.1.1) |
v |
2 |
© |
|
¹ |
|
|
учитывает реальные свойства газа – наличие межмолекулярного взаимодействия в газах и собственный объем молекул.
Уравнение (7.1.1) – это кубическое уравнение относительно v, следовательно, оно имеет три корня, причем возможны три случая:
1)один корень действительный и два мнимых;
2)все три корня действительные и различные;
3)все три корня действительные и равные между собой. Случай трех действительных равных между собой значений при
данном P соответствует критическому давлению. Случай одного действительного и двух мнимых корней соответствует сверхкрити- ческим давлениям, т.к. при заданных P и T возможно единственное значение v, а мнимые корни не имеют физического смысла. Три действительных и различных корня соответствуют докритическим давлениям.
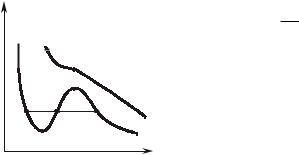
Сверхкритические изотермы ван-дер-ваальсовского газа каче- ственно соответствуют изотермам реального газа. Докритические изотермы вместо горизонтального участка, соответствующего фазовому переходу «жидкость – пар», имеют волнообразный участок (рис. 7.1.3). Участок 1-2 соответствует метастабильному состоянию жидкости (перегретая жидкость), а участок 5-4 – метастабильному состоянию пара (переохлажденный пар); 1-3-5 – это участок изотермы, соответствующий фазовому переходу «жидкость – пар». В отличие от участков 1-2 и 5-4 эта прямая соответствует стабильным состояниям вещества. Участок 2-3-4 имеет волнообразный харак-
тер и поскольку на этом участке
|
|
|
§ wP · |
P |
|
|
¨ |
¸ >0, |
|
|
|
© wv ¹T |
|
k |
|
то он соответствует физически нереа- |
|
|
|
a |
|
|
|
|
4 |
|
|
лизуемым состояниям и лишен физи- |
|
|
|
|
|
|
|
ческого смысла. |
|
1 |
|
|
Положение изотермы 1-3-5 может |
|
|
|
|
3 |
5 |
b |
быть определено с помощью правила |
|
|
|
2 |
|
v |
Максвелла, согласно которому положе- |
|
|
|
ние прямой 1-3-5 относительно волно- |
Ðèñ. 7.1.3 |
|
|
|
Глава 7
РЕАЛЬНЫЙ ГАЗ. УРАВНЕНИЕ СОСТОЯНИЯ РЕАЛЬНОГО ГАЗА
7.1. Опыты Эндрюса. Критическая точка.
Уравнение Ван-дер-Ваальса
Давно было известно, что ряд веществ, находящихся при комнатной температуре в газообразном состоянии, удается перевести в жидкое состояние путем сжатия при постоянной температуре: вна- чале газ сжимается, затем, когда давление газа достигнет величи-
ны P при данной температуре, начинается конденсация газа. После
S
превращения газа в жидкость дальнейшее сжатие будет приводить к увеличению давления жидкости; при этом из-за малой сжимаемости жидкости значительное увеличение давления приводит к весьма малому уменьшению удельного объема.
При уменьшении давления, действующего на жидкость, вещество пройдет те же самые состояния в обратном порядке: оно расширится до точки кипения, произойдет испарение, а затем получившийся пар будет расширяться до атмосферного давления.
До 1869 г. жидкости и их пары считались существенно различными фазами, как, например, твердое тело и жидкость. Это опроверг Т. Эндрюс (английский физик) после проведения опытов в 1857–1869 гг. с углекислотой.
Измеряя зависимость v от P на разных изотермах, Эндрюс установил, что чем выше температура, тем меньше разница между удельными объемами газообразной и жидкой фаз. С повышением температуры величина удельного объема сухого насыщенного пара vs быстро уменьшается, а величина удельного объема насыщенной жидкости (кипящей) vc увеличивается, следовательно, чем выше температура на изотерме, тем меньше величина разности (vs – vc), т.е. с повышением температуры уменьшается разница между плотностями жидкой и газовой фаз.
Характер зависимости v от P по изотермам изображен на рис. 7.1.1.