Материал: Белозеров В.И. Учебное пособие по курсу Техническая термодинамика (оригинал)
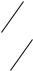
71 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
.емкостью |
дальнейшембудемназыватьудельнуютеплоемкостьпростотепло- |
|||||||||||||||||||||||
.дусТакуютеплоемкостьназываютудельной.теплоемкостьюВ |
|||||||||||||||||||||||
него),чтобыповысить(илипонизить)еготемпературунаодингра- |
|||||||||||||||||||||||
обходимоподвестикединицеколичествавещества(илиотвестиот |
|||||||||||||||||||||||
Теплоемкостьюназываетсятоколичествотеплоты,котороене- |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
знать.теплоемкость |
||||
рабочеетеловпроцессенагреванияилиохлаждения,необходимо |
|||||||||||||||||||||||
Дляопределенияколичестватепла,котороеполучаетилиотдает |
|||||||||||||||||||||||
|
.4.5Теплоемкость |
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
i |
P |
|
|
|
|
1 |
i |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
¦ |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
i |
g |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
. |
|
|
|
|
|
|
|
n |
|
|
|
i |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
i |
P |
|
|
|
|
|
r |
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
i |
g |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
апереходотмассовыхдолейкобъемным–поформуле |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
1 |
i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
i |
|
|
i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
¦rP |
|
|
|
|
|
|
|
|
|
|
|||||
|
, |
|
|
|
|
|
|
|
n |
|
|
i |
g |
|
|
|
|
|
|||||
|
|
|
|
i |
|
i |
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
rP |
|
|
|
|
|
|
|
|
|
|
|
||
реходотобъемныхдолейкмассовымпроизводитсяпоформуле |
|||||||||||||||||||||||
мулывзаимногопереходаотодногосоставасмесик.другомуПе- |
|||||||||||||||||||||||
Исключаявсематематическиепреобразования,приведемфор- |
|||||||||||||||||||||||
|
|
|
|
cì |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
. |
|
|
R |
|
i |
|
|
|
|
|
i |
|
|
|
|
|
|
|
|||
.3.(514) |
|
i |
|
|
|
|
|
Pg |
|
|
P |
|
|
|
|
|
|||||||
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
компонентанауравнениесостояниясмеси,получаем |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
i |
гдеn–числомолейкомпонента;или,деляуравнениесостояниядля |
|||||||||||||||||||||||
|
|
n |
|
|
|
|
i |
|
|
|
|
V |
i |
|
|
|
|
||||||
.3.(513) |
, |
i |
|
P |
|
|
|
|
|
Pr |
|
|
i |
|
P |
P |
|
|
|
|
|||
|
|
n |
|
|
|
|
|
|
|
|
|
|
V |
|
|
|
|
|
|||||
i |
i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
ПозаконуМариотта–БойляможнозаписатьPV=PV,откуда |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ïðèv=.const |
T |
p |
Шарля |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
1 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
p |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
70 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
2 |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
ïðèP=const; |
|
|
|
T |
|
|
v |
Гей–Люссака |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
1 |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
|
v |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ныдавлениям; |
|
стояннойтемпературе,тоудельныеобъемыобратнопропорциональ- |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
2 |
|
|
|
|
|
|
||||
–еслиизменениепроисходитприпо- |
|
|
p |
|
|
|
|
|
v |
|
Бойля–Мариотта |
|||||||||||||||||||||||||||||
2 |
|
|
|
|
|
1 |
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
p |
|
|
|
|
|
v |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вспомнимгазовыезаконы: |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
отспособазадания.смеси |
|||||||||||
Рассмотримопределениепарциальныхдавленийвзависимости |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
i |
i |
|
1 |
|
i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ñì |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
¦gR. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
.3.(512) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
ñì |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
илипоформуле |
|
P |
послепредварительногоопределения |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ê |
|
кмоль |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ñì |
|
ñì |
|
|
|
|
|
|
|
||||||||
.3.(511) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8314 |
|
|
|
|
|
|
R |
|
P |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
Äæ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
отношению |
Величинагазовойпостояннойдлясмесиподсчитываетсяпосо- |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
n |
P |
|
|
|
|
|
2 |
P |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
K |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
n |
g |
2 |
g |
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
g |
|
|
|
|
|
ñì |
|
|
|
|
|
|
|
|||||||||
.3.(510) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
Делячислительизнаменательна |
||||||||||||||||||||||||||
|
,получим |
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
n |
P |
|
|
|
|
|
|
2 |
P |
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
K |
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
n |
|
|
|
2 |
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
m |
|
|
|
|
|
|
|
m |
|
|
|
m |
|
|
|
|
|
ñì |
|
|
|
|
|
|
||||||||
|
|
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
P |
|
|
|
|
|
|
1 |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
,n |
P |
1 |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
и,.д.ттогда |
|
2 |
|
|
|
|
|
|
1 |
n |
учтем,что |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
|
|
|
|
|
m |
|
|
||
|
|
|
|
n |
|
|
|
|
|
2 |
|
|
1 |
|
|
|
n |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
Kn |
|
n |
|
n |
|
|
|
|
|
ñì |
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Еслисмесьзаданапомассовомусоставу,тодляподсчета |
||||||||||||||||||||||||||||||||||||||||
|
|
n |
|
n |
|
|
|
|
|
2 |
2 |
|
|
1 |
1 |
|
|
|
|
|
ñì |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
||||||||||||||||||
.3.(59) |
. |
|
KrP |
|
rPrP |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Если считать теплоемкости C и C постоянными, то
Pv
qP CP T2 T1 è qv |
Cv T2 T1 , |
|
||
следовательно, |
|
|
|
|
qP qv CP T2 T1 Cv T2 T1 P v2 v1 . |
(5.6.3) |
|||
Из уравнения состояния |
|
|
|
|
pv = RT è pv |
= RT , |
|
||
1 |
1 |
2 |
2 |
|
откуда |
|
|
|
|
R T2 |
T1 |
P v2 v1 . |
(5.6.4) |
|
Учитывая (5.6.3), можно записать |
|
|
||
CP T2 T1 Cv T2 T1 R T2 T1 |
|
|||
èëè |
|
|
|
|
|
CP |
Cv |
R. |
(5.6.5) |
|
|
|
|
|
Уравнение (5.6.5) называется уравнением Майера.
Сравнивая (5.6.1) и (5.6.5), находим, что удельная газовая постоянная представляет собой работу, совершаемую 1 кг газа при изменении температуры на 1°С в процессе при постоянном давлении.
Если (5.6.5) умножить на молекулярную массу Π, то получим зависимость между мольными теплоемкостями
|
|
|
|
|
|
ΠCP ΠCv |
ΠR, |
(5.6.6) |
|
|
|
|
|
|
|
|
|
ãäå ΠR 8314 |
Äæ |
. |
|
|
||||
|
|
|
||||||
кмоль К |
|
|
||||||
|
|
|
|
|
|
|
|
|
 |
термодинамике часто используется соотношение |
|||||||
|
CP |
|
ΠCP |
k, называемое показателем адиабаты. |
|
|||
|
Cv |
ΠCv |
|
|||||
|
|
|
|
|
|
|||
При проведении расчетов, связанных с идеальными газами, зна- чение мольных теплоемкостей часто принимают на основании данных молекулярно-кинетической теории газов. По этой теории мольные теплоемкости идеальных газов не зависят от температуры, а являются функцией только их атомности (табл. 5.6.1). Для реальных газов величина k зависит от температуры и давления.
5.5. Зависимость теплоемкости от температуры.
Истинная и средняя теплоемкости
Теплоемкость идеальных газов зависит от следующих факторов: от физических свойств газов, от условий, при которых протекает процесс изменения состояния, и от температуры. Теплоемкость реальных газов зависит, кроме того, и от давления.
Рассмотрим зависимость теплоемкости от температуры. Опыты показывают, что количество тепла, затрачиваемого на нагревание единицы количества газа на одинаковое число градусов при различ- ных температурах, различно. Так, например, для нагревания единицы количества вещества от 0 до 100°С требуется одно количество тепла, а для нагревания от 100 до 200°С – другое, обычно больше первого. Это значит, что теплоемкости для интервалов различных температур неодинаковы.
Зависимость теплоемкости от температуры можно выразить графически (рис. 5.5.1).
Различают среднюю и истинную теплоемкости.
Средней теплоемкостью C называется отношение теплоты q, подведенной или отведенной в процессе, к изменению температуры (t – t ) при условии, что разность температур является конечной ве-
21
личиной.
Допустим, что для нагревания 1 кг газа затрачено q Дж тепла, при
этом температура газа повысилась от t до t , тогда средняя тепло-
1 |
2 |
емкость в интервале температур от t до t |
определится из уравне- |
1 |
2 |
íèÿ
|
|
|
t2 |
|
q |
, |
Äæ |
. (5.5.1) |
|
C |
|
||||||||
t1 |
t2 |
t1 |
êã ãðàä |
||||||
|
|
|
|
|
|||||
|
|
|
|
|
|
||||
Если разность температур (t – t ) бесконечно мала и в
21
пределе стремится к нулю, то получаем истинную теплоемкость, которую можем записать так:
C |
|
|
1χ |
|
2 |
|
|
|
1 |
|
2χ |
|
|
|
Oχ |
|
|
|
|
C |
|
C |
2 |
C |
|
|
|
|
|
1 |
|
|
O |
|
|
a |
|
b |
|
|
t |
t |
|
|
1 |
t |
|
|
|
|
|
2 |
|
|
Ðèñ. 5.5.1 |
|
76 |
73 |