участок c-d – перегреву пара до за- |
P |
|
|
|
|
|
|
|
|
|
|
данной температуры. Таким обра- |
|
|
l |
|
|
|
|
|
зом, на графике вычислены v , vχ, vσ, |
|
|
|
k |
|
|
0 |
|
|
|
|
соответствующие удельным объе- |
|
|
|
|
мам жидкости при 0°С, кипящей жид- |
|
a |
b |
c |
|
2 |
|
2 |
|
2 |
|
|
|
|
|
|
|
|
a |
b |
c |
кости и сухого насыщенного пара. |
|
|
1 |
1 |
1 |
|
|
|
|
|
При подогреве жидкости удель- |
|
a |
b |
c |
|
|
|
|
ный объем ее несколько увеличива- |
|
|
|
|
ется вследствие температурного |
|
|
|
|
расширения, процесс же парообразо- |
|
|
|
v |
|
|
|
|
вания характеризуется резким увели- |
|
|
Ðèñ. 8.1.2 |
чением удельного объема. |
|
|
|
|
|
|
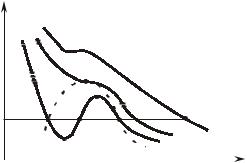
Построив в Pv-диаграмме (рис. 8.1.2) аналогичные графики для |
нескольких различных давлений и соединив одноименные точки плав- |
ными линиями, можно заметить, что в связи с очень малой сжима- |
емостью жидкости линия a-a -a -…, выражающая зависимость |
|
|
1 |
2 |
|
|
|
|
v = f (P), практически вертикальна; в связи с тем, что при увеличе- |
0 |
|
|
|
|
|
|
|
нии давления возрастает температура кипения, от которой зависит |
vχ, линия b-b -b -…, выражающая зависимость vχ = f (P), идет круто |
1 |
2 |
|
|
|
|
|
|
вверх с наклоном в правую сторону; наконец, линия c-c -c -…, выра- |
|
|
|
|
|
|
1 |
2 |
жающая зависимость vσ = f (P), имеет гиперболический характер. |
Линия b-b -b -…, отделяющая область жидкости от области |
1 |
2 |
|
|
|
|
|
|
влажного пара и характеризуемая равенством x = 0, называется ниж- |
ней пограничной кривой; линия c-c -c -…, отделяющая область влаж- |
|
|
|
1 |
2 |
|
|
|
ного пара от области пара перегретого и характеризуемая равен- |
ством x = 1, называется верхней пограничной кривой. |
|
С ростом давления разность vσ – vχ уменьшается и пограничные |
кривые сближаются, плавно сходясь в критической точке k, где они |
обе принимают горизонтальное направление. |
|
|
Как видно из графика (рис. 8.1.2), точка k соответствует некото- |
рому предельному состоянию вещества, при котором исчезает ви- |
димое различие между жидкостью и паром. |
|
|
Критические параметры, характеризующие это состояние для |
каждого вещества, имеют определенные значения. Так, например, |
äëÿ âîäû P = 221,15 áàð, t |
= 374,12°Ñ, v |
= 0,003147 ì3/êã. |
êð |
|
êð |
|
|
êð |
|
|
Линия k-l – условная граница между жидкостью и перегретым |
паром, соответствующая пиковым значениям теплоемкости C . |
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
|
109 |