|
à) |
h |
á) |
|
|
|
P |
P |
|
|
1 |
2 |
|
|
|
T |
1 |
2 |
T |
2 |
|
|
|
|
|
1 |
|
|
|
|
|
|
k |
|
x = 1 |
|
|
|
S |
|
S |
|
|
|
|
Ðèñ. 11.2.2 |
|
|
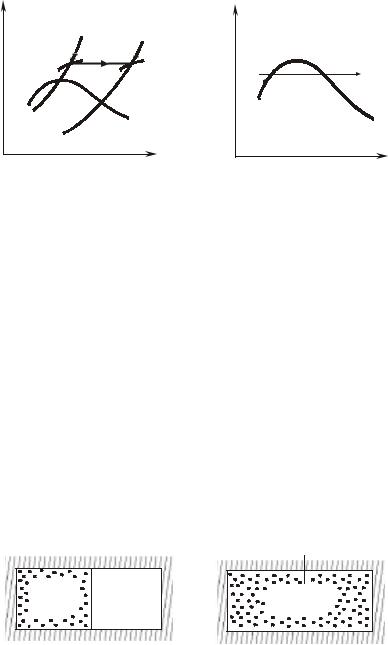
ных паров вначале происходит их некоторое увлажнение, а затем подсушка и перегрев (рис. 11.2.1, б).
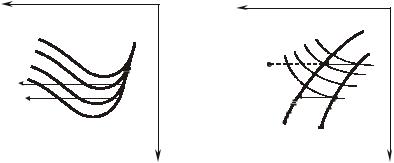
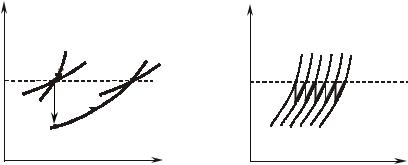
Уменьшение давления и температуры при дросселировании перегретого газа низкого давления приводит к увеличению его объема, энтропии и степени сухости (рис. 11.2.2, а); перегретый пар высокого давления превращается сначала в насыщенный, а затем вновь
âперегретый (рис. 11.2.2, б).
11.3.Адиабатное расширение реального газа
âвакуум (процесс Джоуля)
Рассмотрим еще один типичный необратимый процесс в реальном газе – адиабатное расширение газа в вакуум без отдачи внешней работы.
Рассматривается сосуд, разделенный выдвигающейся перегород-
кой на две части – одну, заполненную газом объемом V , с темпера-
1
турой T , давлением P , и другую, имеющую вакуум V , P = 0 (рис. 11.3.1). Сосуд снабжен идеальной теплоизоляцией, исключающей теплообмен с внешней средой.
P |
V |
T |
P = 0 |
|
1 |
1 |
|
1 |
|
|
|
V |
|
|
|
âàê |
|
Ðèñ. 11.3.1 |
Глава 11
СПОСОБЫ ПОЛУЧЕHИЯ HИЗКИХ
ТЕМПЕРАТУР
11.1. История получения низких температур
Писатель-сатирик Дж. Свифт в книге «Путешествия Гулливера» (вышедшей в 1726 г.) привел описание одной из лабораторий Академии в Логадо.
В распоряжении ученого, известного в Академии «под именем универсального искусника», находятся «две большие комнаты, наполненные диковинами, и 50 помощников. Одни сгущают воздух в вещество сухое и осязаемое…».
Мог ли сатирик предположить, что высмеиваемая разработка «бесплодной» идеи когда-либо станет актуальной проблемой, а превращение воздуха в вещество «сухое и осязаемое» станет реальностью (в те времена не был даже известен состав воздуха). Здесь решающая роль принадлежит низким температурам.
К 1877 г. ученые сконденсировали многие газы. Оставались шесть газов (O , NO, N , H , CH ,CO) из известных к тому времени – не
22 2 4
ожиженных. В декабре 1877 г. С. Кайете во Франции и Р. Пикте в Швейцарии почти одновременно удалось впервые ожижить кислород. Последним из этой группы был ожижен водород Дж. Дьюаром в 1898 г.
Стало известно о существовании гелия (трудно ожижаемый). Только в 1908 г. его ожижение произвел Камерлинг-Оннес в Голландии. Была достигнута температура, всего на 4 К отличающаяся от абсолютного нуля (использовалось ваккуумирование парового пространства). В 1909 г. он же путем снижения давления получил температуру гелия 1,38 К, а затем 1,04 К (вакуумные насосы больше не уменьшали давление).
Штурм низких температур продолжался в космонавтике (важно для промышленности – сверхпроводимость веществ в металлургии, электротехнике).
В 1895 г. Линде в Германии и Хэмпсон в Англии решили задачу получения ожиженных газов в количествах, достаточных для прак-
145