Материал: Белозеров В.И., Жук М.М., Кузина Ю.А., Терновых М.Ю. Физика и эксплуатационные режимы реактора ВВЭР-1000
1.4.Строение атома
В1913 г. была разработана новая модель атома, за основу которой была принята планетарная модель Резерфорда с двумя постулатами:
1.Электроны, движущиеся в атомах по отдельным, стационарным орбитам, не излучают электромагнитных волн, а энергия электронов
принимает дискретный ряд значений W1, W2, ..., Wn.
2.При переходе электрона с одной орбиты на другую энергия электрона изменяется скачком на величину:
W = Wn2 – Wn1, |
(1.4.1) |
где Wn1 и Wn2 – начальная и конечная энергия электрона.
Если W > 0, то атом поглощает энергию, если W < 0 – атом испускает фотон с частотой ν = W/h.
По теории Бора электроны в атоме сгруппированы по электронным оболочкам, номера которых возрастают по мере их удаления от ядра. Номер оболочки n = 1, 2, 3, ... называют квантовым числом. Электронные оболочки с квантовыми числами п = 1, 2, 3, 4, 5, 6, ... обозначают соответственно буквами K, L, M, N, O, P, ... Так, первая оболочка (п = 1) K-оболочка и т.д. Электроны п-й оболочки характеризуются одинаковой энергией Wn, которую обычно отсчитывают от суммарной энергии покоя ядра и всех атомных электронов.
На электрон действует не только сила притяжения ядра, но и сила отталкивания других электронов, которая ослабляет связь электрона с ядром. Чем дальше электронная оболочка от ядра, тем экранировка электронов больше. В многоэлектронных атомах электроны K- и L-оболочек наиболее крепко связаны в атоме.
У атома большое число электронных оболочек. Небольшая доля оболочек заполнена полностью или частично электронами, а на остальных оболочках электронов нет. Если на атом не действуют внешние силы, то электроны в атоме располагаются на самых близких к ядру оболочках. В каждой n-й оболочке может быть не более 2п2 электронов. При таком расположении электронов энергия атома минимальна, что обеспечивает длительное устойчивое состояние атома. Это состояние атома называют основным, а энергию атома – основным энергетическим уровнем (основным уровнем). Если на атом действуют внешние силы (неупругие столкно-
21
вения с другими атомами, свободными электронами и т. д.), то электрон может получить определенную порцию энергии и перейти на вакантное место одной из внешних оболочек. Такое состояние атома называют возбужденным, а его энергию – возбужденным энергетическим уровнем (возбужденным уровнем). Если с оболочки электрон удаляется из атома, то атом ионизируется.
Возбужденный атом неустойчив. Время его жизни составляет примерно 10-8 с. Затем электрон переходит на более близкую к ядру оболочку, и атом возвращается в основное состояние. Во время перехода возбужденного атома в основное состояние испускаются фотоны.
Ядро и атом относятся к связанным системам частиц. В таких системах частицы удерживаются силами притяжения. Связь частицы в системе характеризуется энергией связи εа. Она равна энергии, которую необходимо затратить для удаления частицы из системы (например, электрона из атома). Энергия связи системы частиц Wa равна энергии, необходимой для разрыва связей между всеми частицами системы. После возвращения частицы в связанную систему частиц освобождается энергия.
1.5. Атомные спектры
Линейчатые спектры атомов отражают строение электронных оболочек атомов. В любом атомном спектре наблюдаются определенные закономерности. Атомный спектр состоит из ряда серий оптического и рентгеновского излучения. С увеличением частоты излучения каждая серия заканчивается граничной линией, по направлению к которой линии серии сгущаются, а их интенсивность падает.
Электромагнитное излучение испускается только возбужденными атомами. При переходе электрона с оболочки п2 на оболочку n1 (n2 > n1) испускается фотон с энергией h = – W.
Энергия электронов в оболочках атома изображают в виде диаграмм (рис. 1.3). Они состоят из ряда горизонтальных линий, расположенных друг над другом. Расстояние n-ой горизонтальной линии до начала отсчета пропорционально энергии Wn. Около линий наносят энергии Wn и квантовые числа n. Вертикальные стрелки показывают возможные переходы электронов в возбужденном ато-
22
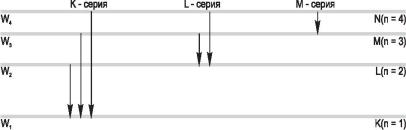
ме. При переходах электронов на K-оболочку испускается K-серия, на L-оболочку – L-серия и т. д.
Рис. 1.3. Энергия электрона в оболочках атома и серии характеристического рентгеновского излучения
Каждый переход электрона в возбужденном атоме сопровождается испусканием одного фотона. Поэтому при многократных переходах электрона в возбужденном атоме возникает несколько фотонов. Так, если на свободное место в K-оболочке переходит электрон сразу из внешней оболочки, то испускается один фотон. Если на K- оболочку попадает сначала электрон с L-оболочки, а на последнюю
– электрон с внешней оболочки, то испускаются два фотона и т. д. Отметим, что переход электрона с одной оболочки атома на
другую соответствует переходу атома с одного энергетического уровня на другой. При этом энергии электрона и атома изменяются на одну и ту же величину.
Простейшим атомом является атом водорода. Ядро водорода – протон – обозначают буквой р, масса протона mp = 1,00727 а.е.м. в 1936 раз больше массы электрона. Положительный заряд протона равен элементарному электрическому заряду 1,6 10-19 Кл.
Спектр излучения водорода по теории Бора описывается соотношением:
|
1 |
|
1 |
|
|
|
ν = cR |
|
− |
|
|
, |
(1.5.1) |
2 |
2 |
|||||
n1 |
|
n2 |
|
|
|
|
где R = 10973731 м-1 – постоянная Ридберга; с – скорость света, м/с. Возбужденные атомы водорода испускают серию Бальмера при переходах электронов с оболочек п2 = 3, 4, 5,... на L-оболочку (n = 2). Эта серия была известна экспериментаторам до теории Бора. По
23

соотношению (1.5.1) Бор предсказал несколько серий излучения водорода, которые были найдены впоследствии экспериментально. Совпадение теории и эксперимента по спектру водорода подтвердило справедливость постулатов Бора об особенностях движения электронов в атоме.
Спектр многоэлектронных атомов имеет очень сложное строение. Эта сложность обусловливается экранировкой электронов в атоме, которая изменяется по мере удаления электронной оболочки от ядра.
Атомы испускают рентгеновское излучение при переходах электронов на внутренние оболочки. С переходами электронов на внешних оболочках связано оптическое излучение, которое подразделяется на ультрафиолетовое, световое и инфракрасное.
Каждый элемент имеет отличное от других элементов расположение линий в рентгеновском спектре. Строение рентгеновского спектра, отражающее свойства внутренних электронных оболочек, является характеристикой атома. Поэтому линейчатый рентгеновский спектр элементов называют характеристическим.
1.6. Основы квантовой механики
Классическая физика рассматривает законы макроскопического мира (макромира). Квантовая механика рассматривает законы микромира. По квантовой теории свет – это фотоны с энергией E и импульсом р:
E= hν,
(1.6.l)
p = λh .
Левые части (энергия, импульс) системы (1.6.1) являются признаками частицы (корпускулы), а правые части (частота и длина волны λ = c/ν) – электромагнитной волны. В записи системы (1.6.1) отражается дуализм (волна – частица) света. Свет, с одной стороны, похож на газ, состоящий из фотонов с энергией E и импульсом р. С другой стороны, он представляется непрерывной электромагнитной волной с частотой ν. В различных условиях эксперимента свет проявляет или корпускулярные, или волновые свойства.
Кинетическая энергия и импульс тела связаны с частотой и длиной волны уравнениями (1.6.1). Длину волны движущихся тел на-
24
ходят из второго уравнения, в котором импульс р заменен произведением релятивистской массы m на скорость v:
λ = |
h |
. |
(1.6.2) |
|
|||
|
mv |
|
|
С увеличением массы тела длина волны стремится к нулю. У макроскопических тел она несравнимо меньше размеров самих тел даже при самых незначительных скоростях.
В квантовых явлениях существенное влияние на движение оказывают волновые свойства частиц. Длина волны частиц, особенно при небольших скоростях, сравнима с размерами атомов и молекул. Поэтому микрочастицы, взаимодействуя между собой, в одних случаях ведут себя как волны, а в других (высокие скорости) – как частицы. Это одна из особенностей микромира.
Вторая особенность микромира – дискретность механических и магнитных величин (энергии момента количества движения и др.) связанных частиц (атома, ядра и т. п.). Если в макромире эти величины изменяются непрерывно, то в микромире они могут принимать только отдельные, дискретные значения.
Отличительная черта микромира – атомизм строения элементарных (простых) и сложных частиц. Атомизм выражается в том, что каждая частица (электрон, протон и т. д.) характеризуется своей массой, зарядом и т.д. Элементарные частицы возникают и уничтожаются не по частям, а как единое целое. Сложные частицы (атом, ядро) образуются из определенных элементарных частиц. Их можно раздробить на эти же элементарные частицы. Сложные частицы существуют только как целое. Достаточно удалить из них хотя бы одну элементарную частицу, как свойства сложной частицы изменятся. Например, атом является носителем химических свойств элемента, в то время как ион атома – заряженная частица – такими свойствами не обладает.
К предмету рассмотрения квантовой механики относятся закономерности движения в микромире. Квантовая механика отражает качественно новую ступень познания природы, поэтому она оперирует новыми понятиями. Часть понятий, таких, как импульс, момент количества движения, магнитный момент и др., она заимствовала из классической физики. Однако в квантовой механике у них другое содержание.
25