Материал: Белозеров В.И., Жук М.М., Кузина Ю.А., Терновых М.Ю. Физика и эксплуатационные режимы реактора ВВЭР-1000
В квантовой механике особую роль играет постоянная Планка. Она входит в выражения для всех величин, характеризующих квантовые явления (энергия фотона, длина волны частиц и т. д.). Если при рассмотрении какого-либо движения можно пренебречь этими величинами, то движение подчиняется классическим законам. Например, при движении макроскопических тел нет смысла учитывать их длину волны λ = h/mv. Поэтому законы классической механики являются предельным случаем законов квантовой механики при переходе от микромира к макромиру.
1.7. Квантовые состояния электронов в атоме
Квантовое состояние электрона в атоме описывается энергией, моментами количества движения и магнитными моментами, которые могут принимать только дискретные значения. Иначе говоря, все эти величины в атоме квантуются. Электроны оболочки с номером n движутся с одной и той же энергией. Числа n = 1, 2, 3, как и в теории атома Н. Бора, характеризуют дискретные энергетические состояния электронов и номер электронной оболочки. В квантовой механике число n называют главным квантовым числом.
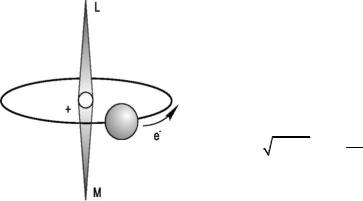
Движение электрона по орбите характеризуется орбитальным моментом количества движения L. Он направлен по оси вращения электрона, перпендикулярно к плоскости орбиты (рис. 1.4). Модуль орбитального момента принимает дискретные значения:
Рис. 1.4. Относительное положение орбитального момента количества движения L и магнитного момента M электрона
L = = l(l +1), = = 2hπ . (1.7.1)
Целое число l называют орбитальным квантовым числом. Для n-ой оболочки оно принимает значения от 0 до n–1. Возможное число значений орбитального квантового числа в n-й оболочке равно n. В K-оболочке орбитальное квантовое число может
26

быть только равным нулю. Для орбитального движения это кажется противоречивым. Все объясняется тем, что электрон с l = 0 не имеет определенной орбиты. Его с равной вероятностью можно найти в любой точке поверхности сферы с радиусом оболочки. Так как орбитальный момент имеет направление в пространстве, то при равновероятном движении электрона по сфере среднее значение орбитального момента равно нулю.
В L-оболочке (n = 2) орбитальное квантовое число принимает два значения: 0 и 1. Электрон с l = 0 движется равновероятно по сфере в L-оболочке, как и в K-оболочке. Орбитальное движение электрона с l = 1 имеет более определенную ориентацию в про-
странстве. Среднее значение модуля L при n = 1 равно = 2 .
В M-оболочке (n = 3) модуль момента количества движения принимает три значения: 0, = 2,= 6 . Состояния электронов n-й
оболочки с различными орбитальными квантовыми числами несколько отличаются друг от друга. Поэтому n-я оболочка расслаивается на n подоболочек электронов. Они характеризуются одним главным, но различными орбитальными квантовыми числами.
Орбитальное движение электрона можно рассматривать как круговой электрический ток. За направление тока принимают направление перемещения положительных зарядов. Поэтому орбитальный ток течет против движения электрона. Круговой ток создает магнитное поле (см. рис. 1.4) с магнитным моментом M. Он направлен в противоположном направлении относительно момента L. Магнитный момент M также квантуется. Его модуль принимает значения, пропорциональные магнетону Бора:
μ0 = |
e= |
= 9,27 10−24 Дж/К. |
(1.7.2) |
|
|||
|
2me |
|
|
Магнитный и орбитальный моменты пропорциональны, поэтому возможные значения модуля магнитного момента равны:
M = μ0 |
l(l +1) = |
eL |
. |
(1.7.3) |
|
||||
|
|
2me |
|
|
Теперь можно рассмотреть, что же произойдет, если атом поместить в магнитное поле, напряженность которого направлена по оси z.
27
Магнитное поле ориентирует орбитальные магнитные моменты в определенных направлениях. Для магнитной стрелки компаса, например, существует одно устойчивое направление, когда ее магнитный момент направлен по полю. Другое дело – в микромире. Магнитный момент располагается так, что проекция орбитального момента на ось z принимает значения, кратные h. Например, орби-
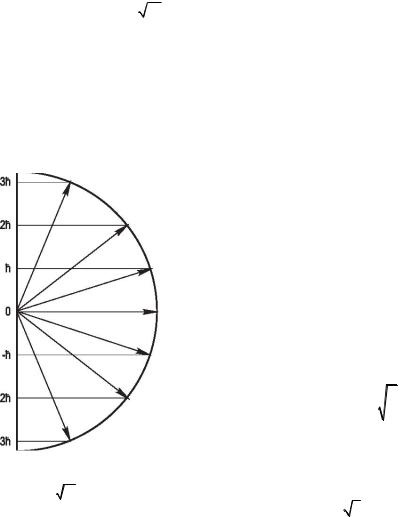
тальный момент L = = 12 ... (l = 3) может иметь семь ориентаций в пространстве, при этом проекция орбитального момента на направление поля принимает значения: –3h, –2h, –h, 0, +h, +2h, +3h (рис. 1.5). Проекции момента Lz на ось z записывают кратко m=. Число m называют магнитным квантовым числом. Для каждого орбитального момента оно принимает 2l + 1 целочисленных значений в единицах h: от –1 до +1.
По своей размерности константа h совпадает с размерностью действия (момент количества движения, произведение энергии на время). Эта константа принята в квантовой механике за единицу измерения действия и названа квантом действия.
Экспериментально измеряют, например, не сам модуль момента L, а его проекцию Lz, которая всегда кратна h.
|
Электрон имеет еще и собственное |
|
вращательное движение с моментом |
|
количества движения S, называемым |
|
спином. Электрон условно можно |
|
представить как волчок, вращающийся |
|
вокруг своей оси. Спин электрона при- |
|
нимает одно значение, равное = 3 . |
|
2 |
|
Вращение электрона как заряда во- |
Рис. 1.5. Возможные значения |
круг своей оси создает подобие круго- |
проекций орбитального |
вого тока. Собственный магнитный |
момента = 12 на направление |
момент электрона направлен противо- |
магнитного поля (l = 3) |
положно спину и равен μ0 3 . |
|
28 |
Ориентация спина электрона в магнитном поле обуславливается ориентацией собственного магнитного момента. Последний устанавливается в пространстве так, что проекция спина S на направление магнитного поля может принимать два значения: – =/ 2 и =/ 2 . Возможные проекции спина записывают одним выражением:
Sz = mz= . |
(1.7.4) |
Число mz, равное 1/2 и –1/2 , называют спиновым квантовым числом.
При рассуждениях о движении связанных электронов и других частиц ради простоты моменты L, S и M заменяют обычно их максимальными проекциями =l, =/ 2, μ0l и т. д. Такие упрощения ис-
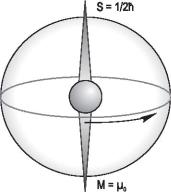
пользуются в дальнейшем тексте. Так, на рис. 1.6 изображен электрон и указаны максимальные проекции спина =/ 2 и собственного магнитного момента μ0.
Квантовое состояние электронов в |
|
|||
атоме характеризуется |
четырьмя |
|
||
квантовыми числами: главным п, ор- |
|
|||
битальным l, магнитным m и спино- |
|
|||
вым mz. Для объяснения состава и |
|
|||
строения электронных оболочек атома |
|
|||
швейцарский физик Паули в 1924 г. |
|
|||
сформулировал общий принцип, на- |
|
|||
званный принципом Паули. Иногда |
|
|||
его называют запретом Паули. По |
|
|||
принципу Паули двум электронам за- |
|
|||
прещается |
находиться в |
одинаковых |
Рис. 1.6. Относительное |
|
квантовых |
состояниях. |
Это значит, |
||
положение собственного |
||||
что квантовые состояния любых двух |
||||
момента количества движения |
||||
электронов в атоме отличаются друг |
(спина) и магнитного момента |
|||
от друга хотя бы одним квантовым |
электрона |
|||
числом из четырёх. |
|
|
||
Максимальное число электронов в п-й оболочке равно сумме
членов прогрессии, т. е. |
|
2 + 2(2n −1) n = 2n2 . |
(1.7.5) |
2 |
|
29 |
|
1.8.Соотношения неопределенностей
Вклассической механике траектория движения тела характеризуется его точными координатой x(t) и импульсом p(t) в любой момент времени t, причем обе величины взаимосвязаны. Например, равномерное прямолинейное движение тела массой m со скоростью
vописывается координатой x(t) = vt, импульсом р = mv. Отсюда
следует, что x(t) = р t/m.
Вмикромире частицы проявляют при одних условиях волновые свойства, при других – корпускулярные. Исходя только из корпускулярных свойств, как в теории атома Н. Бора, можно найти точное месторасположение частицы в пространстве. Однако такой вывод не отражает волновых свойств частицы. Так как волновой процесс заполняет большое пространство, то понятие координаты волны не имеет физического смысла.
Вквантовой механике с учетом волновых свойств частиц показывается, что у частицы не существует одновременно точных координат и импульса и что обе величины не связаны между собой. Если импульс частицы имеет точное значение, то ее местоположение неопределенно, и наоборот. Такая закономерность микромира отражается соотношением неопределенностей. Его иначе называют соотношением Гейзенберга, по фамилии немецкого физика, впервые сформулировавшего его. По соотношению Гейзенберга произ-
ведение неопределенности импульса р на неопределенность коор-
динаты x примерно равно постоянной Планка =: |
|
p x ≈ =. |
(1.8.1) |
Разделив последнее выражение на массу частицы m и учитывая, что р = m v, получится соотношение Гейзенберга для неопреде-
ленности скорости v и координаты |
х: |
|
|
v x ≈ |
= |
. |
(1.8.2) |
|
|||
|
m |
|
|
Соотношение Гейзенберга, отражая природу микромира, ограничивает наши знания об одновременном местоположении и импульсе частицы. Эти ограничения не зависят от точности измерительных приборов.
По соотношению Гейзенберга неопределённость скорости электрона:
30