Материал: Белозеров В.И., Жук М.М., Кузина Ю.А., Терновых М.Ю. Физика и эксплуатационные режимы реактора ВВЭР-1000
килограммах, численно равному его молекулярной (атомной) массе. Например, килограмм-моль углерода равен 12,01115 кг, берил-
лия – 9,0122 кг, воды – 18,0154 кг и т.д.
Масса атома (молекулы) сравнима с массой 10-26 кг. Такие малые величины измеряют специальными приборами, которые были изобретены сравнительно недавно. До появления этих приборов массы атомов и молекул выражали в относительных единицах. Отношение массы атома (молекулы) к атомной единице массы называют относительной атомной (молекулярной) массой [кратко: атомная (молекулярная) масса]. Согласно определению эта величина безразмерная. Она показывает, во сколько раз масса атома (молекулы) больше атомной единицы массы. Атомную массу обозначают буквой А, молекулярную – буквой μ. В килограмм-моле любого однородного вещества содержится число молекул NA, равное 6,02 1026 мол./кмоль. Величину NA называют числом Авогадро. По числу Авогадро и килограмм-молю углерода рассчитывается атомная единица массы:
1 а.е.м.= |
|
1 |
|
AC |
= |
|
1 |
|
12 |
=1,66 10–27 кг. (1.1.1) |
|
12 |
NA |
12 |
6,02 1026 |
||||||||
|
|
|
|
|
|||||||
Количество частиц (молекул, атомов), заключенных в 1 м3 однородного вещества, называют плотностью частиц N. Ее находят по известным плотности вещества ρ (кг/м3), молекулярной μ (атомной А) массе и числу Авогадро:
N = |
ρ NA. |
(1.1.2) |
|
μ |
|
При расчете величины N часто используют приближенные значения μ и А, ограниченные первыми тремя цифрами.
Если известны плотность и химическая формула молекулы вещества, то легко рассчитать число атомов любого элемента в 1 м3 вещества:
N |
|
= n ρ N |
|
, |
(1.1.3) |
|
i |
i μ |
A |
|
|
где ni – число атомов i-го элемента в молекуле.
В атомной физике за единицу длины принят ангстрем (Å), равный 10-10 м. В этих единицах диаметр молекулы воды d равен при-
мерно 3,86 Å.
11
Атомизм строения наблюдается не только у вещества, но и у электричества. Элементарный электрический заряд е = 1,6 10-19 Кл. Любой электрический заряд кратен е и не может быть меньше его. Существуют положительный и отрицательный элементарные электрические заряды. Носителем элементарного отрицательного заряда является электрон, масса которого те = 9,1 10-31 кг = 5,5 10-4 а.е.м., удельный заряд е/m = 1,76 1011 Кл/кг. Элементарный положительный заряд имеет позитрон. У него такие же масса и удель-
ный заряд, как и у электрона. Позитрон обозначают символом е+, электрон – е–.
1.2. Вероятность и спектр
Природные события (явления) подразделяют на достоверные и случайные. Достоверное событие – это такое событие, которое обязательно происходит при выполнении S условий. Событие называют случайным, если в определенных условиях оно или происходит, или нет. Например, подброшенная монета падает на землю или гербом, или цифрой вверх. Выпадение герба и цифры – случайные события.
Закономерности множества случайных событий, выпадающих при определенных условиях, изучает теория вероятностей. Одним из основных понятий теории вероятностей является понятие вероятности появления события.
Допустим, что в опыте при одинаковых условиях наблюдают случайные события А (i = 1,2, ..., k). Пусть событие А1 выпадает n1 раз, событие А2 – п2 раз и т.д., а общее число событий п = п1 + п2+ +...+ пk достаточно велико. Вероятностью события Ai называют величину f(Ai), равную доле событий Ai, в общем количестве событий:
f(Ai) = |
ni |
. |
(1.2.1) |
|
|||
|
n |
|
|
По известной вероятности f(Ai) предсказывают возможность появления события Ai. Так, если монету бросают вверх в одинаковых условиях, то вероятности выпадения герба и цифры равны 0,5.
Из определения вероятности f(Ai) следует, что сумма всех вероятностей:
12
k |
|
∑ f (Ai ) = f (A1) + f (A2 ) + ... + f (Ak ) = 1. |
(1.2.2) |
i=1
Следовательно, при выполнении заданных условий одно из k событий обязательно происходит. Необходимо отметить, что вероятность достоверного события равна единице, а невозможного – нулю.
Аналогично случайным событиям определяются случайные физические величины. К ним относятся такие физические величины, которые принимают различные значения в одних и тех же условиях. Например, скорость молекулы газа – случайная величина. При давлении газа 1 атм молекула испытывает около 108 столкновений за секунду с другими молекулами, после каждого из которых ее скорость изменяется. Поэтому можно говорить лишь о вероятности того или иного значения скорости молекулы.
Теорию вероятностей применяют в различных областях науки и техники. В физике ее используют, например, для описания спектра физической величины.
В природе существует огромное количество систем (множеств) частиц, объединенных или силами притяжения, или другими условиями. Одна из таких систем частиц – газ, заключенный в замкнутом объеме (сосуде).
Килограмм-моль любого газа при нормальных условиях (давление равно 760 мм рт.ст., температура t = 0 °C) занимает объем, равный 22,4 м3. При этих условиях плотность молекул всех газов одинакова. Она находится как частное от деления числа Авогадро на объем килограмм-моля газа и равна 2,7 1025 мол./м3. Из сравнения плотностей молекул воды и газа следует, что расстояние между молекулами газа намного превышает их размеры.
Молекулы вещества находятся в состоянии непрерывного движения, называемого тепловым. В процессе теплового движения молекулы газа часто сталкиваются друг с другом. При нормальных условиях молекула газа пробегает от столкновения до столкновения в среднем 10-8 м. Во время столкновения между молекулами происходит обмен энергией, при котором более быстрые молекулы передают часть своей энергии более медленным. В результате огромного числа таких столкновений в замкнутом объеме газа устанавливается равновесное распределение молекул по скоростям.
13
Наряду с системой молекул газа, существуют и другие системы, в которых частицы характеризуются неодинаковыми массами, скоростями, энергиями, частотами и так далее. Под спектром физической величины (спектры масс, энергий, скоростей, частот) понимают распределение частиц системы по значениям этой физической величины. Так, распределение молекул газа по скоростям называют спектром скоростей, а распределение изотопов элемента по массам – спектром масс элемента.
Различают два типа спектров. Если в системе есть частицы с любыми значениями физической величины, то спектр называют сплошным (непрерывным). Если же в системе встречаются частицы только с отдельными значениями физической величины, то спектр называют дискретным (линейчатым). Примером дискретного спектра служит спектр масс элемента. В нем наблюдаются атомы с отдельными значениями массы. Распределение молекул газа по скоростям (спектр скоростей) относится к сплошному спектру.
Пусть частицы системы характеризуются случайной величиной L, изменяющейся непрерывно. Так как величина случайна, то не имеет смысла говорить о числе частиц с точным значением L. Это число неоднозначно и может быть даже равным нулю. Однако число частиц со значениями в интервале от L до L+dL вполне определенно и равно dN(L). Иначе говоря, dN(L) – это число частиц в интервале dL вблизи значения L. Число dN(L) пропорционально числу частиц в системе N0 и интервалу dL:
dN(L) = f(L) N0 dL. (1.2.3)
Коэффициент пропорциональности
f (L) = |
1 |
dN (L) |
(1.2.4) |
|
N0 |
||||
|
dL |
|
называют плотностью вероятности. Она зависит от L и равна доле частиц системы, отнесенной к единичному интервалу вблизи L. Функция f(L) характеризует также вероятность того, что частица имеет значение физической величины, заключенное в единичном интервале вблизи L. Под сплошным спектром физической величины понимают функцию f(L). Этот спектр нормирован на единицу, так как интеграл от функции f(L) по всем возможным значениям L равен единице:
14
∞ |
1 |
N0 |
|
||
∫ f (L)d(L) = |
∫ dN =1. |
(1.2.5) |
|||
N |
0 |
||||
0 |
0 |
|
|||
|
|
||||
Свойства систем частиц описываются средними значениями физических величин L, которые получаются с помощью усреднения по спектру физической величины:
∞
∫ Lf (L)dL
|
|
= |
0 |
. |
(1.2.6) |
|
L |
||||||
|
∞ |
∫ f (L)dL
0
Так как функция f(L) нормирована на единицу, то
|
|
∞ |
|
|
|
= ∫ Lf (L)dL . |
(1.2.7) |
L |
|||
0 |
|
||
Спектр скоростей f(v) молекул газа в ограниченном объеме впервые изучил Максвелл. По имени ученого функцию f(v) называют спектром Максвелла, или функцией распределения Максвелла. Аналитическая запись спектра Максвелла имеет вид:
|
3 |
|
|
−mv2 |
|
|
|
m 2 |
2 |
|
|
||
f (v) = 4π |
|
|
v |
e |
2kT , |
(1.2.8) |
|
||||||
|
2πkT |
|
|
|
|
|
где v – скорость молекулы, м/с; m – масса молекулы, кг; k = 1,38× ×10-23 Дж/К – постоянная Больцмана; Т – температура газа, К.
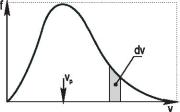
На рис. 1.1 приведен спектр Максвелла f(v). Однако большинство молекул движутся со скоростями, близкими к наиболее вероятной скорости vp, при которой спектр
Максвелла имеет максимум. Со скоростью v < vp движется около 42 % всех молекул. Поэтому средняя скорость молекул в 1,128 раза больше vp. Доля молекул в интервале dv вблизи скорости v изображена заштрихованной площадью столбика. Основание столбика равно dv, а средняя его высота – f(v).
15