чею. Регулює обмін кальцію-фосфору в організмі. |
кальцитоніну. Мішень — кісткова тканина, де |
Органи-мішені — кістки, нирки, шлунково-киш- |
пригнічується мобілізація кальцію. Посередник дії |
ковий тракт (зниження концентрації іонів каль- |
— Са2+-залежна АТФаза. |
цію спричинює секрецію гормону). Сприяє мобі- |
1. Кальцитонін змінює роботу кальцієвого |
лізації солей кальцію у вигляді цитратів із кістко- |
насоса. |
вої тканини в кров (інгібує ізоцитратдегідроге- |
2. Сприяє переходу кальцію з крові в кістко- |
назу і лужну фосфатазу). Стимулює остеоклас- |
ву тканину і сповільнює зворотний процес (впли- |
ти й остеобласти, причому вплив на остеоклас- |
ває на лужну фосфатазу). |
ти переважає, завдяки чому більше Са2+ мобілі- |
3. Підтримує нормальний рівень фосфору в |
зується з кістки (рис. 15.5). |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
крові та виділення фосфатів із сечею. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Кальцитонін захищає кістки матері від над- |
|
|
|
Зменшення в крові Са2+ |
|
|
|
|
|
|
|
|
|
мірної втрати кальцію під час вагітності. Утво- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
рення кісток немовляти та лактація є основними |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
споживачами запасів кальцію, тому рівень 1,25- |
|
|
|
Паращитоподібна залоза |
|
|
|
|
|
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
дигідроксихолекальциферолу під час вагітності |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
підвищений. Якби резорбцію кісток одночасно не |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пригнічувало збільшення рівня кальцитоніну в |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Паратгормон |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
плазмі, відбулася б втрата кісткової маси в ма- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тері. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Нирки |
|
|
|
|
|
|
Кістка |
|
|
|
|
|
|
|
|
|
Вітаміни D |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вітаміни D підсилюють синтез білка-перенос- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Реабсорбція Са2+ |
|
Вимивання Са2+ |
|
|
|
|
ника іонів Са2+ з просвіту кишечнику в кров; у |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
у вигляді цитрату |
|
|
нирках підсилюють реабсорбцію і Са2+, і Н3РО4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(за певних умов можуть бути синергістами як |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
паратгормону, так і кальцитоніну). |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Збільшення у крові Са2+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вітамін D3 є попередником кальцитріолу, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
який функціонує як гормон. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1,25-дигідроксихолекальциферол — це стероїд- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ний гормон, утворений з вітаміну D3 шляхом |
Зменшення виділення Са2+ із сечею |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
гідроксилювання в печінці та нирках, його пер- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
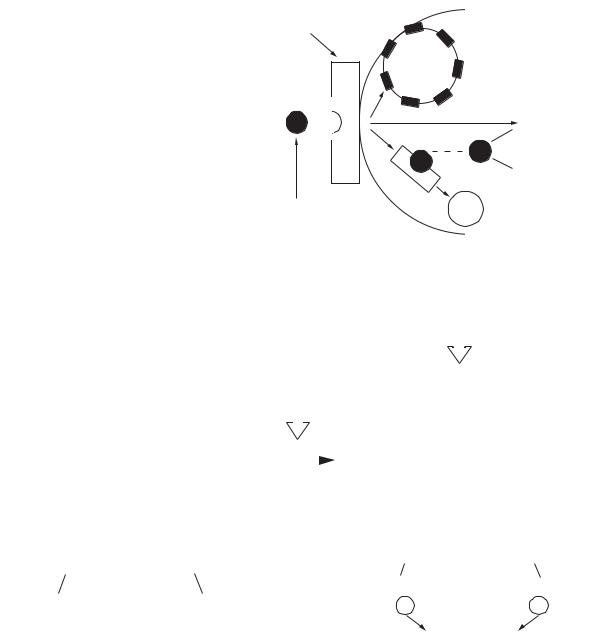
винною дією є збільшення абсорбції кальцію з |
|
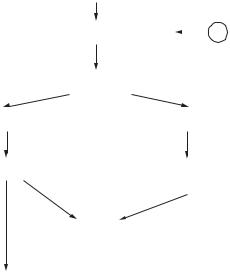
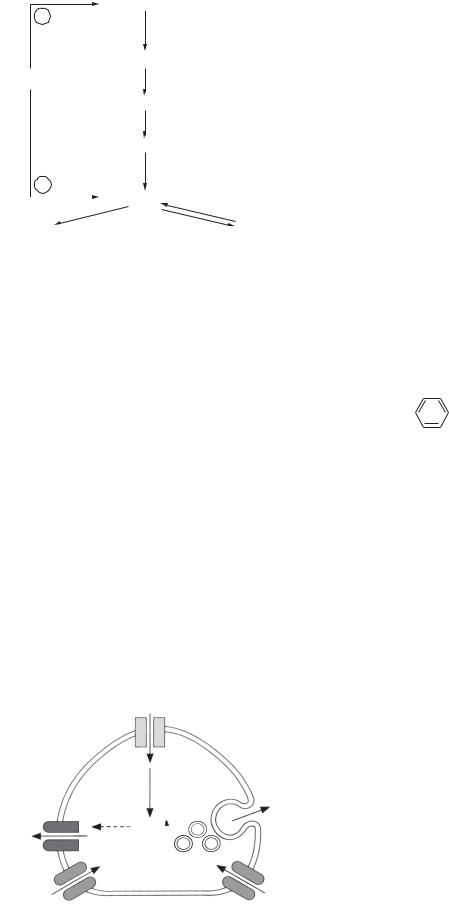
Рис. 15.5. Дія та регуляція паратгормону |
кишечнику (рис. 15.6). |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Перетворення вітаміну D на кальцитріол |
2. Зменшує реабсорбцію фосфатів у дисталь- |
відбувається за участю двох органів — печінки |
і нирок. Специфічні гідроксилази, які каталізують |
них канальцях і підвищує канальцеву реабсорб- |
ці реакції, активуються паратгормоном. При не- |
цію кальцію та магнію, що спричинює підвищен- |
стачі вітаміну D3 у дітей розвивається рахіт, у |
ня концентрації позаклітинного кальцію. |
|
|
|
|
|
|
|
|
|
дорослих — остеомаляція (порушення мінералі- |
3. Підвищує здатність ниркової тканини ут- |
зації D3 кісток, що ростуть), але є форми, які не |
ворювати 1,25-дигідроксихолекальциферол, який |
піддаються лікуванню вітаміном D3. Вони, ма- |
підсилює всмоктування кальцію в шлунково- |
буть, пов’язані з порушенням перетворення віта- |
кишковому тракті. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
міну D3 на кальцитріол (паренхіма нирок ушко- |
Гіпопаратиреоз — зниження рівня іонізова- |
джена). |
ного кальцію і підвищення рівня фосфатів у си- |
Надлишкове надходження вітаміну D3 при- |
роватці крові, що призводить до високої нейро- |
зводить до демінералізації кісток (виникають пе- |
м’язової збудливості, яка викликає судоми і те- |
реломи), підвищення концентрації кальцію в |
танічні скорочення. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
крові та відкладанню його в м’яких тканинах, |
Гіперпаратиреоз — надлишкова продукція |
утворення каменів у нирках. |
паратгормону виникає при аденомі паратиреоїд- |
Можна підсумувати дію трьох головних гор- |
них залоз або їх гіперплазії. У задавнених випад- |
монів, що регулюють концентрацію Са2+ в |
ках — резорбція скелета, різні ушкодження ни- |
плазмі. |
рок, зниження їхньої функції, інфікування сечо- |
Паратгормон збільшує концентрацію каль- |
вих шляхів. Розвиток гіперпаратиреозу зумовле- |
цію в плазмі, мобілізуючи цей іон із кісток. Він |
ний зниженням синтезу 1,25-(OH)2D3 |
|
|
з 25- |
збільшує реабсорбцію Са2+ нирками, однак це |
(OH)D3 у патологічно зміненій паренхімі нирок, |
може бути наслідком зростання кількості від- |
наслідком чого є порушення всмоктування каль- |
фільтрованого Са2+, а також посилює утворен- |
цію в кишечнику. Це порушення, в свою чергу, |
ня 1,25-дигідроксихолекальциферолу, який підси- |
спричинює вторинне вивільнення паратгормону. |
лює абсорбцію Са2+ з кишечнику, мобілізує іон |
Кальцитонін (тиреокальцитонін) — поліпеп- |
із кісток і збільшує реабсорбцію кальцію нирка- |
тид, кальцієзнижувальний гормон щитоподібної |
ми. |
залози, інгібує резорбцію кістки. Підвищення |
Кальцитонін пригнічує резорбцію кісток і |
вмісту кальцію в дієті веде до підвищення секреції |
зменшує кількість Са2+ в сечі. |