Материал: А27631 Бегунов АА методы и средства аналитических измерений
Ионоселективные электроды
|
Определяемый ион
|
Рабочий диапазон, моль/дм3
|
Нижний предел обнаружения, мг/дм3 |
Допустимый диапазон рН
|
Исполнение
|
|
К+ |
5·10–5–5·10–1 |
0,4 |
1–10 |
П |
|
Са2+ |
1·10–5–2·10–1 |
2,30 |
3–10 |
П |
|
Ва2+ |
5·10–5–5·10–1 |
1,40 |
1–10 |
П |
|
|
1·10–5–5·10–1 |
1,30 |
1–10 |
П |
|
|
5·10–5–2·10–1 |
1,00 |
1–10 |
П |
|
|
5·10–5–5·10–1 |
0,60 |
6–9 |
П |
|
Ca2+ Mg2+ |
5·10–5–2·10–1 |
0,01 мгэкв/л |
4–10 |
П |
|
NH4 |
5·10–5–2·10–1 |
0,20 |
1–9 |
П |
|
Анионные ПАВ |
1·10–5 – насыщ. |
0 |
1–10 |
П |
|
F– |
3·10–6–1·10–1 |
0,060 |
4–7 |
К |
|
Cl– |
5·10–5–1·10–1 |
0,350 |
0–13 |
К |
|
Br– |
5·10–5–1·10–1 |
0,400 |
0–13 |
К |
|
I– |
1·10–6–1·10–1 |
0,060 |
0–13 |
К |
|
CN– |
1·10–6–1·10–2 |
0,030 |
12–14 |
К |
|
CNS– |
1·10–5–1·10–1 |
0,600 |
2–10 |
К |
|
S2– |
3·10–6–1·10–1 |
0,003 |
3–14 |
К, Х |
|
Ag+ |
1·10–6–1·10–1 |
0,010 |
0–9 |
К, Х |
|
Hg2+ |
1·10–6–1·10–1 |
0,20; 0,02 |
0–2 |
К, Х |
|
Tl+ |
1·10–6–1·10–1 |
0,200 |
1–11 |
Х |
|
Fe3+ |
1·10–5–1·10–2 |
0,600 |
0–2 |
Х |
|
Cr6+ |
1·10–7–1·10–4 |
0,006 |
0–2 |
Х |
|
Cu2+ |
1·10–6–1·10–1 |
0,006 |
0–7 |
К, Х |
|
Pb2+ |
1·10–6–1·10–1 |
0,20; 0,02 |
2–7 |
К, Х |
|
Cd2+ |
1·10–6–1·10–1 |
0,10; 0,01 |
1–7 |
К, Х |
В табл. 5.1 введены следующие обозначения: П – пленочные электроды: электроды с поливинилхлоридной пленочной мембраной; К – кристаллические электроды: быстродействующие электроды с продолжительным рабочим ресурсом и стабильными характеристиками; Х – халькогенидные стеклянные электроды: оригинальные электроды со сферическими мембранами на основе халькогенидных стекол, они являются химически и коррозионно-устойчивыми в агрессивных средах и при высоких (до 1000 ºC) значениях температуры.
Схема потенциометрической установки показа на на рис. 5.2.
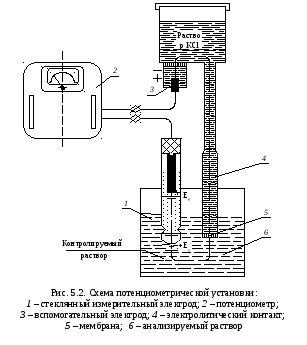
5.5. Измерение рН жидкостей
В ряде растворов вещества распадаются (диссоциируют) на ионы. Благодаря этому на электродах, опущенных в такой раствор, называемый электролитом, образуется потенциал, значение которого зависит от природы образующихся ионов и от их концентрации или активности в растворе. Это свойство используется для измерения содержания анализируемых веществ. Наибольшее распространение потенциометрический метод получил для измерения концентрации водородных ионов. Образование и растворение большей части осадков, как, например, сульфидов, карбонатов, фосфатов, зависит от концентрации водородных ионов. Многие процессы окисления и восстановления (в частности, биохимические) как неорганических, так и органических веществ нередко совершенно меняют свое направление при изменении концентрации водородных ионов. Коррозия металлов и образование защитных пленок также сильно зависят от кислотности или щелочности растворов, которые и характеризуются концентрацией этих ионов. В производстве соды и других минеральных солей, при флотационном обогащении руд, в пищевой промышленности, при дублении кожи, крашении тканей и в прочих производствах для правильной постановки технологического процесса также требуется учи-тывать влияние концентрации водородных ионов и уметь их определять.
На практике
концентрацию водородных ионов принято
выражать водородным показателем рН,
значения которого характеризуют
кислотные или щелочные свойства раствора.
Понятие «рН» впервые было введено
датским химиком Соренсеном и обозначает:
р (начальная буква датского слова
Potenz) –
степень, Н – химический символ
водорода. Физическое содержание этой
величины состоит в следующем.
В водных растворах веществ растворитель –
чистая вода является
химически нейтральным соединением.
Она, хотя и очень слабо, диссоциирует
(распадается) на катионы (положительно
заряженные ионы) водорода (Н+)
и анионы (отрицательно заряженные ионы)
гидроксила (ОН–)
по схеме: Н2О → Н+ + ОН–.
Концентрации диссоциированных ионов
водорода и гидроксила в чистой воде
одинаковы и равны 10–7
моль/л. Их произведение К![]() =
Н+ · ОН– = 10–14
называется ионным произведением. Вода,
а также все растворы, в которых концентрации
водородных и гидроксильных ионов
одинаковы и равны каждая 10–7
моль/л, называются нейтральными
растворами. Преобладание в растворе
кислоты и щелочи приводит к возрастанию,
соответственно, концентрации водородных
или гидроксильных ионов. Однако во всех
случаях их произведение остается
постоянным. Это значит, что если указать
только концентрацию водородных (или
гидроксильных) ионов в каком-либо
растворе, то тем самым будет определена
концентрация другого иона. Поэтому как
степень кислотности, так и степень
щелочности растворов можно количественно
характеризовать концентрацией водородных
ионов. Для этого вместо абсолютной
концентрации водородных ионов используют
ее логарифм, взятый с обратным знаком,
который называют водородным показателем
и обозначают pH:
рН = –lg(Н+).
Например, если Н+ = 10–5,
то рН = 5.
=
Н+ · ОН– = 10–14
называется ионным произведением. Вода,
а также все растворы, в которых концентрации
водородных и гидроксильных ионов
одинаковы и равны каждая 10–7
моль/л, называются нейтральными
растворами. Преобладание в растворе
кислоты и щелочи приводит к возрастанию,
соответственно, концентрации водородных
или гидроксильных ионов. Однако во всех
случаях их произведение остается
постоянным. Это значит, что если указать
только концентрацию водородных (или
гидроксильных) ионов в каком-либо
растворе, то тем самым будет определена
концентрация другого иона. Поэтому как
степень кислотности, так и степень
щелочности растворов можно количественно
характеризовать концентрацией водородных
ионов. Для этого вместо абсолютной
концентрации водородных ионов используют
ее логарифм, взятый с обратным знаком,
который называют водородным показателем
и обозначают pH:
рН = –lg(Н+).
Например, если Н+ = 10–5,
то рН = 5.
Для нейтрального раствора рН = 7. Если pH > 7, раствор обла-дает щелочными свойствами, и тем более сильными, чем выше значение рН; если рН < 7, раствор имеет кислые свойства, и тем более сильные, чем меньше значение рН. Это позволило построить условную шкалу рН. По ГОСТ 8.134 шкала рН основана на приписывании и дальнейшем воспроизведении определенных значений рН пяти растворов буферных веществ. В стандарте приведены их значения рН в интервале температур от 0 до 150 ºС. Шкала рН обладает внутренней согласованностью, т. е. экспериментально измеренное значение рН не зависит от того, какой из растворов был выбран в качестве стандартного. Примерно такой же набор первичных стандартных растворов используется и в других странах.
Индикаторы
|
Индикатор |
Окраска раствора в среде |
||
|
кислой |
нейтральной |
щелочной |
|
|
Лакмус |
Красная |
Фиолетовая |
Синяя |
|
Фенолфталеин |
Бесцветная |
Бесцветная |
Малиновая |
|
Метилоранж |
Розовая |
Оранжевая |
Желтая |
Электрометрический способ измерения рН основан на теорети-ческих предпосылках. Значение потенциала, возникающего на элект-родах, опущенных в электролит, и его знак зависят от природы металла электродов и растворителя, концентрации катионов в растворе и определяется по уравнению, вытекающему из закона Нерста:
E = E0 + lnC · RT/nF, (5.2)
где E0 – потенциал электрода; C – концентрация катионов металлов в растворе; R – универсальная газовая постоянная; Т – абсолютная температура раствора; n – валентность металла; F = 96485 – число Фарадея.
Для измерения электродного потенциала ячейки составляют гальваническую цепь, состоящую из опущенных в электролит изме-рительного и сравнительного электродов, соединенных внешней цепью. В этом случае уравнение (5.2) принимает вид
Eяч = Eи + Eср + lnC · RT/nF, (5.3)
где Еи – нормальный потенциал измерительного электрода; Еср – потенциал сравнительного электрода.
Электрод сравнения – это в основном электрод второго рода. Наиболее распространенными из этой группы являются каломельные электроды (рис. 5.3, а). Он состоит из смеси 2 металлической ртути и твердого хлорида ртути (каломель), находящейся в контакте и в равновесии с насыщенным водным раствором хлорида калия 4 через отверстие 3, платинового электрода 1 и асбестовой ткани 5.
1 2 3 4 5 6 8 7 8 а б в







































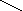
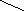


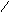


















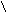
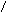

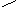


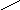


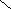

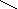

Известны два основных метода измерения рН – колориметрический (индикаторный) и электрометрический (потенциометрический). Первый из них основан на использовании свойств некоторых веществ (так называемых индикаторов) менять свою окраску в зависимости от значения рН контролируемого раствора. Наиболее употребляемые из них приведены в табл. 5.2.
Таблица 5.2
Рис. 5.3. Варианты потенциометрических стеклянных электродов:
а – каломельный; б – хлорсеребряный; в – стеклянный;
1 – платиновый электрод; 2 – смесь металлической ртути и твердого хлорида ртути (каломель); 3 – отверстие; 4 – насыщенный раствор хлорида калия; 5 – асбестовая ткань; 6 – диск из оплавленного стекла; 7 – стеклянная трубка; 8 – чувствительная мембрана
Другим важным электродом сравнения является хлорсеребряный электрод (см. рис. 5.3, б). Он представляет собой аналог каломельного электрода, за исключением того, что вместо ртути и хлорида ртути в нем находятся серебро и хлорид серебра, а асбестовая ткань заменена на диск из оплавленного стекла 6. Из измерительных наиболее распространены стеклянные электроды (см. рис. 5.3, в). Это объясняется их большими метрологическими, конструктивными, эксплуатационными преимуществами перед другими электродами. Электрод представляет собой трубку 7 из обычного стекла, на конце которой напаяна чувствительная мембрана 8 (плоская, конусообразная или сферическая) из специального электродного стекла. Мембрана выполняет функцию одновременно двух электродов, аналогичных водородному: наружного, соприкасающегося с контролируемым раствором, и внутреннего, соприкасающегося с раствором, имеющим известный состав и постоянное значение рН. Контакт между обоими электродами осуществляется через мембрану, обладающую высоким электрическим сопротивлением, значение которого зависит от поверхности, толщины, химического состава стекла и температуры.
Таким образом, потенциал стеклянного электрода является алгебраической суммой потенциалов внутренней и наружной поверх-ностей измерительной мембраны. Для измерения необходимо рН раствора с какой-либо стороны мембраны поддерживать строго постоянным. В этом случае суммарный потенциал стеклянного электрода будет являться функцией рН второго, контролируемого раствора.
Основными достоинствами стеклянных электродов являются простота в работе, быстрое установление равновесия и возможность определения рН в окислительно-восстановительной среде. К недостаткам относят хрупкость их конструкций и усложнение работы при переходе к сильнощелочным и сильнокислотным растворам.
Для обеспечения механической прочности электродов, особенно при использовании в производственных условиях, их армируют, для чего применяют различные конструкции (в зависимости от решаемой задачи) из полимерных материалов или коррозионно-стойкой стали.
В случае работы с растворами, вызывающими образование на электродах мешающих осадков, необходимо обеспечить механическую очистку. Это может быть сделано протиранием мягкими щетками или упругими скребками, приводимыми в движение электро- или пневмоприводом. Опасность замасливания стеклянной мембраны может быть устранена ультразвуком, который одновременно предотвращает и отложение осадков.
В особых условиях, в частности при измерениях в вязких средах с одновременным перемешиванием или при больших скоростях потока, конструкция измерительного датчика должна быть весьма прочной. На практике это достигается тем, что вместо стеклянного электрода используют слой эмали, чувствительной к рН. Такие покрытия наплавляют на стальную трубу.
При измерении ЭДС гальванического элемента через элемент практически не должен протекать ток, так как его прохождение вносит две погрешности в значение ЭДС:
– вследствие изменения концентрации потенциалопределя-ющих частиц у поверхности каждого электрода;
– вследствие того, что каждый элемент обладает внутренним сопротивлением и на нем происходит падение напряжения, которое в зависимости от направления тока либо уменьшает, либо увеличи-вает ЭДС системы.
Наиболее удовлетворительные результаты дают измерения с помощью потенциометра. Воспроизводимость любого такого измерения зависит в основном от чувствительности, с которой известную переменную ЭДС можно компенсировать ЭДС гальванического элемента. Эта чувствительность определяется прибором, применяемым для обнаружения очень слабых токов, которые текут через цепь, когда две противоположно направленные ЭДС недостаточно компен-сированы. рН-метр прямого отсчета, по существу, представляет собой вольтметр с высоким входным сопротивлением, измеряющий ЭДС гальванического элемента и преобразующий ее в пропорциональный ей ток, который проходит через амперметр. Шкала такого амперметра градуирована непосредственно в единицах рН.