Материал: А27631 Бегунов АА методы и средства аналитических измерений
В электролите за счет сил взаимного притяжения каждый ион как бы окружен шарообразным роем противоположно заряженных ионов. Если в раствор опустить электроды, соединенные с источ-ником электрического тока, то разноименно заряженные ионы начинают перемещаться к соответствующим электродам. При этом окружающая ион атмосфера тянет его обратно, замедляя тем самым движение, а следовательно, уменьшая количество ионов, проходящих через раствор в единицу времени, т. е. силу тока. Чем больше концентрация раствора, тем сильнее проявляются эти тормозящие силы, тем меньше будет электропроводность раствора. Поэтому при изменении электропроводности раствора получается несколько заниженное против действительного значение концентрации, которую оценивают активностью, т. е. молярной концентрацией вещества в растворе, умноженной на так называемый коэффициент активности. Поскольку этот коэффициент близок к единице, во многих случаях при анализе концентрации электрохимическими методами активностью можно пренебречь и говорить непосредственно о концентрациях. Такое упрощение оправдано в тех случаях, когда это допускают либо заданная погрешность измерения, либо градуировки прибора.
5.1. Кондуктометрический метод
Кондуктометрический метод основан на зависимости электропроводности или сопротивления электролитов от концентрации анализируемого компонента в материале.
Обычно измерения проводят в электролитической ячейке, представляющей собой сосуд с анализируемым раствором, в который помещены два электрода. В последние годы получили развитие бесконтактные способы измерения, при которых отсутствует контакт электродов с раствором. В простейшем виде измерительная схема прибора представляет собой равновесный мост, в плечо которого включена электролитическая ячейка. Для компенсации температур-ного влияния в автоматических анализаторах используют температурные автоматические компенсаторы электрического типа с термометрами сопротивления или полупроводниковыми термисторами.
Основными источниками погрешности кондуктометрического метода являются влияние побочных присутствующих в растворе веществ, обладающих ионизационными свойствами, а также поляри-зация электродов протекающим через них током. Существенное влияние оказывает также соотношение между скоростью электрохимической реакции и скоростью доставки к электродам ионов. Ослабление этих эффектов достигается снижением плотности тока на электродах и проведением измерений на повышенных частотах.
При бесконтактном способе измерения все погрешности, связанные с поляризацией электродов, отсутствуют. Образование на измерительном участке слоя неэлектропроводных осадков или масел тоже почти не сказывается на результате измерений. С другой стороны, в этом случае значительно усложняется и дорожает само средство измерения. Поэтому бесконтактные способы применяют большей частью тогда, когда контактная техника измерений оказывается неэффективной.
5.2. Диэлькометрический метод
Данный метод основывается на непосредственном измерении диэлектрической постоянной, являющейся функцией концентрации анализируемого вещества в растворе, с помощью высокочастотного переменного напряжения.
Практическое использование метода будет рассмотрено далее на примере измерения влажности твердых и жидких сред.
5.3. Полярографический метод
Полярографический метод основан на определении природы и количества анализируемого вещества по кривым ток–напряжение, получаемым с помощью капельного ртутного электрода.
С развитием электронной техники широкое распространение получили многие виды полярографии (классической, осциллографи-ческий, дифференциальный, переменно-токовый, импульсный и др.).
Поскольку подавляющее число неорганических и органиче-ских соединений способны к электровосстановлению на ртутном капельном электроде, полярографический метод может быть применен для анализа таких биологически активных соединений, как аминокислоты, витамины, белки, углеводы, а также для определения микроэлементов и следов тяжелых металлов в продуктах. При этом возможно одновременное определение ряда элементов, например меди, свинца, олова и цинка.
В настоящее время развитие полярографических методов анализа происходит по трем направлениям:
– совершенствование методик классической полярографии;
– разработка методик переменно-токовой полярографии;
– усовершенствование инверсионной вольтамперометрии.
Применение переменного тока в полярографии повышает разрешающую способность метода, увеличивает чувствительность и точность.
Полярографическая установка состоит из измерительной ячей-ки, включающей сосуд с анализируемым раствором и два электрода, источника поляризующего напряжения, регулятора и измерителя силы тока. Один из электродов представляет собой капли ртути, непрерывно капающие из капилляра с постоянной частотой, благодаря чему поверхность электрода непрерывно обновляется. При постоянной скорости образования капель обеспечивается хорошая воспроизводимость результатов измерений. В качестве второго электрода служит слой ртути на дне ячейки.
Вольтамперную характеристику получают, измеряя силу тока при установлении различных значений напряжений. На рис. 5.1 показана типичная полярограмма однокомпонентного (а) и трехкомпонентного (б) растворов. Мерой концентрации является высота волны, т. е. разность предельной и остаточной силы тока I.
а б
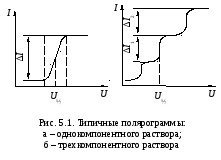
Напряжение U½, соответствующее средней точке волны, характеризует природу вещества. Таким образом, полярограмма содержит полную информацию о характере и количестве вещества. На практике не удается использовать расчетным путем зависимость между высотой волны и концентрацией из-за влияния ряда факторов: скорости диффузии анализируемого вещества в растворе, темпера-туры, параметров капилляра и др. Поэтому анализ проводят сравнением высоты волны в растворе неизвестной концентрации с высотой волны в стандартном растворе. Применяют также способ, при котором рассчитывают концентрацию по приращению высоты полярограммы анализируемого раствора после добавления в него известного количества исследуемого вещества.
Методы полярографического анализа разработаны почти для всех элементов Периодической системы. Все больше и больше этот метод внедряется в практику анализа органических веществ, метал-лургию. Его используют для анализа лекарственных веществ, полимеров, для определения следов ядохимикатов на растениях и в продуктах питания.
Тщательное соблюдение условий эксперимента, достаточно строгий контроль температуры и аккуратность при построении графика позволяют добиться погрешности измерений не более 2 %.
5.4. Потенциометрический метод
Потенциометрический метод основан на измерении разности потенциалов электродов, зависящих от концентрации в электролите анализируемого вещества.
Если в раствор, содержащий окисленную и восстановленную формы одного и того же вещества, например двух-, трехвалентного железа, опустить электрод из благородного металла (платины, зо-лота), то электрод приобретет потенциал, характерный для данного иона. Это явление объясняется следующим. Ионы, находящиеся в растворе, попадая на электрод, способны отдать ему или принять от него электроны. При этом на поверхности электрода создается двойной электрический слой, электрод заряжается положительно или отрицательно. Значение и знак потенциала определяются концентрацией и природой ионов. Вообще говоря, потенциал электрода складывается из целого ряда частных гальванических потенциалов. Сами по себе эти потенциалы измерить невозможно. Однако, когда два электрода соединены в электрическую цепь, можно измерить потенциал как сумму частных потенциалов. В потенциометрической измерительной цепи один из электродов является измерительным, второй – электродом сравнения. На первом формируется потенциал, однозначно характеризующий химическое состояние электролита, которое может быть выражено активностью или концентрацией какого-либо иона. Электрод сравнения, в отличие от измерительного, имеет потенциал, совершенно независимый от состава электролита (электрод сравнения отделен от измеряемой среды мембраной).
Для того чтобы сравнивать между собой потенциалы различ-ных электродов, за нуль приняли потенциал водородного электрода, представляющего собой платиновую пластинку, опущенную в раствор с активностью ионов водорода, равной единице, и обдуваемую газообразным водородом под давлением 0,1 МПа. Сам водородный электрод для практического использования неудобен. Его применяют лишь в метрологических целях для установления потенциалов стандартных электродов сравнения.
Потенциометрический метод позволяет измерять концентрацию или активность конкретного иона. Для этого применяют так называемые ионоселективные электроды. В связи с этим становится более употребляемым термин «ионометрия», который полнее отражает физическую сущность данного метода анализа.
Конструкции электродов будут рассмотрены далее на примере анализа концентрации ионов водорода, как наиболее распростра-ненной и разработанной области ионометрии. Ионоселективные электроды представляют собой электрохимические полуэлементы, для которых разность потенциалов на границе раздела фаз «электродный материал–электролит» зависит от активности определяемого иона в растворе. Для изготовления этих электродов в твердый материал вводят нерастворимое соединение, содержащее ионы, которые нужно определять. Например, электрод на ионы брома можно получить в ходе полимеризации силикатной резины при наличии эквивалентной массы бромида серебра. Смесь после затвердения запрессовывают в нижнюю часть стеклянной трубки. Эта твердая смесь поглощает преимущественно ионы, которые входят в ее состав.
Механизм действия ионоселективных электродов состоит в следующем. При погружении электрода в раствор электролита устанавливается равновесие на границе «электрод–электролит» и имеет место равенство электрохимических потенциалов ионов металла в твердой фазе и растворе. Каждый ионит (так называют нераство-римые неорганические и органические высокомолекулярные соеди-нения, содержащие активные ионогенные группы) обладает фикси-рованным положительным или отрицательным зарядом. Этот заряд компенсируется зарядом ионов противоположного знака (так назы-ваемым противоионом). Последние подвижны внутри ионита и могут замещаться другими ионами того же заряда. При контакте ионита с раствором электролита, ионный состав или концентрация которого отличаются от аналогичной величины в ионите, будет наблюдаться обменная диффузия подвижных ионов в системе в направлении уменьшения градиента концентраций. Вследствие разности подвиж-ности ионов в первый момент имеет место нарушение электронейт-ральности в ионите, приводящее к возникновению электростатиче-ского заряда. Это, в свою очередь, вызывает появление пространст-венного заряда в растворе электролита. Возникающая на границе раздела фаз «ионит–раствор» разность потенциалов зависит от инди-видуальной активности ионов.
Приборная реализация потенциометрического метода и харак-терные погрешности будут рассмотрены на примере измерения активности ионов водорода.
В настоящее время в промышленности освоен выпуск ионо-селективных электродов более чем на 50 ионов. Часть из них приведена в табл. 5.1.
Таблица 5.1