Материал: Preparaty_-_proizvodnye_tsiklopentanpergidrofenantrena__1
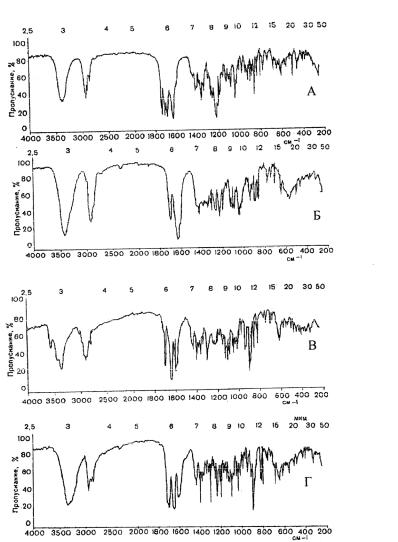
Рис. 5. Инфракрасные спектры кортизона ацетата (А), гидрокортизона (Б), преднизона (В) и преднизолона (Г) в таблетках калия
бромида
ИК-спектр преднизолона практически идентичен спектру преднизона в области 1600–1800 см-1, отличия наблюдаются в области поглощения
3000–4000 см-1 (3360, 3450 и 3560 см-1).
Дексаметазон в отличие от рассмотренных выше препаратов характеризуется наличием широкой полосы с сильной интенсивностью в области 1000–1100 см-1, обусловленной наличием в структуре препарата связи C-F. Область ИК-спектра дексаметазона 1600–1800 см-1 имеет три полосы поглощения: полосы сильной интенсивности валентных колебаний С=О при С3 (1700 см-1), валентных колебаний С=О, сопряженных с двойной связью (1650 см-1), и полоса валентных колебаний С=С связи (1600 см-1).
26
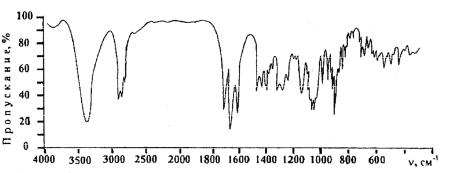
Рис. 6. Инфракрасный спектр дексаметазона в таблетках бромида калия
Производные эстрана. ИК-спектр эстрадиола имеет широкую полосу поглощения с максимумами при 3220 см-1 и 3420 см-1, соответствующим валентным колебаниям гидроксильных групп при С3 и С17. К валентным колебаниям группировок С=С кольца А относятся две полосы средней степени интенсивности при 1575 и 1597 см-1, а также полоса при 1490 см-1. Валентные колебания связи С-О представлены полосой сильной степени интенсивности в области 1238–1282 см-1. Имеется серия полос, соответствующих деформационным колебаниям СН-групп при 777, 810, 865 и 910 см-11.
Идентификация ИК-спектра этинилэстрадиола в таблетках бромида калия затруднена в области 3000–4000 см-1, где поглощают одновременно гидроксильные и этинильная группы. Поэтому для идентификации этинилэстрадиола параллельно снимают спектры его 2,5% раствора в хлороформе. В этом случае полосы поглощения в области 3000–4000 см-1 строго дифференцированы и в спектре имеются интенсивные полосы при 3310 см-1 и 3600 см-1. Первая из них соответствует СН-валентным колебаниям этинильной группы, которые на спектре образца в вазелиновом масле представлены в виде двух интенсивных полос при 3290 и 3320 см-1. Две полосы, соответствующие валентным колебаниям гидроксильных групп, при 3510 и 3610 см-1 в хлороформном растворе проявляются в виде одной полосы с максимумом при 3600 см-1.
Остальные, наиболее характерные для функциональных групп этинилэстрадиола полосы поглощения сохраняются при 1610, 1585 и 1495 см-1, а также в области 1000–1100 см-1.
Для ИК-спектра местранола специфичными являются в области 3000– 4000 см-1 две полосы поглощения при 3240 и 3270 см-1, соответствующие валентным колебаниям СН-группы в этинильном радикале, а также полосы при 3470 и 3520 см-1, свойственные валентным колебаниям гидроксильных групп.
27
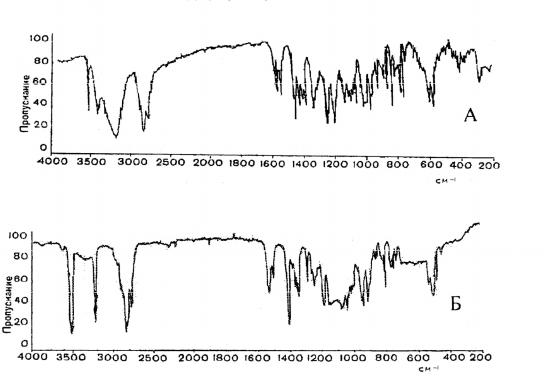
Рис. 7. Инфракрасные спектры этинилэстрадиола в таблетках бромида калия (А) и 2,5% раствора в хлороформе (Б)
В области 1500–1700 см-1 в отличие от этинилэстрадиола, имеющего две узкие полосы равной степени интенсивности, местранол проявляет очень интенсивную полосу поглощения при 1603 см-1 и полосу средней интенсивности при 1570 см-1. Более интенсивно, чем у этинилэстрадиола, выражены полосы поглощения С-О-группы в области 1000–1100 см-1 и валентные колебания СН-группы в области 800–900 см-1. Специфической для местранола является полоса при 695 см-1.
Эстрон применяется в качестве лекарственного средства, а также является исходным продуктом синтеза этинилэстрадиола и местранола. Наличие карбонильной группы при С17 в эстроне приводит к появлению на ИКспектре интенсивной полосы поглощения при 1715 см-1, что в сочетании с полосой валентных колебаний гидроксильной группы при С3 (3330 см-1), а также остальными параметрами, специфичными для эстратриенов, делает спектр эстрона характерным (рис. 23). Эта особенность может использоваться не только для идентификации, но и для определения примеси эстрона в препаратах этинилэстрадиол и местранол.
28
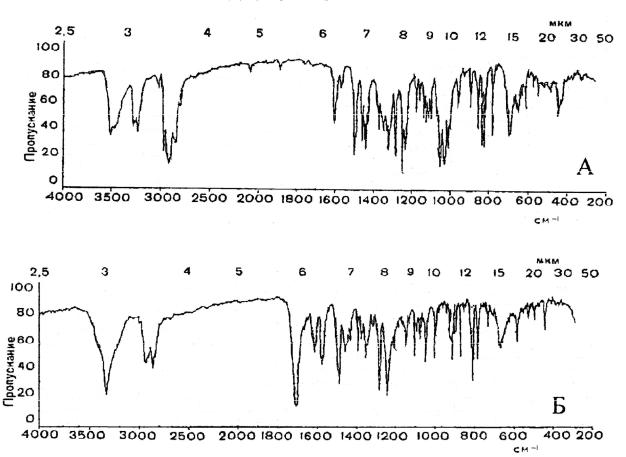
Рис. 8. Инфракрасные спектры местранола (А) и эстрона (Б) в таблетках бромида калия
УФ-спектроскопия
УФ-спектрофотометрия используется на всех этапах фармацевтического анализа стероидных соединений (испытание на подлинность, доброкачественность, количественное определение) и является унифицированным методом анализа лекарственных веществ данной группы и их препаратов. При испытании на подлинность исследования проводятся с целью:
–получения спектров поглощения анализируемого и стандартного образцов в области от 220 до 300 нм;
–изучения характера спектров на основании максимумов и минимумов поглощения;
–измерения величины E1%1см.
Для растворения анализируемого образца стероидных соединений пользуются, как правило, 95% этиловым спиртом. Концентрации растворов готовятся в соответствии с рекомендациями НД на конкретный препарат и в большинстве случаев составляют около 0,001 %.
29
4- и 1,4-3-кетостероиды (андрогены, анаболики, гестагены и кортикостероиды) имеют сходные спектры поглощения с максимумом в области 238–241 нм. Это связано с наличием в структуре данных соединений хромофорной системы, возникающей вследствие сопряжения карбонильной группы при С3 и двойных связей кольца А. Исключение составляют метандиенон, максимум которого смещен в длинноволновую область на +4 нм (λ = 245 нм) и метандриол, не имеющий максимума поглощения в области от 200 до 300 нм, из-за отсутствия хромофорной системы.
Стероидные соединения производные эстратриенов (эстрон, эстрадиол, этинилэстрадиол), содержащие в ароматическом кольце А гидроксильную группу при С3, имеют максимум поглощения при 280 нм. Введение в положение С3 метоксильной группы (местранол) обусловливает наличие максимума поглощения в области 285–287 нм, что свидетельствует о батохромном влиянии этой группы.
Хроматографические методы
Вотечественную и зарубежную НД для установления подлинности и доброкачественности стероидных гормонов включены методы хроматографии: ТСХ и ВЭЖХ на нормальных и обращенных фазах.
Хроматография в тонких слоях сорбента (ТСХ). Среди сорбентов,
рекомендуемых НД для ТСХ стероидных гормонов, основное место занимает силикагель и его смеси («Кизельгель», «Силуфол», «Сорбифил» и др.).
Вкачестве проявителей используются специфические (групповые) и неспецифические (общие) реактивы, а также способность стероидных гормонов и их производных к флюоресценции в УФ-свете (254–365 нм). К неспецифическим реактивам следует отнести 6% растворы хлорной кислоты в метиловом спирте (I), раствор концентрированной серной кислоты в метиловом спирте (1:1) (II), 10% раствор фосфорно-молибденовой кислоты в этиловом спирте (III), раствор анисового альдегида в смеси безводной уксусной и концентрированной серной кислот (IV) и раствор бихромата калия
всерной кислоте (V). После обработки хроматографической пластинки реактивами I–V, ее затем нагревают при температуре 105–120 °С в течение 10–15 минут. Вещества на хроматограммах проявляются в виде окрашенных пятен, после чего хроматограмму просматривают в УФ-свете и отмечают наличие и характер флюоресценции.
Кортикостероиды проявляют с помощью группового реактива – трифенилтетразолия хлорида, – основываясь на его способности образовывать
окрашенную восстановленную форму в результате реакции с α-кетольной
30