Материал: Preparaty_-_proizvodnye_tsiklopentanpergidrofenantrena__1
Решающей стадией синтеза кортикостероидных гормонов является селективное биогидроксилирование кортексолона по С11 с использованием культуры бактерий Rhizopus nigricans. Полученный триол окисляют до гидрокортизона, который ацетилируют с образованием эфира.
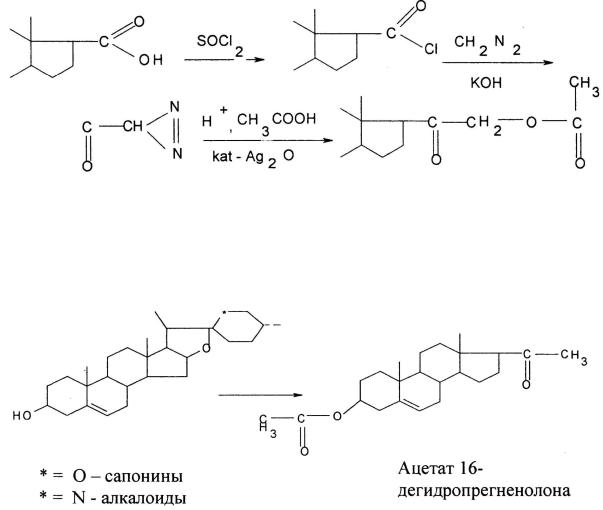
Введение ацилированных α-кетольных групп в 17β-положение глюкокортикоидов может осуществляться и в условиях реакции Арндта – Айстерта разложением диазокетонов:
Химическая трансформация основных сырьевых полупродуктов в синтезе кортикостероидов и гестагенов – стероидных сапонинов и стероидных алкалоидов – проводится в три стадии с получением ацетата 16-деги- дропрегненолона, который является основой для синтеза всех кортикостероидов.
Схема получения ацетата 16-дегидропрегненолона
4.2. Микробиологическая трансформация стероидов
Первые сообщения о трансформации стероидов микроорганизмами появились задолго до того, как было выяснено строение стероидов. Еще в конце прошлого столетия было установлено, что бактериальная флора кишечника млекопитающих способна превращать холестерин в копростерин, а холевую кислоту – в дезоксихолевую.
16
В1908 году была обнаружена способность бактерий Escherichia coli окислять гидроксильные группы холевой кислоты. В 1937 году было открыто восстановление дрожжами 17-кетогрупп и осуществлено превращение эстрона в эстрадиол. В 1952 году получено 11α-оксипроизводное прогестерона при его ферментации с плесенью Rhizopus nigricans.
Врезультате исследований с 1934 по 1954 годы химия стероидов получила новый, чрезвычайно эффективный метод синтеза, отличающийся высокой специфичностью и приводящий во многих случаях к высоким выходам таких соединений, которые трудно получить химическим путем. За этот период открыто около 100 реакций трансформации стероидов с участием около 60 видов микроорганизмов. За последние годы исследований в этом направлении число реакций увеличилось в 60 раз, а число используемых для этих целей микроорганизмов – в 18 раз.
Сиспользованием микроорганизмов можно осуществлять следующие типы превращений:
–образование и расщепление углеродных связей;
–образование и восстановление двойных углеродных связей;
–изомеризация двойных углеродных связей;
–гидроксилирование и дегидратации;
–образование и раскрытие α-окисей;
–гидролиз и этерификация;
–образование и восстановление кетогрупп;
–образование и разрушение связей галоген-углерод;
–образование и разрушение связей азот-углерод;
–образование и разрушение связей сера-углерод;
–расщепление рацематов стероидов, полученных химическим синте-
зом.
Вкачестве сырья для промышленных процессов трансформации стероидов используются природные стерины, выделенные из растительных источников (стероидные сапонины и алкалоиды) и различных органов животных (ситостерины, холестерин и др.). Микробиологический синтез всегда сочетается с химическими превращениями молекулы стероидов.
Первоначально реакции микробиологической трансформации стероидов проводились с помощью неиммобилизованных клеток микроорганизмов в двухфазных водно-органических системах. Клетки при этом локализовались в водной фазе, а стероидные соединения – в органической. Кроме того, микроорганизмы подвергались губительному воздействию органического растворителя. Данный метод имел низкую эффективность и требовал постоянного возобновления трансформирующей культуры клеток микроорганизмов после каждого производственного цикла. Поэтому для трансформации стероидных гормонов в 1970 г. был впервые применен метод прове-
17
дения реакций с использованием иммобилизованных клеток микроорганизмов.
Иммобилизация клеток микроорганизмов осуществлялась путем включения их в различные гели (полиакриламидные гели, гели альгината, каррагинана, агара) или мембраны различных полимеров, а также адсорбции на целлюлозе, керамике, ионитах, силикагеле и др., а также путем ковалентного связывания с силикагелем. Иммобилизованные клетки микроорганизмов, находящиеся внутри гранул носителя в водной фазе, мало подвержены воздействию органических растворителей, не смешивающихся с водой. Например, в качестве катализатора реакции дегидрирования стероидов в среде бензола и гептана используются различные виды бактерий Nocardia sp., включенные в гидрофобные гели (уретановые полимеры). Они обладают высокой активностью и стабильностью, чем бактерии, находящиеся в гидрофильном окружении.
Использование иммобилизованных клеток микроорганизмов имеет множество преимуществ и перед иммобилизованными ферментами. Хорошо известно, что некоторые стероидтрансформирующие ферменты, особенно гидролазы и дегидрогеназы, являются весьма лабильными белками, их выделение и очистка затруднены, а закрепленные на нерастворимых материалах клетки микроорганизмов служат постоянным носителем активных стабильных полиферментных систем.
Основные реакции микробиологической трансформации стероидных соединений, используемые в промышленном синтезе стероидных гормонов, приведены в табл. 1.
Таблица 1
Микробиологическая трансформация стероидов, имеющая промышленное значение
Реакция |
Субстрат |
Продукт |
Микроорганизм |
|
11α- |
Прогестерон |
11α-гидроксипрогестерон |
Rhizopus |
|
гидроксилирование |
nigricans |
|||
|
|
|
|
|
11β- |
Вещества S |
Гидрокортизон |
Curvularia lunata |
|
гидроксилирование |
||||
16α- |
9α- |
9α-фтор-16α- |
Streptomyces |
|
гидроксилирование |
фторкортизол |
гидроксикортизон |
roseochromogenus |
|
|
|
|
|
|
1,2-дигидрирование |
Гидрокортизон |
Преднизолон |
Arthrobacter |
|
simplex |
||||
|
|
|
||
Расщепление |
β-Ситостерин |
Андростадиендиол |
Mycobacterium |
|
боковой цепи |
Андростендион |
sp. |
||
|
||||
|
|
|
|
Одной из важных реакций микробиологического синтеза стероидных гормонов является трансформация природных 5-3-оксисоединений (холе-
18
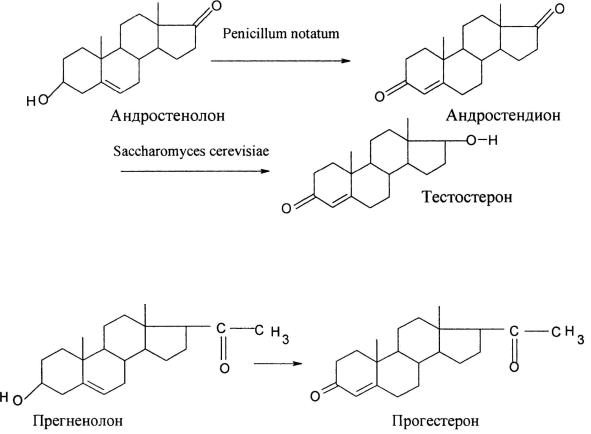
стерин, диосгенин, саласодин и др.) в 4-3-кетопроизводные, поскольку наличие 4-3-кетогруппы необходимо для проявления гормональной активности андрогенов, гестагенов и кортикостероидов. Так, например, тестостерон можно получить в две микробиологические стадии с выходом около 80 % по схеме:
Синтез гестагенов проводят путем превращения прегненолона в прогестерон в одну стадию со 100 % выходом основного продукта реакции, поэтому преимущество микробиологического процесса трансформации молекулы перед химическими методами (по Оппенауэру и др.) очевидно:
Молекулы кортикостероидов и их синтетических аналогов содержат несколько гидроксильных групп. Их введение химическими методами хорошо разработано лишь для гидроксигрупп, находящихся по соседству с -С=О или –С=С-группами. Но если вводимая гидроксигруппа не имеет такого окружения, то все химические методы становятся неэффективными. Это относится, прежде всего, к 11β- и 11α-гидроксигруппам. В современном производстве глюкокортикоидов введение данных групп проводят только с помощью микробиологической трансформации кортексолона, используя гидроксилирующие культуры – Rhizopus nigricans, Curvularia lunata, Tieghemella orchldis, Cunninghamella blakesleana, Trichothecium roseum и др.
19
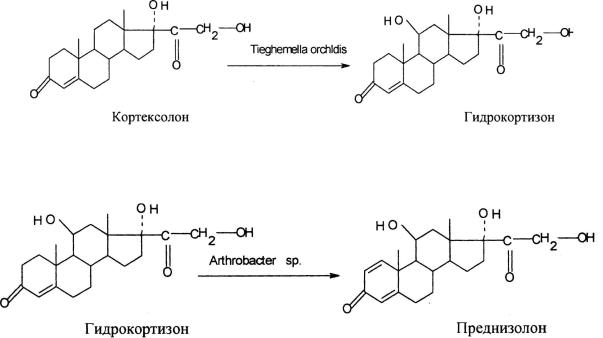
Другой важной реакцией в синтезе физиологически активных анаболиков (метандростенолон) и кортикостероидов (преднизолон, дексаметазон и др.) является реакция микробиологического 1-дегидрирования.
В настоящее время разработаны различные способы интенсификации микробиологической трансформации стероидных гормонов:
– предварительное индуцирование растущей культуры-трансформа- тора соответствующим субстратом или его аналогом;
–использование нерастворимых микрокристаллических стероидных субстратов, полученных путем диспергирования и измельчения субстрата, а также превращением его в водорастворимое состояние с помощью β- циклодекстринов.
5. КОНТРОЛЬ КАЧЕСТВА СТЕРОИДНЫХ ГОРМОНОВ
Основные тенденции в современном фармакопейном анализе препаратов стероидных гормонов и их синтетических аналогов заключаются в повышении требований к избирательности метода. Возможности использования для этого новых химических реакций, селективных с классической точки зрения, практически исчерпаны. Новые перспективы открываются с использованием спектральных и хроматографических методов. При разработке избирательных методов анализа стероидных гормонов, пригодных для фармацевтического анализа, во внимание принимаются их чувствительность и продолжительность. При контроле субстанций стероидных гормонов эти требования не очень высоки, поэтому чаще всего используются методы спектрофотометрии в УФ- и видимой области спектра. Но в некоторых случаях, например, при анализе эстрогенов и гестагенов в контрацептивных препаратах, фторкортикостероидов в мазях, а также следовых
20