Материал: Preparaty_-_proizvodnye_tsiklopentanpergidrofenantrena__1
R - С2Н5, |
4 = норгестрел |
R - СН3, |
4, 3-дезоксо = линоэстренол |
|
3.3. Кортикостероиды |
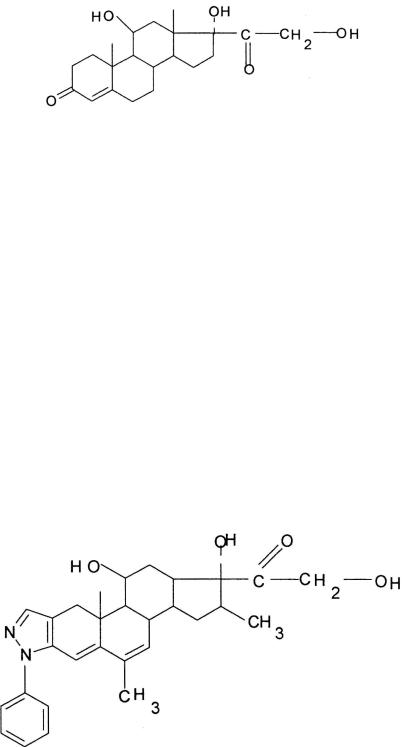
Гидрокортизон
Для поизводных гидрокортизона характерно:
–для проявления глюкокортикоидной активности необходимо наличие в 17α- и 11β-положениях гидроксильных групп;
–у 11-эпипроизводных кортикостероидов резко снижена глюкокортикоидная активность;
–наличие в 9α-положении атома фтора увеличивает глюкокортикоидную активность в 10 раз;
–синтетические аналоги глюкокортикоидов, характеризующиеся высокой физиологической активностью, имеют дополнительную двойную
связь в C1,2-положении (преднизолон), атом фтора в 9α-, a иногда 6αположении и заместитель (метил-, гидроксил- и др.) в С16-положении (дексаметазон, бетаметазон, триамцинолон и др.);
–изменение субдоминантной группы гидрокортизона ацетата, а именно конденсация кольца А в положение 2,3 с фенил-пиразолом, приводит к получению высокоэффективного препарата – кортивазола или его деацилированного производного, обладающего мощным противовоспалительным действием и высоким сродством к специфическим рецепторам (в 40 раз выше чем у дексаметазона).
Структурная формула синтетического глюкокортикоида – кортивазола
11
–16α,17α-диоксикортикостероиды используют в форме циклических кеталей, образующихся в результате взаимодействия с ацетоном или другими кетонами (флюоцинолона ацетонид, триамцинолона ацетонид, будесонид); данная модификация приводит к снижению всасываемости препаратов, которые применяются местно в виде мазей или кремов;
–как природные, так и синтетические кортикостероиды часто применяют в виде сложных эфиров, в основном по С21-гидроксигруппе, а иногда
ипо С17- и С16-гидроксигруппам; особенно важны водорастворимые натриевые соли их 21-фосфатов (дексаметазона натрия фосфат) и 21-сукци- натов (преднизолона гемисукцинат);
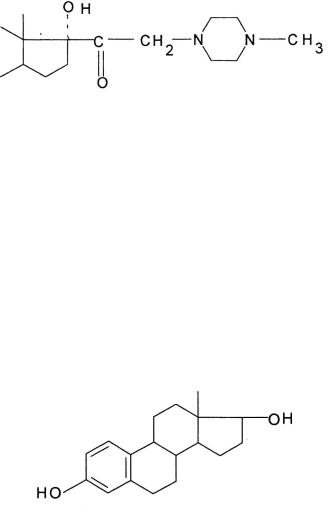
–водорастворимые формы глюкокортикоидов можно получить замещением 21-гидроксигруппы на аминопроизводные, например N-метил-N’- пиперазинил-преднизолона гидрохлорид;
–для некоторых глюкокортикоидов (гидрокортизон, преднизолон, дексаметазон) исследуется возможность использования в форме водорастворимых полимерных производных с целью коррекции их фармакологических и токсических эффектов. Известны полимерные производные гидрокортизона и преднизолона на основе образования полиэфиров в результате реакции ацелирования с сополимером поливинилпирролидона и малеинового ангидрида;
–комплекс флюоцинолона ацетонида с Р-циклодекстрином является основой мази «Синафлан-ЦД», подобная модификация молекулы приводит
кповышению фармакологической активности в 1,5–2 раза по сравнению с прототипом.
3.4.Эстрогены
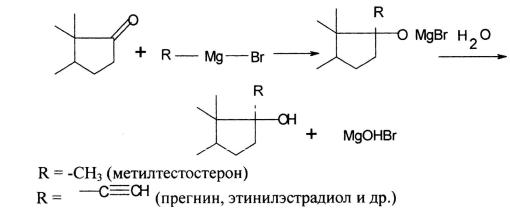
Эстрадиол
Для производных эстрадиола характерно:
12
–для проявления эстрогенной активности необходимо наличие ароматического кольца А и свободной 3β-гидроксигруппы;
–у эстрона (17-кетопроизводное) биологическая активность в 5–15 раз ниже эстрадиола;
–у 17-эпипроизводного эстрадиола (α-эстрадиол) эстрогенная активность снижена в 20 раз;
–наличие в 16α-положении эстрадиола гидроксильной группы снижает его эстрогенное действие, а введение 16β-гидроксигруппы приводит к полной потере биологической активности; 16-гидроксиэстрадиол («Овестин») применяется для лечения состояний и симптомов, связанных с дефицитом эстрогенов (хирургическая или естественная менопауза);
–введение в 17α-положение эстрадиола этинильного радикала приводит к усилению эстрогенной активности и устойчивости при пероральном применении (этинилэстрадиол); этинилэстрадиол и его 3-метоксипроиз- водное – местранол – являются эстрогенными составляющими всех пероральных контрацептивных препаратов;
–11-арилпроизводные этинилэстрадиола обладают антигестагенной активностью (абортирующие контрацептивные препараты – «Мефипристон», «Пенткрофтан»).
4.СПОСОБЫ ПОЛУЧЕНИЯ СТЕРОИДНЫХ ГОРМОНОВ
4.1. Химический синтез стероидных гормонов
Исследования в области полного химического синтеза стероидов начались в 1932 году после установления структуры холестерина. За короткий период так называемой «стероидной лихорадки» с 1932 по 1960 гг. были синтезированы практически все природные стероидные гормоны – эстрон (Мишер, 1948 г.), андростерон, холестерин, кортизол (группы Робинсона и Вудворда, 1951 г.). Полный синтез стероидов позволил полностью подтвердить их химическую структуру, а также явился мощным толчком развития органического синтеза вообще. С 60-х годов исследователи стали стремиться к разработке полного синтеза гормонов, пригодного для осуществления малостадийного, стереоспецифического промышленного синтеза. Впервые данная задача была решена для синтеза эстрона из дешевого сырья – перолина – за 8 химических стадий с выходом 27 %.
Основные трудности полного синтеза стероидов заключаются:
– в наличии 4 углеродных циклов, конденсированных в о-положе-
ниях;
13
–в обеспечении пространственного строения синтезируемой молеку-
лы (холестерин содержит 8 асимметрических атомов углерода, что делает возможным существование 28 = 256 стереоизомеров);
–в разработке стереонаправленных процессов, позволяющих на каждой стадии синтеза получать нужные стереоизомеры.
В настоящее время полный химический синтез стероидов, как правило, не имеет практического значения. Для получения лекарственных препаратов стероидных гормонов используют полусинтез из природных (растительных и животных) стеринов с применением методов химической и микробиологической трансформации молекулы.
Основные реакции, используемые в синтезе стероидных гормонов и их полусинтетических производных, будут рассмотрены на примере синтеза эстрогенных гормонов и кортикостероидов.
Промышленный синтез эстрона основан на гидрировании 2-метокси- нафталина до тетралина, окислением которого хромовой кислотой до тетралона и обработкой винилмагнийбромидом получают спирт.
2-Метилциклопентандион-1,3 как СН-кислота легко присоединяется по винильной группе спирта, образуя после дегидратации щелочью соединение, которое далее подвергают кислотнокатализируемой циклизации с отщеплением одной молекулы воды. В результате возникает конденсиро-
ванный четырехъядерный остов молекулы. Гидрированием (H2/Pd) олефиновой связи с последующим гидролизом метоксильной группы получают эстрон.
Из эстрона присоединением ацетилена синтезируют этинилэстрадиол
иместранол. Введение метальных и этинильных групп в 17α-положение может осуществляться другими методами:
–с помощью магнийорганических реактивов Гриньяра по схеме:
14
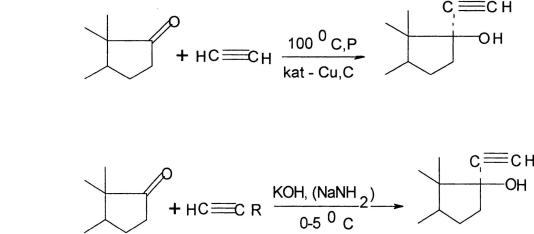
–синтез Реппе:
–синтез Фаворского:
Кортикостероидные гормоны – гидрокортизон, кортизона ацетат и др. – получают из природных соединений – холестерина или стероидных сапонинов (диосгенин, тигогенин) и стероидных алкалоидов (саласодин).
Сначала холестерин окислительным отщеплением боковой алкильной группы при С17 хромовым ангидридом (после предварительной защиты гидроксильных и -С=С- групп соответственно ацилированием и бромированием) переводят в дибромкетон. Этот кетон дебромируют действием цинка и получают ацетат дегидроэпиандростерона, в котором кольцо D химически модифицируют. После цианирования и дегидратации получают цианопроизводное, обработка которого метилмагнийбромидом дает промежуточный имин, легко гидролизуемый добавлением водой, что позволяет преобразовать цианогруппу в ацетильную и снять ацетильную защиту с ОН-группы
при С3.
Спиртовую группу в кольце А оксирана превращают в оксогруппу по Оппенауэру. Реакция идет в присутствии изопропилата алюминия и циклогексанона (акцептор водорода) и сопровождается изомеризацией двойной связи из кольца В в кольцо А, что приводит к сопряженному енону.
Трансформацию 5-3β-окси-стероидов в 4-3-кетоны можно осуществить и другими методами:
– в реакции Веттштайна, разновидности реакции Оппенауэра, вместо циклогексанона используется бензохинон, что приводит к образованию 4,6- 3-кетопроизводных;
–реакция Пфицнера – Маффета проводится в более мягких условиях
вприсутствии дициклокарбодиимида в растворе ДМСО при температуре
20 °С.
На следующей стадии оксирановое кольцо в соединении расщепляют действием НВr. Полученное производное дебромируют до третичного спирта, который окисляют до кетодиола – кортексолона.
15