Материал: Melnuchuk_Promuslova biotexnologij

РОЗДІЛ 9. МЕТОДИ КОНТРОЛЮ ТА УПРАВЛІННЯ БІОТЕХНОЛОГІЧНИМИ ПРОЦЕСАМИ
Робота № 48. Стандартизація та оцінка якості біопрепаратів шляхом визначення титру препарату
Використання мікроорганізмів як основи біологічних препаратів для захисту рослин – порівняно новий напрям біотехнології, але вже має істотні досягнення. В даний час бактерії, гриби, віруси знаходять все більш широке застосування як промислові біопестициди. Технологія виробництва цих препаратів дуже різна, як різна природа і фізіологічні особливості мікроогранізмів -продуцентів.
Однак є ряд універсальних вимог до біопестицидів, основними серед них є: селективність і висока ефективність дії, безпека для людини і корисних представників флори і фауни, тривале збереження і зручність застосування.
Біологічні засоби захисту рослин (біопрепарати та ентомофаги) повинні відповідати певним вимогам, тобто бути стандартизовані. Стандартизацію та оцінку якості біопрепаратів проводять за кількістю діючого початку (спори, включення, клітини, метаболіти) в одиниці маси або об'єму і з біологічної активності.
Для визначення кількості діючого початку (титру препарату) використовують різні методи залежно від природи діючого агента. Так, кількість життєздатних спор або клітин визначають посівом препарату на живильне середовище з подальшим підрахунком вирослих колоній. Титр вірусних препаратів (та інших організмів, що не розмножуються на живильних середовищах ) підраховують в камері Горяєва під світловим мікроскопом.
Кількість токсинів, антибіотиків, інших БАВ визначають хроматографічними і спектральними методами.
Біологічну активність як головний показник якості біопрепарату вимірюють реакцією тест-об'єкта на дію біопестіціда. Тест-об'єктами є комахи (для ентомопатогенних препаратів) або фітопатогени (для препаратів проти хвороб рослин). Стандартизацію та оцінку якості біопрепаратів проводять по кількості діючого інфекційного навантаження (спори, включення, клітини, метаболіти) в одиниці маси або об'єму і по біологічній активності. Останній показник найбільш значущий.
Біологічна активність препаративної форми може бути більше або менше цього показника для штаму в залежності від інгредієнтів. Існують різні методи визначення кількості діючого інфекційного навантаження в одиниці маси або обсягу (титру препарату). Так, кількість життєздатних спор або клітин визначають посівом препарату на живильне середовище з подальшим підрахунком вирослих колоній. Для посіву використовують різні розведення суспензій препарату, що забезпечують ріст не більше 300 і не менше 50 колоній в одній чашці Петрі.
196

РОЗДІЛ 9. МЕТОДИ КОНТРОЛЮ ТА УПРАВЛІННЯ БІОТЕХНОЛОГІЧНИМИ ПРОЦЕСАМИ
Титр визначають за формулою:
Х = N × n,
де N - середньоарифметичне число колоній з двох серій паралельно десятикратних розведень; n - максимальне розведення (10 і); і-кратність розведення.
Як правило, цей метод використовується для бактеріальних і грибних препаратів. Титр вірусних препаратів цим методом не визначають, оскільки віруси не розмножуються на середовищах. У цьому випадку використовують прямий підрахунок кількості діючого початку під електронним мікроскопом, або під світловим мікроскопом у камері Горяєва здійснюють підрахунок великих вірусів ядерного або цитоплазматичного поліедроза. Кількість токсинів, антибіотиків, інших біологічно активних речовин (БАР) визначають хроматографічними, фотометричними і спектрофотометричними методами. Наприклад, спектрофотометричний метод визначення кількості екзотоксину в бітоксібацілліну та інших утримуючих його препаратах заснований на здатності нуклеотидів поглинати УФ-світло в області 260 ... 290 нм. Виділений з препарату екзотоксин гідролізують хлорною кислотою до утворення нуклеотидів і спектрофотомерують. Визначають величину поглинання при 260,270 і 290 нм. Вміст δ-екзотоксину в препараті визначають за формулою:
де С-вміст δ - екзотоксину в препараті,%;m - маса наважки, мкг;
Д270 і Д290-поглинання при довжинах хвиль 270 і 290 нм; V-об'єм вихідної рідини;
n - розведення.
Метод використовують, якщо Д260 і Д270 розрізняються не більше ніж на
10%.
Хід роботи:
1.Провести визначення титру біопрепаратів шляхом підрахунку в камері Горяєва.
2.Описати методи визначення титру біопрепаратів шляхом посіву на живильні середовища, в камері Горяєва або під електронним мікроскопом. Проаналізувати переваги і недоліки всіх методів визначення титру діючого початку.
3.Провести експрес-метод визначення життєздатних клітин бульбочкових бактерій в сухому нітрагіні. Для цього у 99 мл стерильної водопровідної води розводять 1 г сухого нітрагина і витримують на шейкері протягом 2 год. при 200 об/хв. Потім суспензію клітин поміщають
197

РОЗДІЛ 9. МЕТОДИ КОНТРОЛЮ ТА УПРАВЛІННЯ БІОТЕХНОЛОГІЧНИМИ ПРОЦЕСАМИ
в пробірку і забарвлюють розчином прімуліна (кінцеве розведення 1: 1000). Через 15 хв. 0,01 мл забарвлених клітин наносять на предметне скло, накривають покривним склом 18x18 мм, краї якого заливають розплавленим парафіном. Під люмінесцентним мікроскопом МЛ-2 препарат роздивляються і підраховують загальну кількість клітин і відсоток живих клітин в 1 мл суспензії по методу Виноградського - Шульгіною. Прімулін практично не проникає в живі клітини, але накопичується в мертвих. Завдяки цьому при перегляді препарату в світлі люмінесценції при висвітленні об'єкта через об'єктив живі клітини в полі зору тьмяно люмінесцують, а мертві світяться яскравим зеленуватожовтим світлом. Загальна кількість клітин можна визначити в тому ж полі зору також при фазово-контрастному освітленні об'єкта знизу, через конденсор. Кількість життєздатних клітин в 1 г сухого нітрагина визначають з урахуванням того, що для приготування мікроскопічного препарату використовують розведення Нітрагіна 10~ 2.
Робота № 49. Визначення чутливості мікроорганізмів до різних концентрацій біопрепаратів методом паперових дисків
Мета роботи: дослідити ефективність дії різних концентрацій біопрепаратів та фунгіцидів на ріст збудників хвороб методом паперових дисків.
Обладнання та матеріали: чисті культури мікроорганізмів –збудників хвороб (Pectobacterium sp.), бактеріологічні петлі, спиртівки, стерильні пробірки, предметні скла, чашки Петрі з МПА, паперові диски, просочені розчинами препаратів, стерильний фізіологічний розчин, термостат з температурою 37°С.
Хід роботи:
Для визначення антимікробної дії препаратів застосовують метод індикаторних (паперових) дисків.
1.Змийте стерильним фізіологічним розчином культуру бактерій. Для цього в пробірку або чашку Петрі стерильно внесіть 2 - 3 мл фізрозчину. Бактеріологічною петлею обережно зніміть культуру з поверхні агару і ретельно розмішайте в фізіологічному розчині.
2.З отриманої суспензії клітин приготуйте бактеріальну суспензію з концентрацією 500 млн мікробних клітин по стандарту мутності та внесіть
вчашку Петрі з підсушеним стерильним МПА. Рівномірно розподіліть суспензію на поверхні агару і залиште при кімнатній температурі на 30 хв. для адсорбції клітин.
198
РОЗДІЛ 9. МЕТОДИ КОНТРОЛЮ ТА УПРАВЛІННЯ БІОТЕХНОЛОГІЧНИМИ ПРОЦЕСАМИ
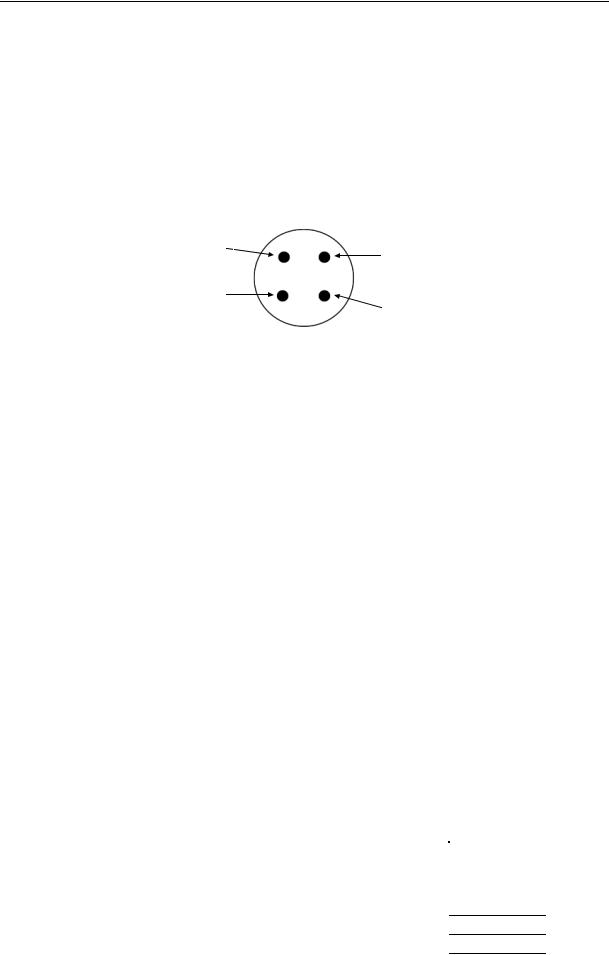
3. Через 30 хв. стерильною піпеткою відберіть надлишок суспензії та помістіть на поверхню засіяної бактеріями середовища на рівному відстані (2,5 - 3,0 см) один від одного і на відстані 1,5 - 2,0 см від краю чашки паперові диски, просочені різними концентраціями препаратів (Рис. 47).
4. |
Інкубуйте посіви |
при температурі |
37°С протягом 24 год. |
5. Через 24 год. виміряйте діаметр зони затримки росту культури |
|||
навколо |
кожного диска і |
визначте ступінь |
чутливості культури за |
наступними
1 |
2 |
|
|
4 |
3 |
|
|
|
|
Рис. 47. Схема розміщення дисків, просочених різними концентраціями препаратів, на поверхні засіяного мікроорганізмами поживного середовища
критеріями:
а) діаметр зони затримки росту більше 25 мм - культура високочутлива; б) від 15 до 25 - чутлива; в) від 10 до 14 - малочутлива;
г) менше 10 мм і повна відсутність - стійка. Чим чутливіші мікроорганізми до препарату, тим ширша навколо диска зона відсутності росту мікроорганізму (стерильна зона). В подальшому вибирають таку концентрацію препарату, яка дає найширшу зону, тобто діє найефективніше.
6. Результати оформіть у вигляді табл. 32.
Контрольні питання:
1.Що таке стандартизація та які показники характеризують якість біопрепаратів і ентомофагів?
2.Яким методом доцільно визначати титр препаратів на основі спор грибів і чому?
Таблиця 32
Визначення чутливості мікроорганізмів до біопрепаратів
Різні |
Найменування або номер дослідної культури |
|||||
1 |
|
|
2 |
|||
концентрації |
Діаметр |
|
Ступінь |
Діаметр |
|
Ступінь |
препаратів |
зони |
|
чутливості |
зони |
|
чутливості |
|
затримки |
|
|
затримки |
|
|
|
росту, мм |
|
|
росту, мм |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
199

РОЗДІЛ 9. МЕТОДИ КОНТРОЛЮ ТА УПРАВЛІННЯ БІОТЕХНОЛОГІЧНИМИ ПРОЦЕСАМИ
3.Назвіть переваги і недоліки методу визначення титру біопрепаратів за допомогою камери Горяєва.
4.В яких випадках слід використовувати методи хроматографії та спектрофотометрії.
5.Яким методом в лабораторних умовах можна найкраще підібрати оптимальні концентрації препаратів, що пригнічують ріст збудників хвороб рослин.
200