Материал: Melnuchuk_Promuslova biotexnologij

РОЗДІЛ 8. ОСОБЛИВОСТІ БІОСИНТЕТИЧНОЇ АКТИВНОСТІ ПРОДУЦЕНТІВ ПЕРВИННИХ ТА ВТОРИННИХ МЕТАБОЛІТІВ
Хід роботи:
Включення клітин Pseudomonas fluorescens в гель альгінату кальцію проводять за такою методикою:
1.3 мл нічної культури бактерій Pseudomonas fluorescens центрифугують 5 хв. при 7000 об/хв.. і ресуспендують в фізіологічному розчині (1,5 мл);
2.Обережно змішують 1,5 мл клітинної суспензії з 1,5 мл 4% розчину альгінату натрію;
3.За допомогою скляної піпетки (обсягом 1-2 мл) отриману суміш скапують з висоти близько 20 см в чашку Петрі з 0,2 М розчином CaCl2;
4.Залишають частинки альгінату кальцію з включеними в них клітинами в розчині CaCl2 на 5 хв. для затвердіння.
5.Для визначення каталази кілька сферичних частинок з іммобілізованими клітинами за допомогою пінцета поміщають в пробірку
зперекисом водню (3% розчин). Ефективність роботи каталази оцінюють по інтенсивності утворення бульбашок водню.
6.Визначення оксидази здійснюють з 1% розчином N'N'- диметилпарафенилендиаміндигидрохлорида (DMPA). Кілька частинок з клітинами поміщають в пробірку з DMPA і витримують при перемішуванні (37°С) 15 хв. Про наявність оксидази буде свідчити забарвлення розчину в рожевий колір.
7.Для визначення наявності нітратредуктази кілька часток з клітинами поміщають в пробірку з 1 мл азотнокислого натрію або калію (1% розчин). Пробірку інкубують при перемішуванні протягом 15 хв. при 37°С. Потім у пробірку вносять 1 мл реактиву Грісса (1% розчин).
8.Враховують реакцію на нітрити: протягом 3-5 хв. з'являється червоне забарвлення.
Контрольні питання:
1.Охарактеризуйте способи іммобілізації клітин і ферментів.
2.Наведіть приклади успішного застосування іммобілізованих клітин і ферментів в практиці.
3.Опишіть переваги та недоліки іммобілізації клітин і ферментів в порівнянні з використанням бактеріальних культур і очищених ферментів.
Робота № 38. Вплив складу живильного середовища на накопичення амілази при твердо фазному культивуванні мікроміцетів
Деякі мікроорганізми здатні використовувати як поживні субстрати самі різні високомолекулярні сполуки: полісахариди, білки, нуклеїнові кислоти, ліпіди та ін. Однак макромолекули не можуть проникати через мембрану клітини. Вони піддаються розщепленню, яке здійснюється під впливом екзоферментів, що відносяться до класу гідролаз. Більшість з них каталізує гідроліз полімеру до розчинних продуктів, зазвичай димерів або
171

РОЗДІЛ 8. ОСОБЛИВОСТІ БІОСИНТЕТИЧНОЇ АКТИВНОСТІ ПРОДУЦЕНТІВ ПЕРВИННИХ ТА ВТОРИННИХ МЕТАБОЛІТІВ
мономерів, які надходять у клітину за допомогою специфічних транспортних механізмів. Утворення екзоферментів широко поширене серед різних груп мікроорганізмів. При пошуку продуцентів ферментів гідролаз в лабораторній практиці застосовують спеціальні методи. Сутність їх полягає в наступному. Мікроорганізми вирощують на агаризованому середовищі, що містить макромолекулярний субстрат. Якщо клітини виділяють в середовище екзоферменти, що гідролізують дані сполуки, то вирослі колонії будуть оточені зоною, в якій виявляються продукти гідролізу.
Крохмаль піддається гідролітичному розщеплення під дією амілаз, активними продуцентами яких є різні види бацил, псевдомонад, стрептоміцетів і міцеліальних грибів.
Мета роботи: вивчення впливу складу і вологості живильного середовища на накопичення амілолітичних ферментів при твердофазному культивуванні мікроскопічного гриба Aspergillus oryzae.
До твердофазної ферментації (культивування) прийнято відносити вирощування мікроорганізмів на твердому, напівтвердому субстраті або твердому носії, інертному до живильних речовин, застосування якого полегшує мікроорганізмам доступ до останніх. Такий тип культивування також називають поверхневим. У роботі пропонується дослідити вплив складу і вологості живильного середовища на рівень накопичення амілолітичного ферменту в процесі вирощування культури мікроскопічного гриба Aspergillus oryzae на твердому сипучому середовищі, що складається з пшеничних висівок і деревної тирси. Амілаза каталізує реакцію гідролізу крохмалю і відноситься до ферментів групи гідролаз. Під дією α-амілази з крохмалю утворюється дисахарид мальтоза, і цей процес називають оцукрювання крохмалю. Оцукрювання лежить в основі приготування сусла з зерна та картоплі в спиртовому виробництві, приготування затору в пивоварінні.
Хід роботи
1. Визначити вологість сировинних компонентів - пшеничних висівок і тирси. Просушити паперові конверти (16 × 16 см) при 160°С протягом 3 хв. і охолодити в ексикаторі. Зважити порожній пакет, заповнити 5 г висівок або тирси і зважити. Розподілити матеріал тонкими шаром і сушити при 160°С 6 хв., охолодити в ексикаторі і зважити. Запис в лабораторному журналі:
Маса порожнього конверта, г ............................................. ...............
Маса конверта з вологим субстратом, г ........................................... .
Маса конверта з висушеним субстратом, г .....................................
Маса випареної вологи ____________, г .......................................
(Найменування середовища)
Вологість _____________, W,% ........................................
172

РОЗДІЛ 8. ОСОБЛИВОСТІ БІОСИНТЕТИЧНОЇ АКТИВНОСТІ ПРОДУЦЕНТІВ ПЕРВИННИХ ТА ВТОРИННИХ МЕТАБОЛІТІВ
(Найменування середовища) Вологість розраховують за формулою:
W=(a-c)x100%/ a-н,
де а – маса конверту з вологою наважкою, г; с – маса конверту з висушеною наважкою, г; н – маса пустого конверту, г.
Результати підрахунків записують до другого десяткового знаку. Виконайте паралельно два визначення вологості пшеничних висівків та тирси, розрахуйте середню величину, результати внесіть до табл.23.
2. Приготуйте 6 варіантів поживного середовища по 20 г, що відрізняються співвідношенням пшеничних висівок та тирси, які приймають участь у розрихлені середовища і регулюванні вмісту крохмалю.
|
|
Результати визначення вологості |
Таблиця 23 |
||||
|
|
|
|
||||
|
|
|
|
|
|
|
|
Номер |
Наймену- |
Маса наважки, г |
Кількість |
Вологість, |
Середня |
||
дослід |
вання |
волога |
вису- |
випареної |
W % |
вологість, |
|
у |
середовища |
|
шена |
вологи, г |
|
W % |
|
1 |
Пшеничні |
|
|
|
|
|
|
|
висівки |
|
|
|
|
|
|
2 |
Пшеничні |
|
|
|
|
|
|
|
висівки |
|
|
|
|
|
|
3 |
Тирса |
|
|
|
|
|
|
4 |
Тирса |
|
|
|
|
|
|
– Розрахуйте масу компонентів для кожного варіанту, зважте на технічних вагах. Приготуйте середовище, змішавши компоненти.
Варіант |
1 |
2 |
3 |
4 |
5 |
6 |
середовища |
|
|
|
70 |
|
|
Пшеничні |
100 |
90 |
80 |
60 |
50 |
|
висівки |
|
|
|
30 |
|
|
Деревна |
0 |
10 |
20 |
40 |
50 |
|
тирса |
|
|
|
|
|
|
–Розрахуйте кількість води, необхідне для зволоження середовища до 60% вологи. Зменшіть розхід води на 1 мл, враховуючи посівний матеріал, що вводиться у вигляді суспензії та конідій. Занесіть дані до таблиці 24.
–Відміряйте необхідну кількість води мірним циліндром, повільно приливаючи її до маси, перемішайте для рівномірного зволоження частинок.
–Зволожену масу перенесіть в конічну колбу, використовуючи металеву воронку для запобігання забруднення поверхні горличка.
173

РОЗДІЛ 8. ОСОБЛИВОСТІ БІОСИНТЕТИЧНОЇ АКТИВНОСТІ ПРОДУЦЕНТІВ ПЕРВИННИХ ТА ВТОРИННИХ МЕТАБОЛІТІВ
Таблиця 24 Результати визначення розходу води для зволоження середовища
Проміжні дані |
|
|
Варіант середовища |
|
|
|
розрахунків |
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Колби закрийте ватною пробкою, паперовим ковпачком та стерилізуйте 30 хв. при 120°С в автоклаві. Вміст колби після стерилізації та охолодження інтенсивно струшують.
3. Для вивчення впливу вологості живильного середовища на накопичення ферментів приготувати 6 варіантів середовища по 20 г з різним вмістом вологи, згідно табл.25.
Таблиця 25
Рекомендуєма вологість живильного середовища
Варіант середовища 1 2 3 4 5 6
Задана вологість,%
Вологість середовища до зволоження, %
Розрахунок води на 20 г середовища, мл
Зважити навіски пшеничних висівок і деревної тирси за варіантом 4. Розрахувати вологість середовища і витрати води до досягнення вологості, зменшуючи його на 1 мл суспензії посівного матеріалу згідно завданням. Алгоритм розрахунку виконати в журналі роботи, результати внести в табл. Подальші операції виконати як в п. 2.
4. Засіяти живильне середовище суспензією спор гриба. Для цього в пробірку з культурою гриба на скошеному агаризованому середовищі заливають стерильну воду до верхнього краю косяка. Конідії переводять кінцем стерильної піпетки у зважений стан і відбирають 1 мл суспензії спор, переносячи її потім в колбу зі стерильним середовищем. Після засіву середовище ретельно перемішують шляхом струшування і пересипають в стерильні кювети, потім закривають її кришкою. Кювети мають перфорації для повітрообміну. Операції по засіву середовища необхідно проводити, дотримуючись асептичних умов, біля полум'я спиртівки. Кювети з засіяним середовищем поміщають в термостат. Вирощування триває 48 - 54 год. при температурі 33°С протягом перших 12 год. росту, а далі підтримується на рівні 28 - 30°С.
174
РОЗДІЛ 8. ОСОБЛИВОСТІ БІОСИНТЕТИЧНОЇ АКТИВНОСТІ ПРОДУЦЕНТІВ ПЕРВИННИХ ТА ВТОРИННИХ МЕТАБОЛІТІВ
Робота № 39. Визначення амілолітичної активності бактерій
Для виявлення амілолітичною активності часто використовують середовище наступного складу (г/л):
–пептон - 10,0;
–КН2РО4 -5,0;
–розчинний крохмаль - 2,0;
–агар - 15,0;
–рН середовища 6,8 - 7,0.
1.Середовище стерилізують при 1,0 атм і розливають в стерильні чашки Петрі.
2.Коли середовище застигне, досліджувані мікроорганізми висівають штрихом по діаметру чашки або уколом. Тривалість культивування 2-10 діб.
3.Гідроліз крохмалю виявляють після обробки агарової пластинки розчином Люголя. Для цього на поверхню середовища наливають 3 - 5 мл розчину Люголя. Середовище, що містить крохмаль, забарвлюється
всиній колір, а зона гідролізу залишається безбарвною або набуває червоно-бурого забарвлення, якщо крохмаль гідролізований до декстринів.
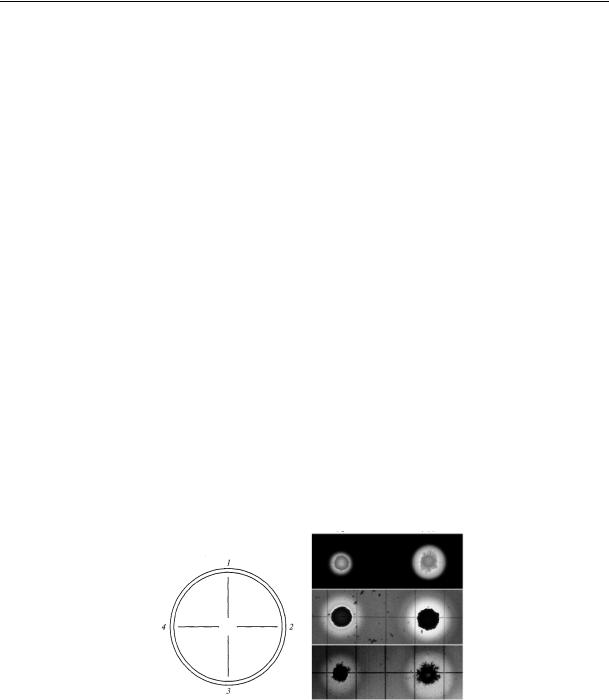
4.Зону гідролізу крохмалю вимірюють в міліметрах від краю штриха (колонії) до кордону світлої зони. Чим більше діаметр світлої зони, тим вищає амілолітична активність (рис.43).
а |
б |
Рис.43. Визначення амілолітичної активності:
а) схема посіву (1-4 – штрихи різних культур); б) середовище з культурами після обробки розчином Люголя
Робота № 40. Визначення амілолітичної активності Aspergillus oryzae
Хід роботи:
1. Провести екстракцію ферментів з вирослої культури гриба. Міцелій з середовища ретельно подрібнюють в кюветі за допомогою шпателя і на технічних вагах відважують 5 г поверхневої культури. Шпатель обов'язково занурити в дезінфікуючий розчин. Зважену порцію
175