Материал: Melnuchuk_Promuslova biotexnologij

РОЗДІЛ 4. ТИПИ ФЕРМЕНЦІЙНИХ ПРОЦЕСІВ
живильний склад, за основу якого прийнята сольове середовище Шлегеля:
Na2HPO4×H2O - 9,1; KH2PO4 - 1,5; MgSO4×H2O - 0,2; Fe3C6H5O7×7H2O - 0,025(г/л). Мікроелементи вводяться за прописом Хоагланда з розрахунку
3 мл стандартного розчину на 1 л середовища. Стандартний розчин містить: H3BO3 - 0,288; CoCl2×6H2O - 0,030; CuSO4×5H2O – 0,08; MnCl2×4H2O - 0,008; ZnSO4×7H2O - 0,176; NaMoO4×2H2O - 0,050; NiCl2 - 0,008 (г/л). В якості субстратів можуть бути прийняті хлористий амоній і фруктоза.
З ферментативного каталізу відомі дві принципово різні найпростіші кінетичні схеми, що призводять до дискримінуємих залежностей швидкості процесу від концентрацій двох субстратів. З урахуванням автокаталітичного процесу мікробного росту ці дві схеми можуть бути представлені в наступному вигляді:
S1+N↔S1N↔ S1S2N→2N+P (1),
S1+N↔S1N→X+P S2+X↔S2X→2N+P (2),
де S1, S2 - концентрації субстратів, N – ненасичена форма клітини, X - «насичена» форма клітини, здатна до поділу; P – продукт.
Механізм (1) включає дві оборотні рівноважні стадії приєднання субстратів (механізм потрійного комплексу). Механізм (2) включає стадії приєднання субстратів, які, принаймні, розділені однією незворотною стадією (пінг-понг-механізм).
Для механізму групи (2) характерна наступна залежність від концентрації субстратів:
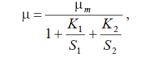 (3)
(3)
де K1 і K2 - ефективні константи спорідненості мікроорганізму до субстратів S1 і S2. Для механізмів групи (1) рівняння питомої швидкості росту може бути записано у вигляді
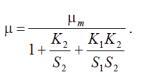 (4)
(4)
Подальші дослідження зводяться до аналізу рівнянь (3) або (4).
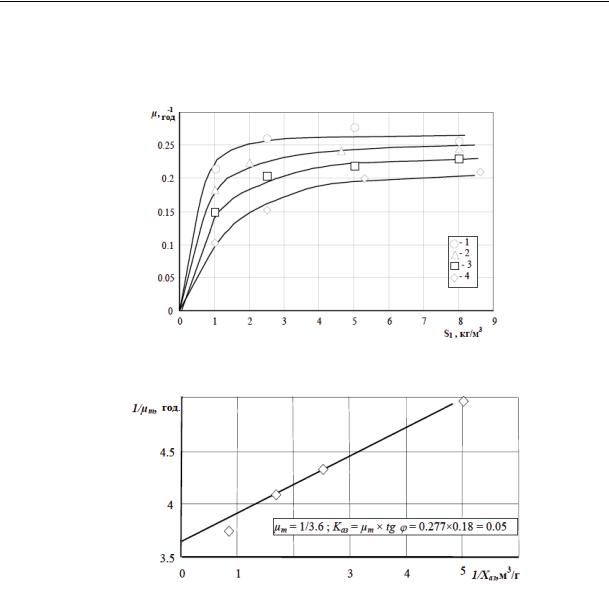
Для цього проводять дослідження і будують залежність виду
μ=f(S1;S2) (Рис.19.)
Обробка експериментальних даних дозволяє отримати значення ефективних констант спорідненості мікроорганізму до субстратів в
обернених координатах. Точки (1 - 3, дані рис.20): 1 - Xфр = 1кг/м3; 2 - 2,5; 3 - 8.
56
РОЗДІЛ 4. ТИПИ ФЕРМЕНЦІЙНИХ ПРОЦЕСІВ
Мета роботи: побудова моделі для розрахунку питомої швидкості росту біомаси в умовах збалансованого субстрату при гетеротрофному культивуванні бактерій Ralstonia eutropha.
Рис. 19. Зміна питомої швидкості росту сумарної біомаси від концентрації фруктози S1. Експериментальні точки (1-4): 1 - S2 = 1,2 кг/м3; 2 - 0,6; 3 - 0,4; 4 - 0,2
Рис. 20. Залежність кінетичних параметрів 1/μm від 1/Xаз
Матеріали та обладнання:
1.Музейна культура штаму Ralstonia eutrophus B-5786;
2.Стерильний розчин базового фосфатного буфера для середовища;
3. Маточні стерильні розчини мікроелементів, заліза лимоннокислого, сульфату магнію і хлористого амонію;
4.Шпателі, спиртівка, мірний посуд, піпетки, колби для вирощування бактерій, гумові пробки з мікробіологічними фільтрами;
5.Термостатуєма качалка.
Хід роботи:
1.Розділитися на 4 групи по числу заданих значень концентрації хлористого амонію в середовищі (0,2, 0,4; 0,6 і 1,2 кг/м3) і концентрації фруктози (1, 2, 4, 8 кг/м3).
2.Кожній групі приготувати варіанти живильного середовища для бактерій із заданим значенням концентрацій фруктози і азоту:
57

РОЗДІЛ 4. ТИПИ ФЕРМЕНЦІЙНИХ ПРОЦЕСІВ
-в мікробіологічному боксі до 0,5 л середовища в стерильних умовах над спиртівкою додати 2,5 мл стандартного розчину заліза, 1,5 мл розчину мікроелементів, 2 мл розчину сульфату магнію і необхідний обсяг розчину хлориду амонію (в 1 мл якого міститься 100 мг солі);
-близько 200 мл середовища відлити;
-залишені 300 мл середовища засіяти інокулятом, для цього змити культуру з одного музейного "косяка" (використовувати шпателі);
-інокулят розлити в ферментаційні колби об'ємом 100 мл;
-колби щільно закрити пробками;
-колби підписати згідно номеру експерименту;
-на ФЕК виміряти оптичну щільність (без розведення) кожного інокуляту;
-колби встановити на качалку.
3.Після закінчення 15 годин культивування через кожні 30 хв. (здійснити чотири повторності) провести вимірювання оптичної щільності
культури та по калібрувальній кривій визначити концентрацію біомаси в культурі, а потім розрахувати питому швидкість росту μ, год-1.
4.Дані представити у вигляді графічної залежності (рис.1).
5.Побудувати залежності 1/μ = f (1/S1) і 1/μ = f (1/S2) і визначити вид механізму і константи, що входять до рівняння (3) або (4).
6.Оформити роботу і зробити висновки.
Контрольні питання:
1.Якими методами визначають питому швидкість росту мікроорганізмів?
2.Періодичне і безперервне культивування.
3.Моделі росту культури.
Робота № 10. Вивчення кінетики росту дріжджів при глибинній ферментації
Існує два способи культивування популяції мікроорганізмів у глибині рідкого середовища: періодичний і безперервний. Вид кривої росту дріжджів змінюється в залежності від умов культивування, але послідовність фаз залишається незмінною.
Для кількісної характеристики культивування мікроорганізмів користуються 2 показниками – середньою та питомою швидкістю росту. Середня швидкість росту V характеризується приростом біомаси за одиницю часу
де х0 – кількість біомаси на початку культивування, кг/м3; х – біомаса за час культивування, кг/м3; t0, t –початковий та кінцевий час відліку, год.
58
РОЗДІЛ 4. ТИПИ ФЕРМЕНЦІЙНИХ ПРОЦЕСІВ
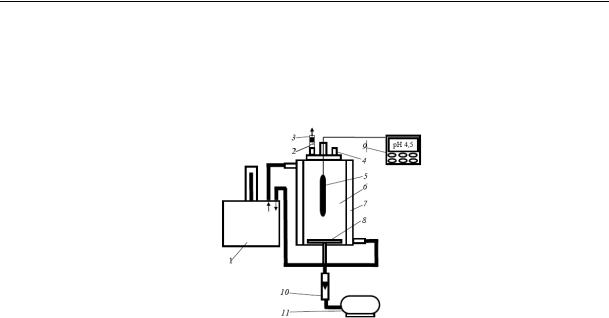
Для вивчення кінетики росту мікробної популяції в умовах глибинної ферментації використовують дріжджі роду Saccharomyces. Експериментальні дані для визначення технологічних показників процесу культивування отримують на лабораторній установці (рис.21).
Рис.21. Схема лабораторної установки для вирощування дріжджів:
1 – ультратермостат, 2 – фільтр очищення повітря; 3 – штуцер виходу повітря, 4- штуцер введення середовища та відбирання проб, 5 – електрод рН-метра, 6 – ємність культиватору, 7 – рубашка, 8 – барботер, 9 -іонометр, 10 –ротаметр, 11компресор.
Установка складається з ємності об'ємом 1 л для вирощування дріжджів (6), забезпеченою барботером (8) для рівномірного розподілу повітря, що нагнітається компресором (11). Відпрацьоване повітря очищається, проходячи систему фільтрів (2). Ємність культиватора забезпечена рубашкою (7), в яку подається вода від ультратермостату (1) для підтримки температури процесу вирощування. Рівні рН і температура середовища вимірюється електродом (5) іонометра (9). Витрата повітря встановлюється ротаметром (10).
Мета роботи: визначення основних технологічних характеристик періодичного процесу глибинної ферментації дріжджів.
Хід роботи:
1.Приготувати 1 л живильного середовища, наступного складу: цукор - 9%; діамоній фосфат - 0,3%; амоній сірчанокислий - 0,16%; хлористий калій - 0,06%; магній сірчанокислий - 0,02%. Заміряти величину рН розчину на іонометр і довести при необхідності до 4,5 70%-ною ортофосфорною кислотою або аміачною водою.
2.Провести асептичну обробку ємності культиватора етанолом. Після чого заповнити його живильним середовищем, відібравши в пробірку 15 мл вихідної суміші для визначення в ній вмісту цукру.
3.Включити ультратермостат і нагріти живильний розчин до температури 30-31°С. Після чого через штуцер (8) ввести через воронку засівну суспензію: дріжджів (посівного матеріалу) в кількості 12% до об'єму живильного середовища. Температура середовища протягом процесу, також як і рН середовища контролюється за допомогою іонометра, електрод якого постійно знаходиться в рідині.
59

РОЗДІЛ 4. ТИПИ ФЕРМЕНЦІЙНИХ ПРОЦЕСІВ
4.Включити компресор 3 і встановити витрати повітря з розрахунку 5 - 10 м3/м3год за допомогою ротаметра (10). Відпрацьоване повітря видаляється через штуцер (3), забезпечений фільтром (2) з активованого вугілля і скловати для затримки крапель середовища і клітин дріжджів.
5.Відлік часу культивування слід починати з моменту внесення в живильне середовище дріжджів. Першу пробу для визначення початкової
концентрації дріжджових клітин х0 відбирають в кількості 1 мл стерильної піпеткою через штуцер (4) через 1 - 3 хв. після початку процесу. Потім
відбір проб проводять через кожну годину для визначення хn - кількості вирослої біомаси.
6.Провести підрахунок кількості дріжджових клітин, використовуючи камеру Горяєва, результати внести в табл. Для підрахунку дріжджів невелику краплю живильного середовища з біомасою клітин відібрати піпеткою або скляною паличкою, нанести її на поверхню лічильної камери і накрити шліфувальним склом, і притерти покривне скло до сторін камери до появи райдужних кілець. Камеру помістити на предметний столик і з об'єктивом 8×, знайти зображення сітки, а потім замінити об'єктив на 40×. Вести підрахунок через 3 - 5 хв. від моменту заповнення. Підрахувати кількість клітин в 10 великих або 20 малих квадратах сітки, розкладених по діагоналі. Врахувати всі клітини, що лежать в квадратику сітки і перетинають верхню і праву сторони квадрата. Визначити середнє число
nср дріжджів в квадраті (табл.8). Число дріжджів в одному квадраті не повинно бути більше 20, в іншому випадку вихідну суспензію розбавляють і повторюють розрахунок.
|
|
Результати розрахунку дріжджових клітин |
|
Таблиця 8 |
||||||
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
Середня |
|
Кількість |
|
|
|
|
|
|
|
|
кількість |
|
|
Час |
Кількість клітин в одному квадраті сітки, шт. |
|
|
клітин в |
||||||
|
клітин, |
|
||||||||
росту |
|
|
|
|
|
|
|
|
1 мл |
|
|
|
|
|
|
|
|
шт. |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
2 |
3 |
4 |
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Кількість клітин в 1 мл суспензії обчислити за формулою :
де Ncр - середнє число дріжджів у квадраті, шт.; h - глибина камери; S - площа квадрата сітки, мм (площа великого квадрату 1/25 мм2; малого –
1/400 мм2).
7. В кожній пробі, починаючи з вихідного моменту культивування, визначити вміст цукру в середовищі, як основного вуглецевовмісного субстрату, а також вимірюють кількість розчиненого азоту.
Одночасно зафіксувати в табл. 9 значення рН середовища та температур за показниками шкали іонометра.
60