Материал: IR1
100
% |
|
|
пропускания, |
80 |
|
60 |
||
Интенсивность |
||
40 |
||
|
20
0
4000 |
3500 |
3000 |
2500 |
2000 |
1500 |
1000 |
500 |
, см-1
vm ghb
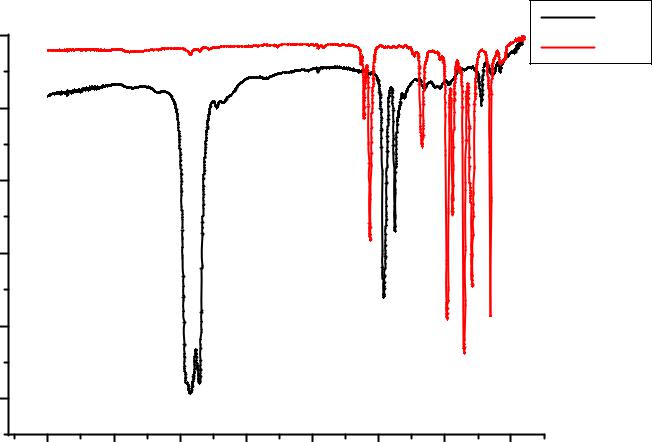
Рис.4.3. ИК спектры вазелинового масла (vm) и гексахлорбутадиена
Задача №2. Исследование ИК-спектров пивалата церия
Введение
Пивалаты (триметилацетаты) редкозумельных элементов (III) представляют собой карбоксилаты с разветвленными алкильными радикалами (терт-бутил) и, в связи с этим, обладают хорошей летучестью, что делает их привлекательными прекурсорами для использования в CVD процессах. В частности, интерес представляет пивалат церия [Ce(Piv)3(HPiv)3]2, т.к. он может быть использован как прекурсор для осаждения тонких пленок оксида церия CeO2, которые применяются в различных областях науки и техники (буферный подслой для осаждения пленок ВТСП, химические сенсоры и т.д.). Также изучение карбоксилатов церия может быть интересно с точки зрения стабилизации Ce (III) и Ce (IV) в координационных соединениях [8].
Нами были проведены исследования ИК–спектров пивалата церия, снятых методом НПВО. Сделаны выводы о структурных превращениях, происходящих с комплексами Ce (III) в процессе синтеза пивалата церия.
Пивалевая кислота как лиганд
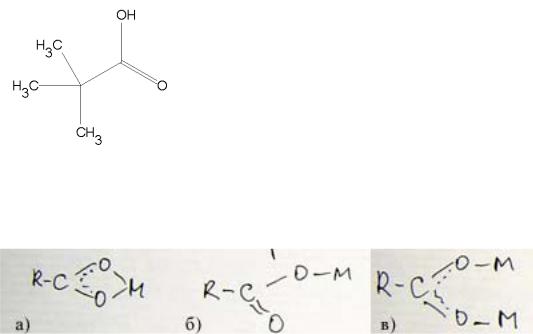
Пивалевая кислота (HPiv) представляет собой карбоксильную органическую кислоту с терт-бутильным фрагментом. Формула пивалевой кислоты представлена на рисунке 4.4.:
Рис. 4.4. Структурная формула пивалевой кислоты
Пивалевая кислота может выступать как лиганд. В случае Ce (III) возможны два варианта координации, которые представлены на Рис.
Рис. 4.5. Возможные типы координации карбоксилатных лигандов
С пивалевой кислотой церий (III) образует биядерный комплекс, где остатки пивалевой кислоты выступают в качестве мостика (см. Рис. в). Дополнительные возможности для координации в комплексе церия (Се (III) – КЧ = 8) могут быть заняты либо водой, либо пивалевой кислотой.
Синтез пивалата церия (III)
Синтез пивалата церия [Ce(Piv)3(HPiv)3]2 проходит в две стадии: 1) Синтез водного пивалата:
Ce(NO3)3 + 3 HPiv (изб.) + x H2O → Ce(Piv)3·xH2O↓ + 3HNO3
2) Перекристаллизация из н-гексана в избытке HPiv: 2Ce(Piv)3·xH2O + 6HPiv → [Ce(Piv)3(HPiv)3]2↓ + 2xH2O
Результаты
Полученный на каждой стадии продукт выделялся и в виде порошка снимался на ИКспектрометре методом НПВО. Полученные спектры представлены на Ошибка! Источник ссылки не найден. и Ошибка! Источник ссылки не найден..7.
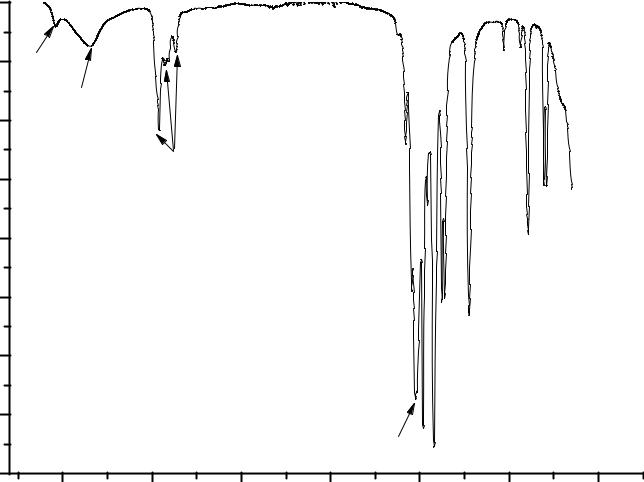
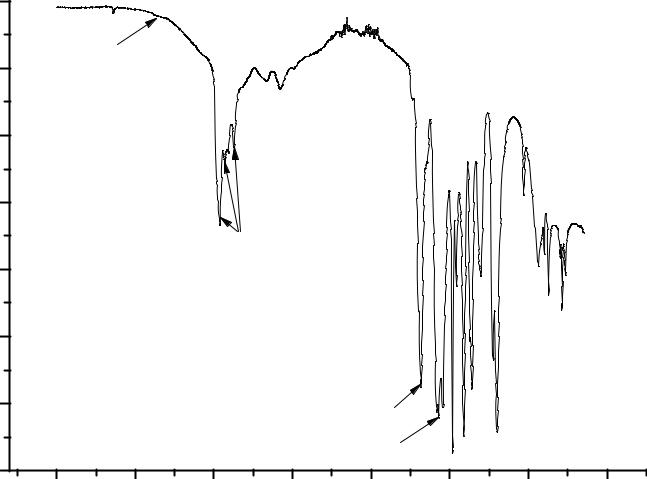
Из приведенного спектра (рис.4.6.) видно, что водный пивалат (продукт первой стадии синтеза) содержит в качестве лигандов как воду, так и гидроксильные группы, а остатки пивалевой кислоты присутствуют в комплексе только в качестве мостиковых лигандов, так как полоса поглощения, относящаяся к СО колебаниям в карбоксильной группе сильно смещена в область низких частот (1520 см-1) по сравнению со значением частоты поглощения СО колебаний свободной карбоксильной группы (1700 – 1780 см-1). Из спектра на Ошибка! Источник ссылки не найден..7. видно, что в пивалате церия, перикристаллизованном из н-гексана в присутствии избытка пивалевой кислоты, отсутствует вода, но присутствуют немостиковые лиганды пивалевой кислоты HPiv. Об этом можно судить по появлению в спектре вещества полосы поглощения с максимумом на 1686 см-1, который соответствует СО колебаниям карбокси-группы в координированной пивалевой кислоте. Положение этого пика также смещено в длинноволновую область по сравнению с СО колебаниями свободной карбоксильной группы, но не так сильно как в случае мостиковых группировок (1520 см-1).
Выводы
1.Методом ИК-спектроскопии исследованы образцы водного и безводного пивалатов церия (III)
2.Проведена интерпретация полученных ИК-спектров, сделаны выводы о координации лигандов воды и пивалевой кислоты в комплексах.
|
100 |
|
|
|
|
|
|
|
,% |
90 |
OH группы |
|
|
|
|
|
|
пропускания |
|
|
|
|
|
|
||
|
CeOH |
|
|
|
|
|
|
|
80 |
OH группы |
|
|
|
|
|
||
воды |
|
|
|
|
|
|
||
70 |
|
CH колебания |
|
|
|
|
|
|
|
метильных групп |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
Интенсивность |
60 |
|
|
|
|
|
|
|
50 |
|
|
|
|
|
|
|
|
40 |
|
|
|
|
|
|
|
|
30 |
|
|
CO колебание в |
|
|
|
||
|
|
|
карбоксильной группе |
|
|
|||
|
|
|
|
|
|
1520 см-1 |
|
|
|
20 |
|
|
|
|
|
|
|
|
|
3500 |
3000 |
2500 |
2000 |
1500 |
1000 |
500 |
|
|
|
|
|
, см-1 |
|
|
|
|
|
|
|
Рис. 4.6. ИК спектр Ce(Piv)3·xH2O |
|
|
||
|
100 |
|
|
|
|
|
|
|
|
, % |
90 |
нет OH колебаний воды |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
пропускания |
80 |
|
|
|
|
|
|
|
|
70 |
|
|
|
|
|
|
|
|
|
|
|
|
CH колебания |
|
|
|
|
|
|
Интенсивность |
60 |
|
|
метильных групп |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
50 |
|
|
|
|
|
|
|
|
|
40 |
|
|
|
|
1686 см-1 |
|
|
|
|
|
|
|
|
|
CO в HPiv |
|
|
|
|
|
|
|
|
|
1570 см-1 |
|
|
|
|
|
30 |
|
|
|
|
CO мостиковые |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4000 |
3500 |
3000 |
2500 |
2000 |
1500 |
1000 |
500 |
|
|
|
|
|
, см-1 |
|
|
|
|
|
|
|
|
Рис. 4.7. ИК спектр [Ce(Piv)3(HPiv)3]2 |
|
|
|
||