Материал: IR1
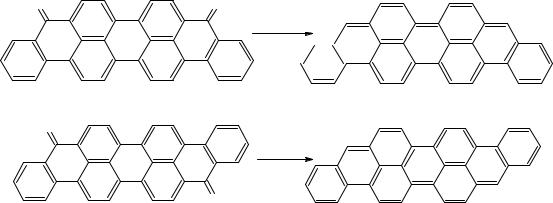
Задача №3. Исследование реакции восстановления хинонов до углеводородов методом ИК-спектроскопии
При восстановлении кетонного кислорода в хинонах (виолантрон и изовиолантрон) под действием цинковой пыли (схемы реакций приведены на рис.4.8.) оказалось, что продукты и исходные вещества в реакциях сходны по химической структуре и подвижности в хромотографических системах, что сильно затрудняет их анализ с помощью этих методов. Возникла необходимость экспрессной оценки эффективности реакции. Для этого был проведен анализ ИК-спектров исходных веществ и продуктов реакции. Спектры виолантрона и продукта его восстановления – виолантрена приведены на рис.4.9., а спектры изовиолантрона и продукта его восстановления – изовиолантрена приведены на рис.4.10.
а O |
O |
ZnCl2-NaCl
Zn, H2O 
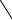
виолантрон |
виолантрен |
O
б
O
ZnCl2-NaCl
Zn, H2O
изовиолантрон |
изовиолантрен |
Рис.4.8. Схемы реакций восстановления кетонного кислорода в виолантроне (а) и в изовиолантроне (б)
Из ИК-спектров видно (см. рис.4.9. и рис.4.10.), что интенсивность поглощения С=О колебаний значительно уменьшается после восстановления относительно других полос в спектре, что свидетельствует о прохождении реакции восстановления хинонов. Также появляется высокоинтенсивный пик около 890 см-1, который соответствует появлению нового колебания в системе С-Н связей на ароматическом ядре.
Таким образом, с помощью ИК-спектроскопии было доказано, что реакция восстановления хинонов цинковой пылью действительно протекает.
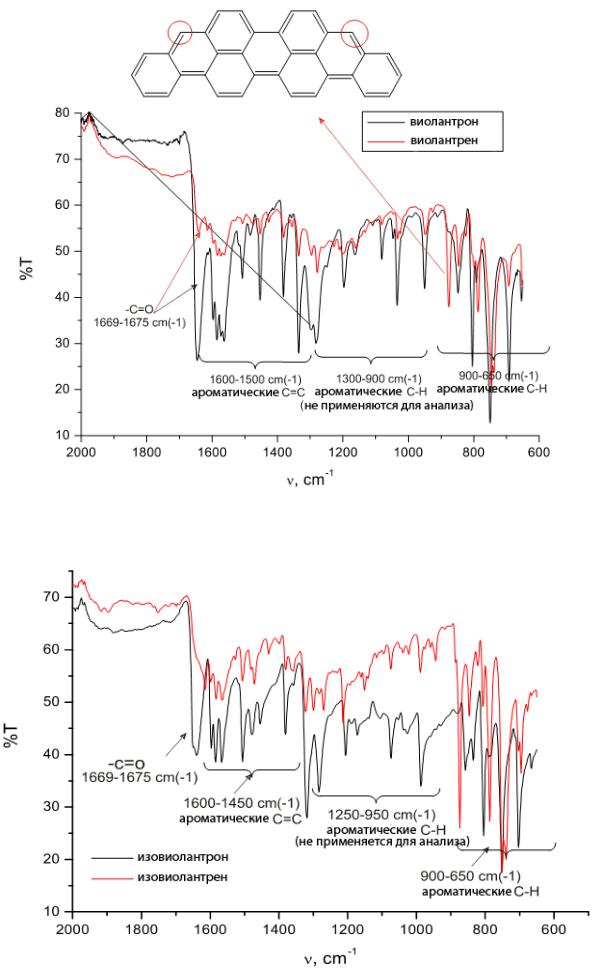
Рис. 4.9. ИК спектры виолантрона и продукта го восстановления – виолантрена.
Рис. 4.10. ИК спектры изовиолантрона и продукта го восстановления – изовиолантрена.
Задача № 4. Исследование процесса образования водородной связи в растворах этилового спирта в четыреххлористом углероде методом ИКспектроскопии
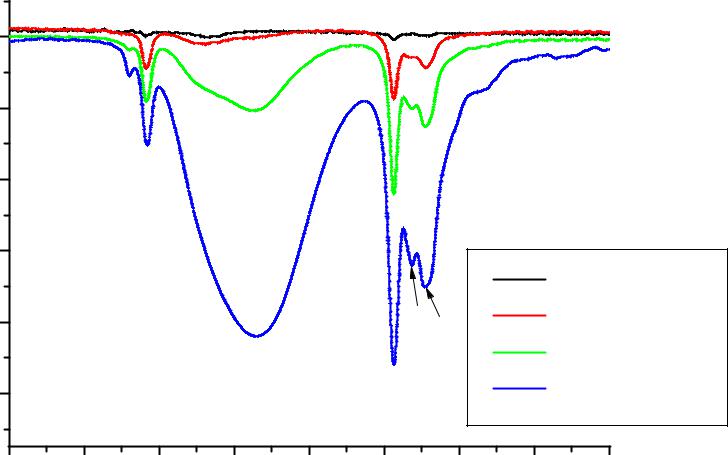
Известно[9], что молекулы этилового спирта образуют между собой водородную связь. Целью данной задачи стало исследование этого процесса в растворах этилового спирта в четыреххлористом углероде различной концентрации. На рис.4.11. приведены спектры пропускания с растворов C2H5OH в ССl4 c различной концентрацией этилового спирта. Полосы валентных колебаний CH групп при 2974, 2926 и 2890 см-1 не изменяются с изменением концентрации (см. рис.4.11, табл. 4.3.). Полосы поглощения 3631, 3508 и 3343 см-1 связаны с поглощением мономерной, димерной и полимерной гидроксильных групп, соответственно. Этиловый спирт существует в мономерной форме при концентрациях, не превышающих 0,01 М, а сильное поглощение полимерной группы OH становится явным при концентрации 1,0 М.
Полоса 3631 см-1, обусловленная концевым “мономерным” гидроксилом, в истинном мономере слегка сдвинута в сторону более высоких частот (концевой гидроксил поглощает при 3620 см-1, а мономер – при 3650 см-1).
CH3-CH2 CH3-CH2 CH3-CH2
–O–H—[—O–H—]n—O–H
3515 см-1 3343 см-1 3631 см-1
Таким образом, методом ИК-спектроскопии был исследован процесс образования водородной связи в растворах этилового спирта в четыреххлористом углероде.
Таблица 4.3. Частоты колебаний некоторых групп атомов в растворах C2H5OH в
CCl4
|
|
Частота колебаний, см-1 |
Характеризация |
3631 |
поглощение мономерной гидроксильной группы |
3508 |
поглощение димерной гидроксильной группы |
3343 |
поглощение полимерной гидроксильной группы |
2974 |
валентные колебания -CH группы |
2926 |
|
2890 |
|
|
100 |
|
|
|
|
|
|
|
|
|
|
|
Интенсивность пропускания |
|
|
|
-1 |
|
|
|
|
|
|
|
|
80 |
|
|
3508 см |
|
|
|
|
|
|
|
|
|
|
|
-1 |
|
|
|
|
|
|
|
|
||
60 |
|
3631 см |
|
|
|
|
|
|
|
|
||
40 |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
0,01M C2H5OH |
|||||
20 |
|
|
|
|
-1 |
1- |
0,1M C H OH |
|||||
|
|
-1 |
|
|
2926см |
2890 см |
|
2 |
5 |
|||
|
|
|
|
0,25M C2H5OH |
||||||||
|
|
3343 см |
|
1 |
||||||||
0 |
|
|
- |
1M C2H5OH |
||||||||
|
|
2974 см |
||||||||||
|
|
|
|
|
|
|||||||
|
4000 |
3800 |
3600 |
3400 |
3200 |
3000 |
|
2800 |
2600 |
2400 |
|
|
|
|
|
|
|
|
, см-1 |
|
|
|
|
|
|
|
Рис.4.11. Спектры пропускания с растворов C2H5OH в ССl4 c различной концентрацией этилового спирта |
|
||||||||||
Задача № 5. Количественный анализ
Карбонат-гидроксиапатиты (карбонат ГАП) являются весьма перспективными биоматериалами, пригодными для восстановления или даже замены поврежденных костей, суставов и зубов [10].
Получающиеся при синтезе карбонат-гидроксиапатиты с различной степенью замещения гидроксильных групп и фосфат-ионов на карбонат-ионы обладают различными свойствами. В связи с этим, исключительно важной задачей является определение степени замещения карбонат ионов на анионы ГАП. При этом карбонат-ионы могут замещать в гидроксиапатите гидроксильные группы (карбонат-ГАП А типа) или фосфат-ионы (карбонат-ГАП Б типа) или и гидроксильные группы и фосфат-ионы (карбонат ГАП смешанного АБ типа).
Одним из наиболее подходящих методов для решения этой задачи является метод ИК-спектроскопии, который позволяет количественно определить содержание карбоната, замещающего те или иные ионы, поскольку частоты колебаний карбонат-ионов в карбонат-ГАП А и Б типа будут отличаться.
В рамках данной задачи практикума проводился количественный анализ карбоната кальция в его механической смеси с гидроксиапатитом методом ИК-спектроскопии с использованием приставки для снятия спектров диффузного отражения. На первом этапе настоящей работы проводился подбор оптимальной концентрации ГАП в его смеси с бромидом калия. Для этого были сняты ИК-спектры со смесей с массовым отношением гидрокисапатита и бромида калия 1/15, 1/7, 1/3, 1/1 (рис.4.12.). При соотношении ГАП:KBr = 1:15 интенсивность колебаний недостаточно высока, однако при увеличении соотношения ГАП:KBr до 1/1 полосы колебаний уширяются и размываются. В связи с чем, в качестве оптимальной концентрации ГАП было выбрано соотношение ГАП:KBr=1:7, которое было использовано в дальнейшем количественном анализе карбоната кальция в его механической смеси с гидроксиапатитом.