Материал: 4 2015

Метод Хартри-Фока для молекул Зафиксируем ядерную конфигурацию молекулы. Тогда для анализа электронного поведения молекул достаточно рассматривать только электронное уравнение Шредингера. Чтобы решить его
используют приближения, введенные в квантовой химии атома, и прежде
всего - метод Хартри-Фока:
FΨ = εiΨ
|
1 |
N |
N |
N |
N |
|
|
2 |
1 |
|
|
1 |
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
F = − |
∑ i2 − ∑ |
Z |
+ ∑∑ |
∫ |
χ j (x2 ) |
|
dx2 |
− |
∫ |
χi*(x2 ) |
χ j |
(x2 )dx2 |
||||||
|
|
|
|
|
|
|||||||||||||
2 |
i |
i ri |
i |
j |
|
|
x12 |
2 |
|
x12 |
|
|
||||||
|
|
|
||||||||||||||||
Детерминант Слейтера - |
приближение к N-электронной волновой |
|||||||||||||||||
функции молекулы - составляется из занятых электронами молекулярных орбиталей (МО) ϕi( x ):
11

Каждая МО ϕi(x) = ϕi(x)η(s) описывает поведение одного электрона
в поле остальных электронов и всех ядер, т.е. является одноэлектронной.
ϕi(x) характеризуется своим значением энергии εi - собственным значением оператора Фока молекулы.
Электроны заполняют МО в порядке повышения энергии молекулы.
Полная ХФ энергия молекулы с замкнутыми оболочками
12

Замечания.
1)В минимизации энергии участвуют только занятые электронами МО, следовательно лишь они являются найденными физически обоснованно. Метод ХФ дает также характеристики свободных МО,
которые соответствуют возбужденным энергетическим уровням молекулы с ошибкой ~100%.
Такие МО называются виртуальными.
13
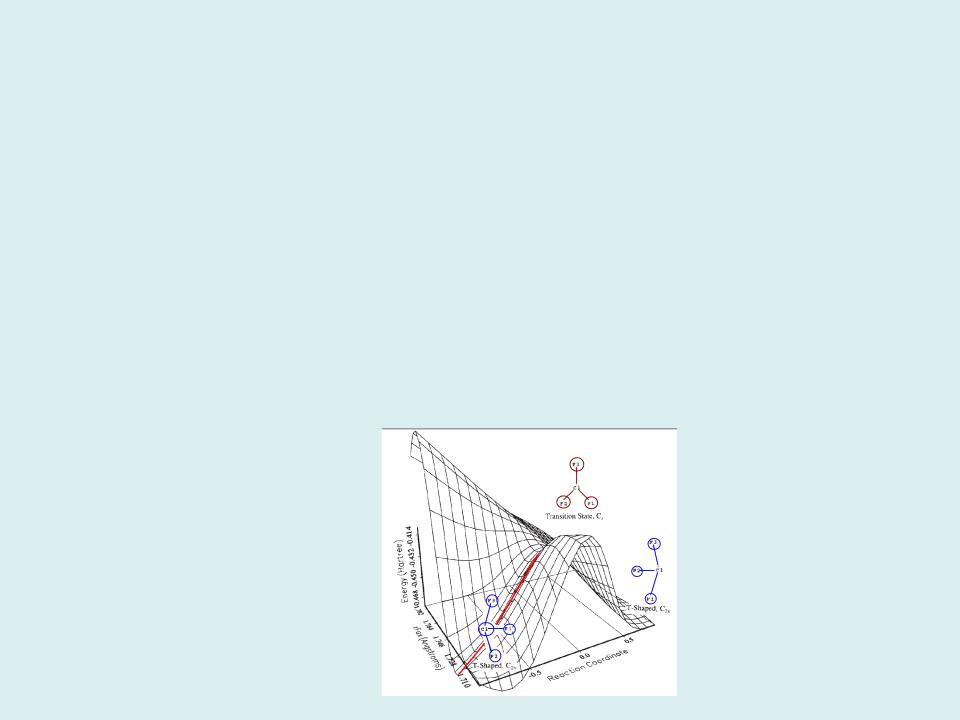
2) В дополнение к ХФ энергии, для оптимизации геометрии молекулы и определения частот гармонических колебаний ядер, вычисляются первые и вторые производные полной энергии относительно ядерных координат. Минимум полной энергии соответствует наилучшей геометрии молекулы, а диагонализация матрицы вторых производных, (силовых постоянных) молекулы, дает частоты нормальных колебаний.
Стационарные точки энергетической потенциальной поверхности (точки, где первые производные энергии по ядерным координатам обращаются в нуль) -это минимум, максимум или седловая точка. Анализируя расположение и типы точек, можно охарактеризовать превращения молекул в ходе химических реакций.
14
Приближение МО ЛКАО. Уравнения Рутана
Уравнения Хартри-Фока для молекул
Численное решение |
МО ЛКАО решение уравнений ХФ и |
|
интерпретация результатов упрощается |
||
|
МО электрона, который находится в данный момент вблизи некоторого ядра, должна быть близка к соответствующей АО. Каждую МО можно представить как линейную
комбинацию всех АО системы:
φi (r) = ∑ci χ (r)
Одна и та же АО входит в разные МО с разными коэффициентами разложения сiµ
С учетом ортонормированности МО, из условия минимума энергии получают уравнения ХФ в виде уравнений Рутана
N |
|
∑ciµ (Fµν − EiSµν ) = 0, |
=1,2...N |
ν =1 |
|
Элементы матрицы Фока Fµν в приближении МО ЛКАО имеют вид:
Fµν = hµν + ∑∑∑cjλcjσ |
µν |
|
λσ |
− |
1 |
µλ |
|
νσ |
|
|
|
|
|
||||||||
|
|
|
||||||||
j λ σ |
|
|
|
|
2 |
|
|
|
15 |
|
|
|
|
|
|
|
|
|
|
|
|