Материал: 4 2015
Квантовая химия молекул
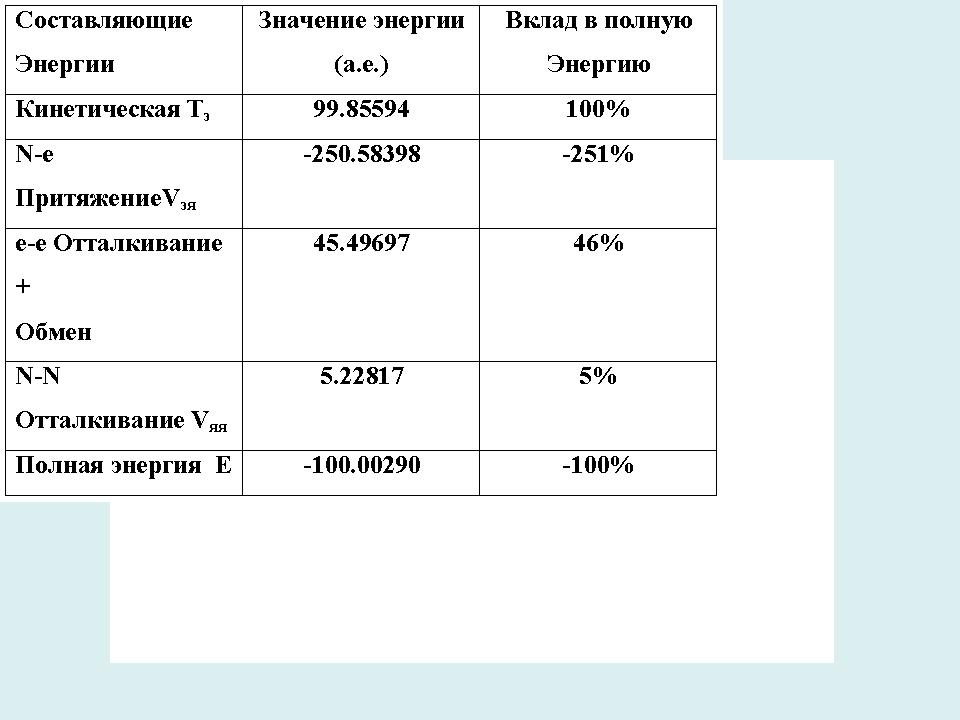
Энергия молекулы состоит из кинетических энергий каждого электрона и ядра и парных энергий их кулоновских взаимодействий.
Вклады в молекулярную энергию фтористого водорода HF
1
Основное уравнение молекулярной квантовой химии – независящее от времени нерелятивистское уравнение Шредингера:
Н Ψ ({r, R}) = Е Ψ({r, R})
{r, R} - совокупность координат всех электронов и ядер.
Гамильтониан молекулы:
Н= = Tя ( R) + Тэ (r) + Vяя(R) + Vэя (r,R)+ Vээ(r)=
-(ħ2/2)∑(1/ Mа ) 2а – (ħ 2/2m) ∑ 2i +
+∑∑ ZaZb e2/4πε0Rab - ∑∑ Za e2/4πε0rab + ∑∑ e2/4πε0rij
2

Приближение Борна-Оппенгеймера Электрон-ядерное взаимодействие Vэя описывает связывание и пренебречь им нельзя.
Hмол зависит от координат электронов и ядер и Ψточн не разделяется на ядерную и электронную части.
Приближение Борна-Оппенгеймера: зафиксируем R и рассчитаем Ψэл , т.е.
сделаем зависимость электронной волновой функции Ψэл от расположения ядер R параметрической.
Тогда молекулярная волновая функция может быть записана как
Ψмол ({r,R})=Ψэл({r,R})Ψяд ({R})
а уравнение Шредингера
НΨмол({r, R})=ЕΨмол ({r, R}) |
|
заменяется двумя другими. |
3 |

1) Ψэл удовлетворяет электронному уравнению Шредингера
НэΨэл=ЕэлΨэл,
где
Hэ = Tэ(r) + Vяя(R) + Vэя(R,r) + Vээ (r) .
Электронная энергия Еэ зависит от координат ядер, как от параметров.
2) mэ/Mz ≤ 1/1836 и движение ядер много медленнее, чем электронов. Часто положения ядер можно считать фиксированными. Тогда уравнение Шредингера для Ψяд имеет вид
(Tя +Eэл )Ψяд =EΨяд
Электронная энергия Еэл (адиабатический потенциал) играет роль потенциальной энергии. Тя – колебательно-вращательная энергия ядер.
4

Полная энергия молекул в приближения Борна-Оппенгеймера:
Е = Е эл + Т я
Рассчитывая Еэл для разных значений {R}, получим поверхность потенциальной энергии (ППЭ), вдоль которой ядра перемещаются в энергетическом пространстве.
5