Материал: 2674
|
|
6 |
|
OH |
OH |
OH |
OH |
|
CH2OH |
|
|
|
/ |
CH2 |
CH2 |
|
+ n |
+ n CH2=О -nH2O |
|
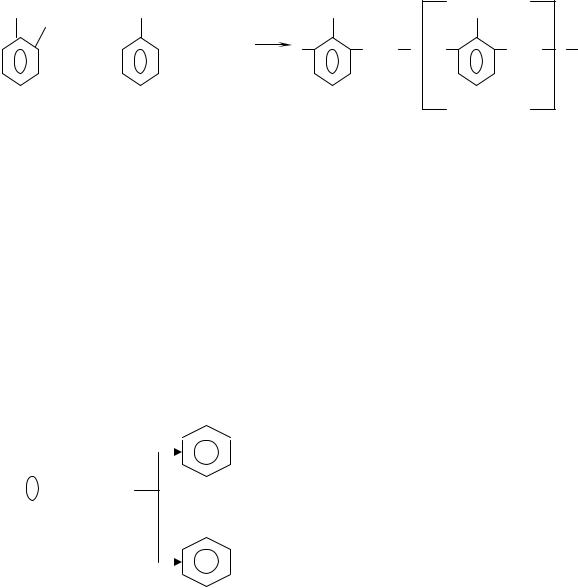
новолак n
Новолачная фенолоформальдегидная смола является термопластичным полимером. Она плавится при нагревании и затвердевает при охлаждении без изменения химической структуры полимера. Легкорастворима в различных растворителях.
По-другому идет реакция в присутствии щелочных катализаторов. В щелочной среде (катализаторы – аммиак, едкий натр, едкий барий) при избытке формальдегида на начальной стадии образуются диметилольные производные фенола:
ОН
ОН |
НОСН2 |
СН2ОН 2,6-диметилолфенол |
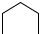 + 2СН2 =О
+ 2СН2 =О
ОН
СН2ОН
2,4 – диметилолфенол
СН2ОН
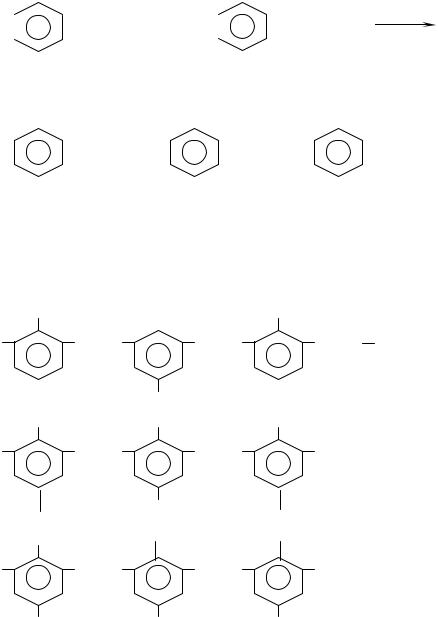
При нагревании диметилолфенолы конденсируются с выделением воды за счет гидроксида метилольных групп и подвижных атомов водорода бензольного кольца с образованием резола. При этом рост цепи может происходить линейно (с увеличением длины боковых ответвлений за счет свободных метилольных групп в n–положении по отношению к фенольному гидроксилу).
Полученная таким образом резольная смола является термореактивным полимером.
Термореактивные резольные смолы отверждаются, то есть превращаются в трехмерный пространственный полимер – резит при нагревании их до 80-2000 С. Реакция идет с выделением воды за счет свободных метилольных групп.
|
|
|
|
|
|
|
|
|
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ОН |
|
|
|
ОН |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
n НОСН2 |
|
|
|
СН2ОН |
|
|
|
|
|
СН2ОН |
|||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
-n H2O |
|||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СН2ОН |
|
|
|
|
|
|
|
||||
|
|
|
|
ОН |
|
|
|
|
|
|
ОН |
|
|
|
|
|
ОН |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
…- |
|
|
|
|
|
|
СН2 |
|
|
|
|
|
|
|
|
СН2 |
|
|
|
|
|
|
|
|
СН2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
n |
|
|
|
|
|
|
|
m |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
СН2ОН |
|
СН2ОН |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
Резит может быть получен также из новолака при нагревании его в щелочной среде с дополнительной порцией формальдегида:
|
ОН |
|
ОН |
|
|
СН2 |
СН2 |
СН2 |
… + n СН2О → |
|
|
ОН |
|
|
|
ОН |
СН2 … |
ОН |
|
|
СН2 |
СН2 |
… |
|
|
|
|
||
|
|
ОН |
|
резит |
|
СН2 |
ОН |
СН2 |
|
… |
СН2 |
СН2 |
СН2 … |
|
|
ОН |
СН2 … |
ОН |
|
Отверженная смола не разлагается при нагревании до 200 0С и не набухает в растворителях, обладает хорошими диэлектрическими свойствами, механической прочностью и твердостью, стойкостью к воздействию воды, растворителей и разбавленных кислот.
Фенолоформальдегидные смолы (ФФС) находят широкое применение в производстве различных видов пластмасс (фенопласты). Большие количества резольных смол применяют для производства слоистых пластиков из ткани и бумаги. ФФС – основа спиртовых лаков, политур, применяемых при отделке изделий из дерева. Для них характерна высокая скорость отверждения.
8
Резольные ФФС используют для изготовления электроизоляционных и химически стойких лаков. Широкое применение нашли клеи на основе резольных фенолоформальдегидных смол в технологии деревообработки. Они используются для склеивания конструкций из древесины, металлов и пластмасс с древесиной, для изготовления фанеры. Клеи на основе резольных смол обладают высокими диэлектрическими показателями, водостойкостью, химической стойкостью.
Новолачные ФФС используются в качестве связующего при производстве пресспорошков, из которых изготавливаются различные строительные детали в виде арматуры, плит, труб.
Экспериментальная часть
Опыт 1.1. Получение новолачной ФФС
Помещают в пробирку 2,5 г фенола, 2 мл 40 % формалина, вносят кипятильный камешек. Нагревают смесь с холодильником до образования однородной жидкости и осторожно кипятят ее 1-2 мин. Затем вливают из пипетки или из другой пробирки 0,2 мл (несколько капель) концентрированной соляной кислоты (катализатор). При встряхивании горячая смесь начинает кипеть без подогревания через 1-2 мин. Жидкость мутнеет и внизу отслаивается тяжелое, непрозрачное масло. Если кипение прекращается, снова подогревают смесь на открытом огне 1-2 мин. Сливают верхний мутный слой и добавляют в пробирку примерно такой же объем воды, сливают воду, а смолу с остатками воды выливают на часовое стекло. Остывшую светло-сиреневую смолу снимают со стекла, высушивают в фильтровальной бумаге, снимают комочек и взвешивают. При хранении она постепенно твердеет и делается хрупкой тем быстрее, чем дольше продолжалось кипячение.
Опыт 1.2. Получение резольной ФФС
Помещают в пробирку 3 г фенола и 10 мл 40 % формалина. Смесь нагревают с холодильником на водяной бане до полного растворения фенола. Осторожно в слегка остывшую смесь вводят 3 мл концентрированного раствора аммиака (NH4OH – катализатор) и продолжают нагревание на горячей водяной бане (t = 80-90 0С) еще 10-15 мин. По окончании реакции происходит расслое-
9
ние смеси на верхний водный слой и нижний слой (прозрачная желтокоричневая смола). Резольная смола образуется несколько медленнее новолачной и в меньшем количестве.
Водный слой сливают, смолу вливают в пробирку и проводят опыт 1.3.
Примечание: необходимо тщательно проводить нагрев, так как при недостаточной продолжительности нагревания смола в опытах 1.1, 1.2 получается липкой и почти не твердеет.
Опыт 1.3. Резит из резольной смолы
Часть полученной в опыте 1.2 смолы осторожно нагревают на открытом огне в сухой пробирке, держа пробирку горизонтально. При этом удаляется избыток воды, а смола при продолжительном нагревании вспучивается и затвердевает. Образуется неплавкий и нерастворимый резит.
Вопросы и задания
1.Какие вещества используются в качестве мономеров при поликонденсации? Приведите пример.
2.Что такое функциональность мономера? Чему равна функциональность фенола, формальдегида?
3.Что такое олигомеры?
4.Напишите реакцию поликонденсации фенола с избытком формальдегида в кислой среде, выделите элементарное звено. Назовите полученную смолу.
5.К чему приводит нагревание новолачной ФФС в присутствии формальдегида? Напишите реакцию.
6.Чем отличаются термореактивные полимеры от термопластичных?
7.Напишите реакцию образования новолачной смолы из n-крезола и формальдегида.
8.Какой из трех изомерных диоксибензолов наиболее активен в реакции конденсации с формальдегидом?
9.Напишите реакцию резорцина с формальдегидом:
а) в кислой среде, б) в щелочной среде. 10.Каковы особенности реакции поликонденсации?
11.Как проявляется ступенчатый характер поликонденсации при реакции фенола с формальдегидом?

10
Лабораторная работа № 2
Поликонденсация карбамида с формальдегидом
Цель работы: ознакомиться с особенностями синтеза карбамидоформальдегидных (мочевиноформальдегидных) смол, влиянием различных факторов на процесс поликонденсации.
Теоретическая часть
Одной из важнейших реакции поликонденсации, нашедшей широкое техническое применение, является реакция карбамида (мочевины) с формальдегидом. Характер и скорость взаимодействия карбамида с формальдегидом в водном растворе зависят от условий реакции: катализатора, рН среды, температуры, соотношения исходных веществ, а также их концентрации в реагирующей среде. При этом влияние рН среды на молекулярную массу и структуру карбамидоформальдегидных смол (КФС) является определяющим. Рассмотрим влияние отдельных факторов на эту реакцию.
Влияние pH среды. В нейтральной или слабощелочной среде при температуре, не превышающей 40 оС, в зависимости от соотношения карбамида и формальдегида образуется преимущественно моноили диметилолкарбамид. При молярном соотношении карбамида и формальдегида 1:1 образуется преимущественно монометилолкарбамид.
NH2 |
|
NHCH2OH |
|
NHCH2OH |
|
|
|
NH4OH |
|
NH4OH |
|
CO + |
CH2O |
CO |
+ |
CH2O |
CO |
|
|
|
|
|
|
NH2 |
|
NH2 |
|
|
NHCH2OH |
мочевина |
формаль- |
монометилол- |
|
формаль- |
диметилол- |
(карбамид) |
дегид |
мочевина |
|
дегид |
мочевина |
Метилолкарбамиды растворяются в воде и образуют вязкие растворы. При нагревании этих растворов при 100о в слабощелочной среде в присутствии NH4OH происходит поликонденсация монометилолкарбамида с отщеплением воды и образованием макромолекул линейного строения (полиметиленкарбамиды):