Материал: 2674
31
Лабораторная работа № 7
Определение содержания свободного формальдегида в карбамидных смолах
Цель работы: ознакомиться с методом химического анализа карбамидной смолы на содержание свободного формальдегида.
Теоретическая часть
Мочевино-формальдегидные (карбамидные) смолы широко применяются в деревообрабатывающей промышленности для производства древесностружечных и древесно-волокнистых плит, склеивания массивной и слоистой древесины, получения покрытий, пропитки бумаги, шпона, как связующие в лаках, клеях, для изготовления пластмасс.
Содержание свободного формальдегида в смолах характеризует токсичность смолы, создает загазованность промышленных помещений, цехов деревообрабатывающих и мебельных производств, нарушает условия труда, отравляюще действует на организм человека. Предельно допустимая концентрация свободного формальдегида в смолах составляет 1,5 %. Для отдельных марок смол она составляла 0,15-0,20 %. Количественное определение свободного формальдегида можно осуществить различными способами: с помощью реакции присоединения по альдегидной группе (например, NaHSO3) или с помощью реакции замещения кислорода при реакции альдегида с гидроксиламином, гидразином и др.
В данной работе приводится сульфитный способ определения содержания свободного формальдегида в смоле. Определение проводится методом обратного титрования по следующим реакциям:
Na2SO3 + HCl → NaHSO3 + HCl
избыток
+δ -δ
CH2=O + NaHSO3 → CH│ 2-OH SO3Na
HCl + NaOH → NaCl + H2O
( т и т р о в а н и е )
32
Экспериментальная часть
В конической колбе емкостью 200-250 мл взвешивают 1 г смолы с точностью до 0,002 г и растворяют в 50 мл дистиллированной воды. Вводят в полученный раствор 20 мл 0,1 н раствора H2SO4 (или HCl) и 25 мл 25 % -го свежеприготовленного раствора сульфита натрия, добавляют 2-3 капли индикатора тимолфталеина. Избыток кислоты титруют 0,1 н раствором едкого натра до появления слабо-синей окраски. Записывают объем NаОH, израсходованный на титрование.
Параллельно проводят контрольный опыт. Для этого в коническую колбу помещают 50 мл дистиллированной воды, вводят 20 мл 0,1 н раствора серной или соляной кислоты и 25 мл 25 %-го свежеприготовленного раствора сульфита натрия, добавить 1-2 капли тимолфталеина. Избыток кислоты титруют 0,1 н раствором едкого натра до появления слабо-синей окраски.
Содержание свободного формальдегида рассчитывают по формуле
Х = |
0,003(а −в)k |
100% , |
(13) |
|
c |
||||
|
|
|
где 0,003 – количество формальдегида, соответствующее 1 мл 0,1 н раствора; а – объем 0,1 н раствора NaOH в контрольном опыте, мл:
в– объем 0,1 н раствора NaOH , израсходованный на титрование испытываемого раствора, мл:
с – навеска смолы, г:
k – поправочный коэффициент 0,1 н раствора NaOH (0,95÷1,0).
Вопросы и задания
1.Сделайте вывод о токсичности смолы и пригодности ее для использования в мебельной промышленности.
2.Какова роль индикатора в процессе определения?
3.Что значит понятие «свободный формальдегид» в смоле?
4.Почему в феноло- и карбамидоформальдегидных смолах есть свободный формальдегид и каковы пути снижения его содержания?
5.Каково элементарное звено КФС?
6.Какие вещества используются в качестве отвердителей КФС?
33
Лабораторная работа № 8
Определение степени набухания полимеров
Цель работы: ознакомиться с теорией набухания полимеров; определить степень набухания полимера, используя объемный метод.
Теоретическая часть
Растворы полимеров отличаются повышенной вязкостью и проявляют ряд термодинамических аномалий. Кроме того, полимеры способны значительно набухать в жидкостях и образовывать ряд систем, промежуточных между твердым телом и жидкостью.
Растворение высокомолекулярных соединений принято рассматривать как процесс смешения двух жидкостей. Основная особенность растворов полимеров – их неидеальное поведение даже при незначительных разбавлениях.
Растворение полимеров с линейными и гибкими макромолекулами сопровождается набуханием – процессом, в котором происходит не только диффузия молекул растворяемого вещества в растворитель, (как у НМС), но, главным образом, диффузия молекул растворителя в высокомолекулярное соединение. Это связано с тем, что макромолекулы в обычных аморфных полимерах упакованы сравнительно неплотно и в результате теплового движения гибких цепей между ними образуются весьма малые пространства, в которые могут проникать молекулы растворителя, обладающие малыми размерами и большой подвижностью.
Набухание не всегда заканчивается растворением. Очень часто после достижения некоторой степени набухания процесс прекращается. Одна из причин такого явления – ограниченное смешение полимера и растворителя, другая – в том, что между молекулами полимера существуют поперечные химические связи. Чем больше последних, тем меньше степень набухания.
Экспериментальная часть
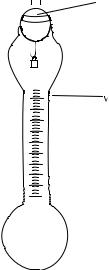
Определение набухания проводится в приборе, состоящем из двух стеклянных шариков, соединенных градуированной трубкой объемом 2 мл (рис. 3). Через отверстие верхнего шарика заливается растворитель до верхней метки трубки (V1).
34
Взвешенный с точностью до 0,01 г на воздухе образец полимера (а) накалывают на проволоку и подвешивают к пробке, которой закрывают верхний шарик. Прибор переворачивают так, чтобы растворитель покрыл полимер, выдерживают 1 час и возвращают в исходное положение.
|
|
|
а |
По шкале отмечают объем растворителя после по- |
|
|
|||
|
|
|
|
|
|
|
|
|
глощения (V2). Находят V = V1 – V2, т. е. количество |
|
|
|
|
|
|
|
|
|
поглощенного растворителя. Из полученных данных |
|
|
|
|
рассчитывают степень набухания, %: |
|
V ρp |
100 |
|
|
x = |
|
|
, |
(14) |
a |
|
|||
|
|
|
|
|
где ρp – плотность растворителя; а – навеска полимера, г.
Рис. 3. Прибор для определения степени набухания полимеров
Вопросы и задания
1.Какие вы знаете растворители для различных полимеров?
2.От чего зависит растворимость полимеров?
3.Какое применение находят растворы полимеров?
4.Каковы стадии растворения?
5.Как зависит растворимость полимеров от их структуры?
6.Чем отличается истинный раствор от коллоидной системы?
Лабораторная работа № 9
Определение температуры размягчения по методу “кольцо–шар”
Цель работы: освоить один из методов определения температуры размягчения.
Теоретическая часть
Определение температуры размягчения по методу «кольцо и шар» связано с расплавлением полимера до жидкого состояния. Поэтому этот метод
35
пригоден лишь для испытаний сравнительно низкомолекулярных, а также пластифицированных полимеров.
Прибор для определения температуры размягчения (Тразм) состоит из двух стаканов, входящих один в другой. Наружный стакан, заполняемый глицерином, служит термостатом. Во внутренний стакан помещают латунный штатив с двумя пластинками. Верхняя пластинка имеет отверстие для термометра и четыре кольца, на которые кладут шарик. Нижняя пластинка служит для смягчения удара при падении шарика на дно стакана.
Экспериментальная часть
Кольца помещают на металлическую пластинку, заполняют до краев гранулами полимеров и нагревают до расплавления гранул. После охлаждения избыток полимера срезают горячим ножом и, установив на эту поверхность шарики, переносят кольца на пластинку.
Штатив помещают в стакан и нагревают глицериновую баню со скоростью 1 оС в минуту. По термометру отмечают температуру, при которой шарик, провисая в слое полимера, коснется поверхности нижней пластинки.
Вопросы и задания
1.Что такое теплостойкость и термостойкость полимеров?
2.Какие типы термомеханических кривых возможны для: а) низкомолеку-
лярного соединения; б) олигомеров; в) кристаллического полимера; г) аморфного полимера?
3.Что такое температура стеклования, температура текучести, температура размягчения?
4.Какие физические состояния характерны для аморфного полимера?
5.Что такое гибкость полимерной цепи? Чем она обусловлена?
6.Расположите следующие полимеры в ряд с увеличением гибкости: целлюлозы; белки; полистирол; полиэтилен; поливинилхлорид; полиакриловая кислота.