Материал: 2018_02_15_01
Задача 8.1
Дано: водный раствор HCN.
Используя данные о свойствах растворов HCN в воде (табл.8.1):
1)постройте графики зависимости удельной и эквивалентной электрических проводимостей растворов HCN от разведения V;
2)проверьте, подчиняются ли растворы HCN в воде закону разведения Оствальда;
3)вычислите для растворов HCN по данным зависимости эквивалентной электрической проводимости от концентрации эквивалентную электрическую проводимость при бесконечном разведении и сопоставьте результат со справочными данными.
Решение задачи 8.1
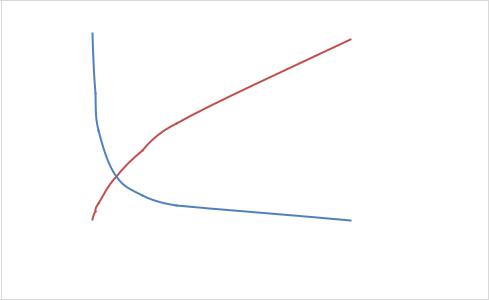
Строим график зависимости удельной и эквивалентной электрических проводимостей растворов HCN от разведения V. Из графика следует, что удельная электропроводность падает с разведением,
а эквивалентная электропроводность – растет.
|
|
|
|
|
Таблица 8.1 |
|
Характеристики раствора HCN в воде |
|
|||
|
|
|
|
|
|
№ |
Концен- |
Разве- |
r∙10-3, |
æ∙104, |
λ∙103, |
п/п |
трация, С, |
дение, V, |
Ом∙м |
См∙м-1 |
См∙см2∙моль-1 |
|
моль/л |
л/моль |
|
|
|
|
|
|
|
|
|
1 |
0,1 |
10,00 |
3,10 |
3,226 |
32,26 |
|
|
|
|
|
|
2 |
0,05 |
20,00 |
4,37 |
2,288 |
45,76 |
|
|
|
|
|
|
3 |
0,03 |
33,30 |
5,84 |
1,712 |
57,06 |
|
|
|
|
|
|
4 |
0,01 |
100,00 |
10,10 |
0,990 |
99,00 |
|
|
|
|
|
|
5 |
0,005 |
200,00 |
14,30 |
0,699 |
139,80 |
|
|
|
|
|
|
6 |
0,003 |
333,30 |
18,30 |
0,546 |
182,00 |
|
|
|
|
|
|
7 |
0,001 |
100,00 |
31,90 |
0,313 |
313,00 |
|
|
|
|
|
|
51
106, Ом-1 м2 моль-1
350
300
250
200
150
100
50
0
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3,5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2,5 |
Ом |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
,æ1− |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1,5 |
м |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1− |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
200 |
400 |
600 |
800 |
1000 |
1200 |
|
||||||||
V, л/моль
Рис. 8.1. Зависимость удельной и эквивалентной электропроводности от разведения V
Согласно закону разведения Оствальда (8.1) для очень слабых электролитов Кдисс= α2∙С, где α – степень диссоциации раствора электролита; α = λс /λ∞, где λс – эквивалентная электропроводность при концентрации С; λ∞ - эквивалентная электропроводность при бесконечном разведении.
Если растворы HCN подчиняются закону Оствальда, зависимость lg λ должна быть линейной функцией lg С. Для построения графика зависимости lg λ от lg С (рис 8.2) рассчитываем логарифмы λ и
концентрации С (табл. 8.2).
|
|
|
|
Таблица 8.2 |
|
|
К определению значений λ∞ |
|
|
||
|
|
|
|
|
|
№п/п |
С, |
|
- lg C |
-lg λ |
|
|
(моль/м3)∙103 |
|
|
|
|
1 |
0,1 |
|
4,000 |
1,4949 |
|
|
|
|
|
|
|
2 |
0,05 |
|
4,301 |
1,3395 |
|
|
|
|
|
|
|
3 |
0,03 |
|
4,523 |
1,2436 |
|
|
|
|
|
|
|
4 |
0,01 |
|
5,000 |
1,0044 |
|
|
|
|
|
|
|
5 |
0,005 |
|
5,301 |
0,8545 |
|
|
|
|
|
|
|
6 |
0,003 |
|
5,523 |
0,7399 |
|
|
|
|
|
|
|
7 |
0,001 |
|
6,000 |
0,5045 |
|
|
|
|
|
|
|
|
|
52 |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
1,8 |
|
|
|
|
|
|
|
|
1,6 |
|
|
|
|
|
|
|
|
1,4 |
|
|
|
|
|
|
|
l |
1,2 |
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
0,8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,6 |
|
|
|
|
|
|
|
|
0,4 |
|
|
|
|
|
|
|
|
0,2 |
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
3 |
3,5 |
4 |
4,5 |
5 |
5,5 |
6 |
6,5 |
|
|
|
|
|
-lg |
|
|
|
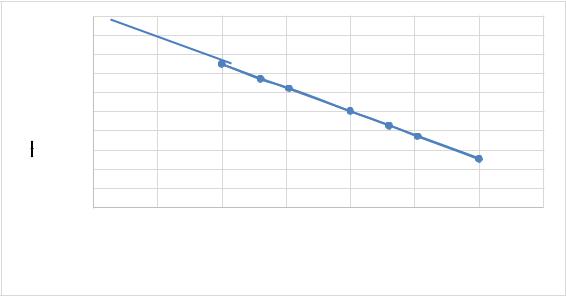
Рис. 8.2. Зависимость lg λ от lg С
На рис. 8.2 видно, что зависимость lg λ от lg С является прямолинейной, значит, раствор HCN подчиняется закону Оствальда, и
HCN является слабым электролитом.
Доказательство подчинения поведения водных растворов HCN
закону Оствальда можно получить также расчетом значений Кдисс при различных концентрациях раствора по формуле: Кдисс = α2С = (λс /λ∞)2∙С.
Значение λ∞ берем из справочника. Если получаются постоянные значения Кдисс, то это означает, что HCN является слабым электролитом.
Таблица 8.3
Результаты расчета константы диссоциации HCN
№ п/п |
С, моль/л |
|
λ, См∙см2∙моль-1 |
Кдисс.∙1010 |
|
|
|
|
|
1 |
0,1 |
|
0,03226 |
5,60 |
|
|
|
|
|
2 |
0,05 |
|
0,04576 |
5,70 |
|
|
|
|
|
3 |
0,03 |
|
0,05706 |
5,34 |
|
|
|
|
|
4 |
0,01 |
|
0,0990 |
5,35 |
|
|
|
|
|
5 |
0,005 |
|
0,1398 |
5,34 |
|
|
|
|
|
6 |
0,003 |
|
0,1820 |
5,42 |
|
|
|
|
|
7 |
0,001 |
|
0,3130 |
5,35 |
|
|
|
|
|
|
|
53 |
|
|
Из данных табл. 8.3 видно, что значение Кдисс.(HCN) не зависят от концентрации раствора, значит, во-первых, HCN является слабым электролитом, во-вторых, свойства раствора подчиняются закону разбавления Оствальда.
Из полученного по уравнению (8.3) графика (рис.8.2) находим отрезок на оси ординат, равный const: const = lg λ∞ + 1/2 lg K и
определяем λ∞. Const = -1,94.
Расчет: const = -1,94 = lg λ∞ + 1/2 lg K. Кдисс(HCN) = 7,2∙10-10. 1/2 lg Kдисс = 1/2 lg 7,2∙10-10= 1/2(-10) 0,8573 = - 4,2865.
lg λ∞ = -1,65 + 4,2865 = 2,636. λ∞ = 433,5 См∙см2∙моль-1.
Табличные данные: λ∞ (HCN) = λ∞ (Н+) + λ∞(CN-) = 349,8 + 78,0 = 427,8 См∙см2∙моль-1.
Задача 8.2
Рассчитайте эквивалентную электрическую проводимость λ∞ BaCI2
при 298 К, если эквивалентные электрические проводимости при бесконечном разведении для растворов SrCI2, Ba(NO3)2, Sr(NO3)2 равны
0.0136, 0.0132, 0.01318 См∙м2∙моль-1, соответственно.
Решение задачи 8.2
Составляем систему уравнений согласно (8.7):
1)1/2λ∞[Ba(NO3)2]= 1/2λ∞(Ba2+) + λ∞( NO3-) = 0,0132,
2)1/2λ∞[(SrCI2)] = 1/2λ∞(Sr2+) + λ∞(CI-) = 0,0136,
3)1/2λ∞[Sr(NO3)2] = 1/2λ∞(Sr2+) + λ∞( NO3-) = 0,01318.
Складываем уравнения (1) и (2), вычитаем из них уравнение (3): 1/2λ∞(Ba2+) + λ∞( NO3-) + 1/2λ∞(Sr2+) + λ∞(CI-) -1/2 λ∞(Sr2+) - λ∞( NO3-) = 1/2λ∞(Ba2+) + λ∞(CI-) = 1/2λ∞(BaCI2) = 0.01320 + 0.0136 – 0.01318 =
= 0.01362 См∙м2∙моль-1.
54

Задача 8.3
Удельное сопротивление насыщенного раствора труднорастворимой соли А при 298 К равно r. Удельное сопротивление воды при той же температуре rН2О = 1 · 104 Ом · м. Вычислите:
1)растворимость соли А в чистой воде;
2)произведение растворимости вещества А, приняв, что коэффициенты активности ионов γ± = 1 (растворы сильно разбавлены);
3)растворимость вещества А в растворе, содержащем 0.01 моль вещества В; 4) растворимость вещества А в растворе, содержащем 0.01 моль вещества С. Вещества А, В, С полностью диссоциированы.
|
|
|
|
Таблица 8.4 |
|
Исходные данные для решения задачи 8.3 |
|
|
|||
|
|
|
|
|
|
r · 10-4, Ом·м |
|
Вещество |
|
|
|
|
|
|
|
|
|
А |
В |
|
С |
|
|
|
|
|
|||
|
|
|
|
|
|
0.0248 |
PbSO4 |
Li2SO4 |
|
KBr |
|
|
|
|
|
|
|
Решение задачи 8.3
1. Рассчитаем удельную проводимость насыщенного раствора
PbSO4:
æ = |
1 |
− |
|
1 |
|
= |
1 |
|
− |
1 |
|
= 3,93 · 10−3 |
См |
. |
|
|
|
|
248 |
10000 |
|
||||||||
|
|
|
|
|
|
м |
||||||||
|
|
|
н |
|
|
|
|
|
|
|
|
|||
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
По определению, |
|
эквивалентная |
электрическая проводимость |
|||||||||||
λ равна отношению удельной проводимости к нормальной концентрации растворенного вещества С:
æ
λ = .
Отсюда следует, что
= æλ .
Будем считать, что в нашем случае эквивалентная проводимость равна предельной эквивалентной проводимости. Тогда эквивалентная
55