Материал: 2018_02_15_01
|
87 |
|
|
|
|
|
|
|
|
|
P∞*106, |
86 |
|
|
|
|
|
|
|
|
|
м3/моль 85 |
|
|
|
|
|
|
|
|
|
|
|
84 |
|
|
|
|
|
|
|
|
|
|
83 |
|
|
|
|
|
|
|
|
|
|
82 |
|
|
|
|
|
|
|
|
|
|
81 |
|
|
|
|
|
|
|
|
|
|
80 |
|
|
|
|
|
|
|
Y |
|
|
79 |
|
|
|
|
|
|
|
|
|
|
78 |
|
|
|
|
|
|
|
|
|
|
77 |
|
|
|
|
|
|
|
|
|
|
76 |
|
|
|
X |
|
|
|
|
|
|
3,25 |
3,3 |
3,35 |
3,4 |
3,45 |
3,5 |
3,55 |
3,6 |
3,65 |
3,7 |
|
|
|
|
|
1/T*103 |
|
|
|
|
|
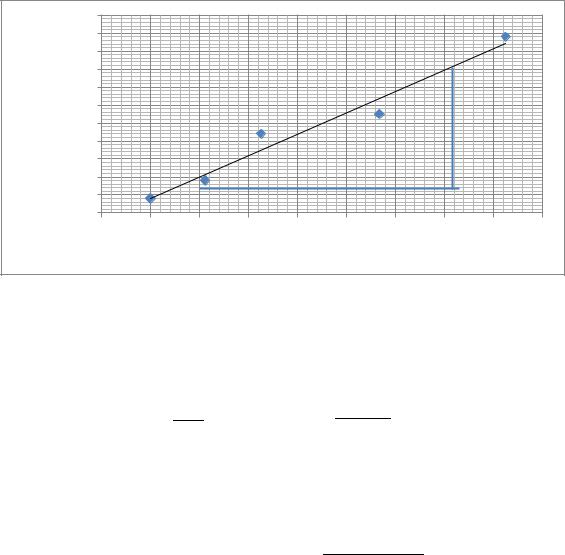
Рис. 7.1. Зависимость полярной рефракции от 1/Т |
|
|
|
|||||||
Для вычисления дипольного момента воспользуемся следующей формулой:
= 4,27 ∙ 10−29√ = 4,27 ∙ 10−29√0,0235 = 6,55 ∙ 10−30 Кл ∙ м.
б) Дипольный момент также можно рассчитать с помощью молекулярной рефракции:
= 4,27 · 10−29 · √( − ) · ,
где RM - молекулярная рефракция;
T – температура;
P – поляризация при температуре T.
|
Вычислим молекулярную рефракцию при 20 0С: |
|
|
||||||||||
|
= |
2 |
− 1 |
∙ |
|
= |
1,352722 |
− 1 |
∙ |
112,56 ∙ 10−3 |
= 3,447 ∙ 10−5 |
м3 |
, |
|
|
|
|
|
|
|
|||||||
|
|
2 |
+ 2 |
|
|
1,352722 |
+ 2 |
|
0,70760 ∙ 103 |
моль |
|
||
|
|
|
|
|
|||||||||
где n – коэффициент преломления вещества;
M – молярная масса;
ρ – плотность.
46

Рассчитаем дипольный момент:
= 4,27 · 10−29 · √( − ) · =
=4,27 · 10−29 · √(55,0 · 10−6 − 3,447 · 10−5) · 293 =
=5,409 · 10−30 Кл · м.
Полученные результаты различаются. Разница составляет:
5,409 · 10−30= (1 − 6,55 · 10−30 ) · 100 = 17,42 %
Различие можно объяснить явным разбросом исходных экспериментальных данных. Помимо этого, различие результатов можно объяснить тем, что в расчетах мы пренебрегли атомной поляризацией.
Задача 7.2
При 293 К плотность а-% раствора вещества А в растворителе В равна ρ, показатель преломления раствора равен n.
Вычислить молярную рефракцию вещества А, если при 293 К
плотность растворителя равна ρ0 , а его показатели преломления n0.
Решение задачи 7.2
|
|
|
|
|
Таблица 7.2 |
|
|
Исходные данные для решения задачи 7.2 |
|
|
|||
|
|
|
|
|
|
|
а, % |
А |
В |
ρ·10-3, кг/м3 |
|
n |
|
|
|
|
|
|
|
|
90 |
С2Н4Br2 |
C8H7OH |
1,866 |
|
1,503 |
|
|
|
|
|
|
|
|
Молярная рефракция раствора R вычисляется следующим образом:
= 2 4 2 · 2 4 2 + 3 7 · 3 7 = = 2 4 2 · 2 4 2 + 3 7 · (1 − 2 4 2),
где R - молярные рефракции веществ;
x - молярные доли веществ в растворе.
Отсюда мы можем рассчитать молярную рефракцию 2 4 2:
|
= |
− |
|
· (1 − |
) |
|
3 7 |
|
2 4 2 . |
||||
2 4 2 |
|
|
|
|
|
|
|
|
|
2 4 2 |
|
|
|
|
|
|
47 |
|
|
|

Для расчетов нам нужна молярная доля 2 4 2 в растворе:
|
|
|
|
|
|
|
|
2 4 |
2 |
|
|
|
|
|
|
90 |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
187,9 |
|
||||||
|
2 |
= |
|
|
|
|
|
2 4 |
|
|
= |
|
|
|
= 0,7422, |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
2 4 |
|
|
|
|
100 − |
|
|
|
90 |
|
+ |
100 − 90 |
|
|||||||||
|
|
|
|
|
2 4 |
2 |
|
+ |
|
|
|
2 4 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
187,9 |
|
60,1 |
|
|||||||
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
2 4 |
|
|
3 7 |
|
|
|
|
|
|
|
|
|
|
|||||
где 2 4 2 – процентная массовая концентрация 2 4 2 в растворе;
М - молярные массы веществ.
Теперь нам надо рассчитать молярную рефракцию раствора:
= |
2 |
− 1 |
· |
|
, |
2 |
+ 2 |
|
где n – коэффициент преломления;
M – молярная масса раствора; ρ – плотность раствора.
Найдем среднюю молярную массу смеси:
= 2 4 2 · 2 4 2 + 3 7 · (1 − 2 4 2) = = 187,9 · 0,7422 + 60,1 · (1 − 0,7422) = 155, 0 мольг .
Молярная рефракция раствора
|
1,5032 |
− 1 |
|
155,0 · 10−3 |
= 2,456 · 10−5 |
м3 |
|
= |
|
|
· |
|
|
. |
|
1,5032 + 2 |
1,866 · 103 |
|
|||||
|
|
|
моль |
||||
Таблица 7.3
Исходные данные для различных растворителей
B |
d ·10-3, кг/м3 |
n0 |
B |
P0, кг\м3 |
n0 |
|
|
|
|
|
|
H2O |
1,000 |
1,333 |
CSNC3H5 |
1,019 |
1,530 |
|
|
|
|
|
|
CH3OH |
0,805 |
1,329 |
C5H10NH |
0,863 |
1,461 |
|
|
|
|
|
|
C2H5OH |
0,808 |
1,364 |
C6H6 |
0,885 |
1,504 |
|
|
|
|
|
|
CH3COOC2H5 |
0,903 |
1,375 |
C6H5CH3 |
0,867 |
1,447 |
|
|
|
|
|
|
CH3CH2CH2OH |
0,807 |
1,386 |
C6H4(CH3)2 |
0,881 |
1,505 |
|
|
|
|
|
|
|
|
48 |
|
|
|
Рассчитаем молярную рефракцию пропилового спирта:
|
|
|
2 − 1 |
|
|
|
|
|
1,3862 − 1 |
|
60,1 · 10−3 |
|
||
|
|
= |
|
· |
3 7 |
= |
|
|
|
· |
|
= |
||
|
2 + 2 |
|
|
1,3862 |
+ 2 |
0,807 · 103 |
||||||||
3 7 |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
3 7 |
|
|
|
|
|
|
|
|
|
|
|
|
= 1,749 · 10−5 |
|
м3 |
|
|
|
|
|||||
|
|
|
|
|
|
, |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
моль |
|
|
|
|
||
где n – показатель преломления пропилового спирта;
3 7 – плотность пропилового спирта.
Теперь мы можем рассчитать молярную рефракцию 2 4 2:
|
|
= |
− |
|
· (1 − |
|
4 2 |
) |
|
|
|||
|
|
3 7 |
|
2 |
|
|
|
|
|||||
2 |
4 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 4 2 |
|
|
|
|
|
|
||
|
|
|
= |
2,456 · 10−5 − 1,749 · 10−5 · (1 − 0,7422) |
= |
||||||||
|
|
|
|
|
|
0,7422 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
= 2,702 · 10−5 |
м3 |
. |
|
|
|
|
|
|||
|
|
|
моль |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ТЕМА 8. ЭЛЕКТРИЧЕСКАЯ ПРОВОДИМОСТЬ. РАВНОВЕСИЕ
В РАСТВОРАХ ЭЛЕКТРОЛИТОВ
Зависимость между λ и концентрацией раствора может быть
установлена с помощью закона разбавления Оствальда:
К = α2С/(1 – α), |
(8.1) |
где К - константа диссоциации электролита; |
|
α - степень диссоциации электролита; |
|
С - концентрация электролита. |
|
Поскольку λ = λ∞∙α, и для очень слабых электролитов можно |
|
пренебречь знаменателем в (8.1), получим: λ = λ∞. |
В логарифмической |
форме эта зависимость имеет вид: |
|
ln λ = ln λ∞ + 1/2 ln K – 1/2 ln С . |
(8.2) |
49 |
|

Величины К и λ∞ являются постоянными, следовательно, ln λ –
линейная функция ln С. Уравнение (8.2) в виде: |
|
lg λ = const – lg С |
(8.3) |
хорошо выполняется для электролитов с Кдисс ≤ 10-5. Отрезок оси
ординаты (const) на графике зависимости lg |
λ = f(lg С ): |
|
|
const = lg |
λ∞ + 1/2 lg K |
(8.4) |
|
Отсюда определяем λ∞ для слабых электролитов с Кдисс ≤ 10-5. |
|||
Для электролитов с Кдисс˃ 10-5 приложимо уравнение, основанное на |
|||
зависимости (7.1), где α замещено на λ/λ∞: |
|
|
|
1/λ – 1/ λ∞ = λ∙С/(λ∞2∙К). |
|
(8.5) |
|
откуда 1 – (λ/λ∞) = λ2 ∙ С/(λ∞2∙К). Разделив все на λ, получим: |
|
||
1/λ – 1/ λ∞ = λ∙С/(λ∞2∙К). |
|
(8.6) |
|
В формуле (8.6) λ∞2∙К и |
1/λ∞ |
- величины |
постоянные. |
Следовательно, в координатах 1/λ = f(λ∙С) эта зависимость будет уравнением прямой. Угловой коэффициент (tg α) будет равен 1/(λ∞2∙К).
Отсюда определяем λ∞ для слабых электролитов с Кдисс˃ 10-5.
Для сильных электролитов, которые хорошо диссоциированы в растворах, уравнения (8.2) и (8.6) не выполняются; для них зависимость λ
от С подчинена эмпирическому уравнению Кольрауша: λ = λ∞ - В√С.
Согласно эмпирическому закону Кольрауша о независимости движения ионов в растворах электролита при бесконечном разведении для сильных и слабых электролитов λ∞ равна сумме электрических
проводимостей (подвижностей) катиона и аниона: |
|
λ∞ = λ∞+ + λ∞- . |
(8.7) |
Связь между эквивалентной и удельной электропроводностями |
|
растворов электролитов выражается соотношением: |
|
λ = æ/ С, См∙м2∙моль-1= 1000 ∙ æ/ С, См∙см2∙моль-1. |
(8.8) |
50