Материал: 1547
где знак минус означает, что электрон находится в связанном состоянии. Из формулы следует, что энергетические состояния атома образуют последовательность энергетических уровней, изменяющихся в зависимости от значения п. Целое число п в выражении (1), определяющее энергетические уровни атома, называется главным квантовым числом. Энергетическое состояние с п = 1 является основным (нормальным) состоянием; состояния с п > 1
являются возбужденными.
Энергетический уровень, соответствующий основному состоянию атома, называется основным (нормальным) уровнем; все остальные уровни являются возбужденными. Придавая п различные целочисленные значения, получим для атома водорода (Z = 1), согласно формуле (1), возможные уровни энергии, схематически представленные на рис.1. Энергия атома водорода с увеличением п возрастает, и энергетические уровни сближаются к границе, соответствующей значению п = ∞. Атом водорода обладает, таким образом, минимальной энергией (E0 = -13,55 эВ) при п = 1 и максимальной (Е = 0) при п = ∞. Согласно второму постулату Бора, при переходе атома водорода (Z = 1) из стационарного состояния п в стационарное состояние т с меньшей
hv En Em |
|
me4 |
|
1 |
1 |
|
|||||
|
|
|
|
( |
|
|
|
|
), |
||
8h |
2 0 |
2 |
n |
2 |
m2 |
||||||
откуда частота излучения |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
v |
me4 |
( |
1 |
|
1 |
) R( |
1 |
|
1 |
), |
|||||
|
|
|
2 |
|
2 |
|
2 |
|
2 |
|
2 |
||||||
|
|
3 |
|
m |
|
n |
|
m |
|
n |
|
||||||
|
me4 |
|
8h |
0 |
|
|
|
|
|
|
|
|
|
||||
где R |
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8h3 02 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Воспользовавшись при вычислении R современными значениями универсальных постоянных, получим величину, совпадающую с экспериментальным значением постоянной Ридберга в эмпирических формулах для атома водорода. Это совпадение убедительно доказывает правильность полученной Бором формулы для энергетических уровней водородоподобной системы. Подставляя, например, в формулу т = 1 и п = 2, 3, 4, ... , получим группу линий, образующих серию Лаймана и соответствующих переходам электронов с возбужденных уровней (п = 2, 3, 4, ...) на основной
(т = 1).
60
Аналогично, при подстановке т = 2,3,4,5,6 и соответствующих им значений п получим серии Бальмера, Пашена, Брэкета, Пфунда и Хэмфри (часть из них схематически представлена на рис. 1). Следовательно, по теории Бора, количественно объяснившей спектр атома водорода, спектральные серии соответствуют излучению, возникающему в результате перехода атома в данное состояние из возбужденных состояний, расположенных выше данного.
Задание к лабораторной работе
Упражнение 1. Определение зависимости радиуса орбиты, скорости и энергии электрона на орбите от номера орбиты
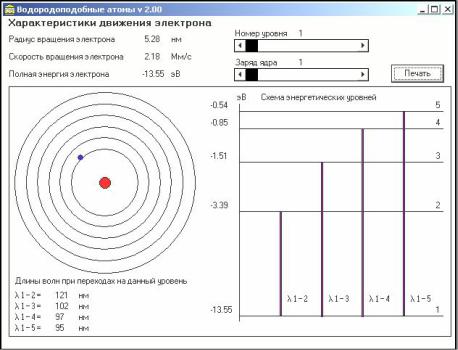
1. Задавая различные номера орбит, определите с помощью программы значения радиуса орбиты, скорости и энергии электрона для атома водорода и одного из ионизированных атомов (рис.2). Занесите данные в табл. 1 и 2.
Рис.2. Рабочее окно программы
2.Постройте графики зависимостей r,υ и Е от номера уровней.
3.Сделайте выводы:
а) Как зависят эти величины от номера уровня? В каких координатах «спрямляются» эти зависимости?
61
б) Как влияет заряд ядра на величину и поведение этих характеристик электрона?
|
|
Результаты измерений |
Таблица 1 |
|
|
|
|
|
|
|
|
|
|
Атом водорода |
|
n |
r, м |
υ, м/с |
E, эВ |
1 |
|
|
|
2 |
|
|
|
3 |
|
|
|
4 |
|
|
|
5 |
|
|
|
6 |
|
|
|
|
|
Результаты измерений |
Таблица 2 |
|
|
|
|
|
|
|
|
|
|
Ион Z = |
|
n |
r, м |
υ, м/с |
E, эВ |
1 |
|
|
|
2 |
|
|
|
3 |
|
|
|
4 |
|
|
|
5 |
|
|
|
6 |
|
|
|
Упражнение 2. Изучение спектра одноэлектронных атомов. Определение постоянной Ридберга
1. Определите с помощью программы длины волн фотонов, которые испускаются атомом при переходе электрона с вышележащих орбит на п–ю. Занесите данные в табл. 3 и 4.
Таблица 3
Результаты измерений
Атом водорода H
n |
λ 1 |
λ 2 |
λ 3 |
λ 4 |
1
2
3
4
62
Таблица 4
Результаты измерений
Атом водорода He+
n |
λ 1 |
λ 2 |
λ 3 |
λ 4 |
1
2
3
4
Таблица 5
Результаты измерений
Атом водорода Li++
n |
λ 1 |
λ 2 |
λ 3 |
λ 4 |
1
2
3
4
2.Зарисуйте схематично спектр атома водорода, а также ионизированных атомов гелия и лития.
3.Из табл. 3–5 выберите несколько спектральных линий. Используя формулу
|
|
R |
|
|
1 |
|
|
|
|
, |
|
||
|
|
Z |
2 |
1 |
1 |
|
|
||||||
|
|
|
|
|
( |
|
|
|
) |
|
|
||
|
|
|
n2 |
m2 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
определите постоянную Ридберга. Заполните табл. 6. |
|
||||||||||||
|
|
Результаты измерений |
Таблица 6 |
||||||||||
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||
|
Z |
n |
|
m |
|
|
|
|
R', м-1 |
R'ср, м-1 |
|||
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4. Сделайте вывод о зависимости вида спектра от заряда ядра. Найдите по табл. 3–5 участки видимого спектра для каждого атома. Сравните вычисленное значение постоянной Ридберга с табличным.
63
ЛАБОРАТОРНАЯ РАБОТА № 8
Радиоактивность
Цели работы: изучить закон радиоактивного распада, определить период полураспада элемента с помощью моделирующей программы. Исследовать радиоактивное семейство 238U.
Основы теории
Явление радиоактивности было обнаружено Беккерелем в 1896 г. Оно заключается в том, что ядра некоторых изотопов способны самопроизвольно, без всякого внешнего воздействия, распадаться, испуская лучи, способные проходить сквозь непрозрачные для видимого света вещества. Исследованиями Пьера и Марии Кюри, Содди и др. было установлено, что не только уран и его изотопы, но и изотопы всех элементов, расположенных в таблице Менделеева за висмутом (Z = 83), радиоактивны.
Радиоактивное излучение бывает трех типов: α - лучи, β - лучи и
γ- лучи.
а- лучи представляют поток ядер гелиевых атомов с зарядовым числом Z = 2 и массовым числом А = 4. α - излучению соответствует α - распад, в ходе которого из ядра вырывается α - частица, в результате чего материнское ядро превращается в дочернее. Последнее имеет зарядовое число на 2, а массовое на 4 единицы меньше материнского. Зная это правило смещения для а - распада,
легко записать уравнение распада любого изотопа:
AX A 4Y 4He |
(1) |
Z Z 2 2 |
|
β - лучи оказались потоком отрицательно заряженных частиц – электронов, имеющих высокую энергию; β - излучение соответствует β - распаду, в котором материнское ядро превращается в дочернее без изменения массового числа, но с увеличением зарядового числа на единицу. Это правило смещения β - распада позволяет записать уравнение распада любого изотопа:
AX |
AY 0e |
(2) |
|
Z |
Z 1 |
1 |
|
Впоследствии оказалось, что β - распад сопровождается испусканием еще одной частицы – антинейтрино, а помимо β - распада существует β+ - распад, который сопровождается испусканием позитрона (античастицы по отношению к электрону) и
64