Материал: Введение в нанотехнологии (Рыбалкина), c.87
Итак, принципиальное свойство света – его двойственная природа, или корпускулярно-волновой дуализм. С одной стороны, свет – это совокупность электромагнитных волн разной частоты, с другой – это поток частиц (квантов, фотонов). Чтобы увидеть ту или другую сторону природы света, нужно поставить соответствующие опыты. Например, если мы поставим опыты по интерференции или дифракции света, то убедимся, что свет – это волновой процесс. Если же экспериментально изучаем законы фотоэффекта, то убедимся, что свет – это поток фотонов. Разрешение этого противоречия как раз и привело к становлению и развитию квантовой механики.
Структура атома
С точки зрения классических законов физики непонятна устойчивость атома и линейчатый характер атомных спектров. К началу XX века эмпирическим путем было установлено, что электроны представляют собой отрицательно заряженные частицы, являющиеся составной частью атома. Электрический ток является ничем иным, как упорядоченным движением электронов вдоль металлического провода, и в этом смысле электрон есть квант электричества.
Модель атома Резерфорда
Исходя из такой информации, Э. Резерфорд предложил в 1910 г планетарную модель атома,
согласно которой отрицательно заряженные электроны вращаются как планеты вокруг центрального положительно заряженного ядра, которое притягивает их подобно Солнцу (напомним, что заряды одинаковых знаков отталкиваются, а противоположных -
притягиваются). Такая аналогия между атомом и Солнечной системы сразу же захватила воображение большинства людей. Она действительно позволяет очень наглядно создать зрительный образ атома и объяснить некоторые его свойства, например различия в величине зарядов электронов.
Однако пользоваться данной аналогией можно только до определенного предела. Основной недостаток этой модели следует из природы электрических зарядов. Если на заряд действует магнитное поле или силы притяжения какогонибудь атомного ядра, то заряд не может двигаться равномерно и прямолинейно. Его траектория будет искривлена, а из теории Максвелла следует, что такой заряд при движении должен испускать электромагнитные волны, теряя при этом часть своей энергии.
Таким образом, по законам классической физики неизбежно следовал вывод, что, двигаясь ускоренно по определенным орбитам, электрон, излучающий энергию в виде электромагнитных волн, со временем должен терять скорость и, в конце концов, упасть на ядро (что положило бы конец существованию атома).
Время падения электрона порядка 10-9с, что, конечно же, противоречит стабильности атома в действительности.
Кроме того, совокупность таких атомов должна была бы давать сплошной спектр излучения, а не линейчатый, наблюдаемый на опыте.
Постулаты Бора и квантование орбит
Успех в устранении изложенных выше противоречий был достигнут Н. Бором в 1913 г., когда он распространил идеи Планка и Эйнштейна о квантовых свойствах электромагнитного излучения на атомы вещества. Бор ограничился рассмотрением атома водорода, так как он очень прост (единственный электрон вращается вокруг одного протона) и поддается математическому анализу.
Изучая линейчатый спектр атома, Бор понял, что существуют очень простые правила, управляющие излучением световых волн атомами вещества, которые хорошо объясняют множество существующих электронных орбит. Свои выводы он сформулировал в виде известных постулатов - постулатов Бора.
Первый постулат Бора (постулат стационарных состояний) гласит: электроны в отдельном атоме могут обладать лишь определенными (разрешенными) значениями энергии, или, другими словами, находится на определенных энергетических уровнях. Уровни энергии образуют дискретный энергетический спектр атома (см. рис).
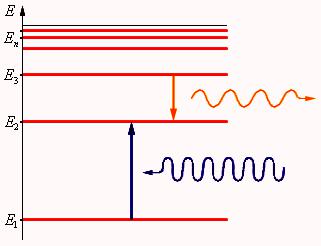
Рис 2. Энергетическая схема атомных уровней Энергия Е1 соответствует основному состоянию, Е2 – возбужденному.
Второй постулат Бора (правило частот): при определенных условиях электроны могут переходить с одного уровня на другой (или с одной орбиты на другую), поглощая или испуская световой фотон.
Существует орбита с наименьшей возможной энергией, на которой электрон может находится неограниченно долго – это его основное состояние. При переходе с одного энергетического уровня на другой, электрон возбуждается,

но при каждом удобном случае всегда стремиться вернуться из возбужденного состояния обратно в основное.
Каким же образом происходит переход электрона с одного уровня на другой? Предположим, атом находится в состоянии n и обладает энергией En . Чтобы вынудить электрон перейти на уровень m, мы должны каким-то образом "выбить" его из основного состояния, придав ему некоторую дополнительную энергию. Для этого мы будем "обстреливать" электрон световыми фотонами различной частоты. Напоминаем, что энергия фотона зависит от частоты излучения, поэтому энергия одного кванта света равна
Е = h ν
где ν – частота
h –постоянная Планка,
Оказывается, не каждый фотон способен вынудить атом перейти в возбужденное состояние, а лишь тот, чья энергия в точности равна разности энергий возбужденного и основного состояний электрона в атоме, то есть:
hν = Em − En
При этом электрон поглотив световой фотон, перейдет на уровень, соответствующий энергии Еm.
Если же энергия фотона окажется больше либо меньше необходимой, то он "пролетит" сквозь атом, никоим образом не повлияв на состояние электрона.
Итак, электрон находится в возбужденном состоянии, из которого он в силу своей природы стремиться вернуться обратно на "родной" уровень. Для этого ему нужно "освободиться" от энергии, полученной от фотона. Поэтому, обратный переход сопровождается испусканием светового фотона абсолютно той же частоты, то есть:
En = Em −hν
Таким образом, квантовая механика обнаружила то, что атом обладает способностью поглощать и испускать фотоны света, что в дальнейшем послужило основой для создания различного рода технических устройств, использующих этот принцип (например, лазеров).
Итак, сформулируем важный вывод из теории квантовой механики:
Физические величины в квантовом мира изменяются дискретно.
Принцип запрета Паули – один из главнейших квантомеханических принципов – гласит, что на каждом энергетическом уровне атома в данном состоянии может находиться только один электрон, при этом, чем выше уровень электрона, тем большая энергия ему соответствует. Электрон с данной энергией может двигаться только по замкнутой орбите вокруг ядра.
Строго говоря, орбита в квантовой механике понятие довольно условное. Из-за несовершенства современной аппаратуры и ввиду невозможности четко зафиксировать положение электрона в атоме, можно лишь приближенно говорить о некоторой "размытой" орбите электрона, а ее замкнутость означает только то, что "в среднем" электрон находится на определенном расстоянии от ядра.
–
– +
Рис 3. Условная схема атома водорода
Следует отметить, что и квантование энергии атома, и требование стационарности орбит связано с постоянной Планка. Отсюда делаем вывод:
Постоянная Планка и связанное с ней понятие элементарного кванта
Волновая функция
действия играют в квантовой физике фундаментальную роль при описании поведения микрообъектов.
Принцип работы лазера.
Лазер (оптический квантовый генератор) – это замечательный пример практического применения умения электронов поглощать и излучать световые кванты. Это источник света, свойства которого резко отличаются от всех других источников (ламп накаливания, люминесцентных ламп, свечи и т.д.).
В настоящее время созданы лазеры, генерирующие излучение в инфракрасном, видимом и ультрафиолетовом диапазоне длин волн. За создание лазеров советские физики Н.Г. Басов и А. М. Прохоров вместе с американским физиком Чарльзом Таунсом в 1964 году получили Нобелевскую премию по физике.
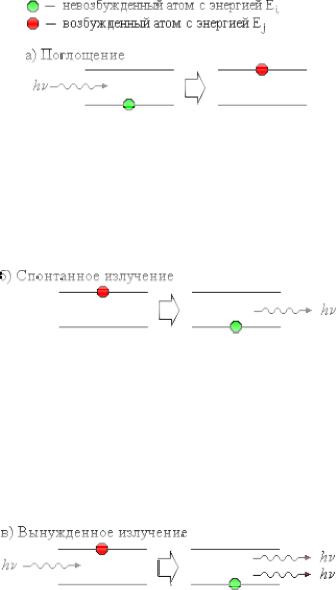
Рассмотрим вкратце принцип работы простейшего лазера. Мы выяснили, что при переходе атома из основного состояния, которому соответствует более низкий энергетический уровень в возбужденное (где энергия, соответственно, выше), происходит поглощение фотона веществом (рис а).
Из возбужденного состояния электрон всегда стремиться вернуться в основное, поэтому время его пребывания в таком состоянии чрезвычайно мало – 10-8 с. Переход электрона на более низкий энергетический уровень сопровождается излучением кванта света. Такое самопроизвольное излучение принято называть спонтанным (рис б).
Однако существует и другой вид излучения, открытый А. Эйнштейном и называемый вынужденным, или индуцированным, или стимулированным.
Индуцированное излучение происходит тогда, когда электрон, находящийся в возбужденном состоянии подвергается действию внешнего электромагнитного излучения. При этом электрон переходит на более низкий энергетический уровень, испуская фотон, когерентный (идентичный по энергии и направлению) фотону, спровоцировавшему данный переход (рис в).
Таким образом, при индуцированном излучении мы уже имеем два
абсолютно идентичных (когерентных) фотона, |
двигающихся в одном |
направлении. |
|
А теперь представить себе цепочку атомов, вытянутую в прямую линию. Если все эти атомы находятся в возбужденном состоянии, то внешний фотон, ударив в крайний атом по направлению вдоль цепочки, вызовет излучение фотона из этого атома, причем излученный фотон будет иметь такую же энергию и то же направление излучения, что и ударивший фотон. Таким образом, будут двигаться уже два одинаковых фотона. Один из этих фотонов ударит в следующий атом, который даст излучение ещё одного такого же фотона. Начинается движение уже