Материал: Влияние соединений d-металлов на скорость диссоциации молекулы воды в биполярной мембране
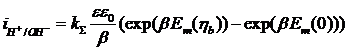 , (15)
, (15)
где kS - суммарная эффективная константа скорости реакции диссоциации воды в области пространственного заряда в отсутствии электрического поля;
Em - напряженность электрического поля на границе раздела катионо- и анионообменных слоёв,
Е0 - напряженность электрического поля при нулевом перенапряжении биполярной области;
β - энтропийный фактор;
e - относительная диэлектрическая проницаемость в области пространственного заряда;
e0 - абсолютная диэлектрическая проницаемость вакуума.
Параметры kΣ и β, входящие в уравнение (13), находили
минимизацией остаточной дисперсии экспериментальных точек относительно
расчётных точек
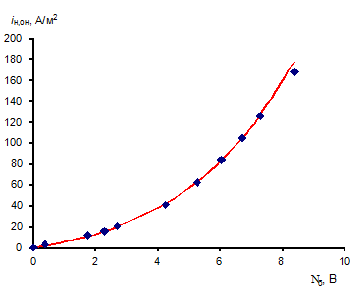
Рисунок 9 - Парциальная вольт-амперная характеристика биполярной области мембраны - аналога МБ-2 в координатах «плотность тока по ионам H+, OH-» - «перенапряжение биполярной области» и её аппроксимация (линия) с помощью уравнения
3. РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
.1 Результаты определения размеров частиц порошков гидроксидов переходных металлов
Использование разработанной в данной работе лабораторной установки для
фракционирования частиц гидроксидов позволяет выделять фракции частиц с
диаметром менее 5 мкм (рисунок 10, 11) и достаточно узкой кривой распределения
по размерам (рисунок 12).
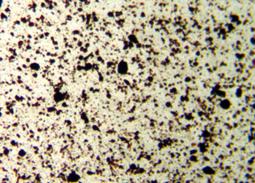
Рисунок 10 - Оптическое изображение исходной суспензии гидроксида железа
(III)
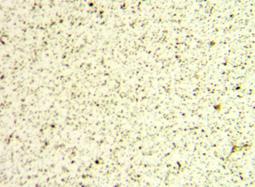
Рисунок 11 - Оптическое изображение суспензии гидроксида железа (III) с размером частиц 0-5 мкм,
полученной воздушным фракционированием исходной суспензии


а б
Рисунок 12 - Оптическое изображение суспензии гидроксида железа (III) с размером частиц 0-5 мкм,
полученной воздушным фракционированием исходной суспензии (а) и гистограмма
распределения числа частиц порошка гидроксида железа (III) по диаметрам (б)
Такие фракции гидроксидов металлов были использованы при получении модифицированных биполярных мембран.
.2 Зависимость электрохимических характеристик биполярных мембран от количества порошка гидроксида металла
Видно, что гидроксид железа (III), введенный в биполярную мембрану уменьшает сопротивление биполярной
области (рисунок 13).
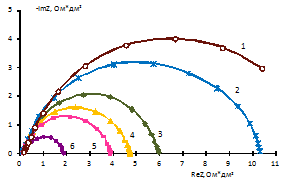
Рисунок 13 - Частотные спектры электрохимического импеданса биполярных
мембран, измеренные при плотности тока 0,22 A/дм2
- аналог МБ-2; мембраны модифицированные гидроксидом железа (III): 2-6,25 мг/дм2, 3-12,5 мг/дм2, 4-25 мг/дм2, 5-37 мг/дм2, 6-75 мг/дм2
Данные свидетельствуют об эффективности гидроксида железа (III) в качестве каталитической добавки при получении модифицированных биполярных мембран.
Импеданс мембраны, в которую внесена каталитическая добавка, изменяется
линейно в зависимости от количества введенного порошка, это подтверждается
графиком зависимости обратного сопротивления биполярной области от (рисунок 14).
Так сопротивление биполярной области мембраны при внесении гидроксида железа (III) массой 75 мг/дм2
составляет 78 Ом это в 8 раз меньше по сравнению с исходной мембраной.
Сопротивление биполярной области мембраны при внесении гидроксида железа (III) массой 37 мг/дм2
составляет 175 Ом это в 4 раз меньше по сравнению с исходной мембраной.
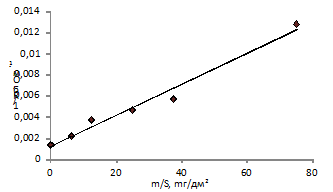
Рисунок 14 - Зависимость обратного сопротивления биполярной области от
количества введённого гидроксида железа (III)
Более наглядную информацию об электрохимических характеристиках биполярных мембран даёт перенапряжение на биполярной области и её парциальная вольтамперная характеристика.
Анализ зависимостей плотности тока от перенапряжения (рисунок 15)
показывает, что у мембран с большим количеством гидроксида железа (III)
перенапряжение меньше при одной плотности тока. Так при плотности тока 0,22 A/дм2 перенапряжение на
мембране с количеством внесённого гидроксида железа (III) 75 мг/дм2 составляет 0,25 В это в 6 раз меньше чем у
мембраны с количеством внесённого порошка гидроксида 6,25 мг/дм2,
перенапряжение на которой составляет 1,5 В.
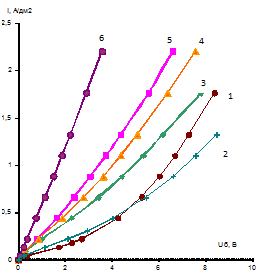
Рисунок 15 - Парциальные вольтамперные характеристики по перенапряжению
биполярной области мембраны, модифицированные разным количеством гидроксидом
железа (III)
- аналог МБ-2, мембраны с количеством гидроксида железа (III)
- 6,25 мг/дм2, 3-12,5 мг/дм2,4-25 мг/дм2, 5-37 мг/дм2,6-75 мг/дм2
.3 Влияние природы тяжёлого металла на электрохимические характеристики биполярной области мембран
Сравнение парциальных вольт-амперных характеристик биполярной области
мембран показывает (рисунок 16), что природа гидроксида, введённого в
биполярную область мембраны, слабо влияет на перенапряжение на ней. Так при
плотности тока 2,2 A/дм2 разница между перенапряжением на мембране с
гидроксидом хрома (III) и гидроксидом кобальта (III) составляет 1,21 В, в то
время как перенапряжение на исходной мембране при той же плотности тока
составляет 9,16 В.
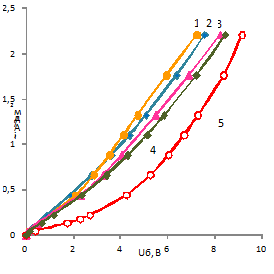
Рисунок 16 - Парциальные вольтамперные характеристики по перенапряжению
биполярных областей мембран
Мембраны, модифицированные гидроксидами d-металлов: 1 - кобольта (III), 2 - железа (III), 3 - никеля (II), 4 - хрома (III), 5 - мембрана аналог МБ-2
Таким образом, введение малорастворимых гидроксидов металлов в биполярную мембрану приводит к улучшению её электрохимических характеристик. Введение гидроксидов способствует уменьшению сопротивления биполярной области, а также снижает напряжение на мембране. Природа гидроксида влияет на характеристики мембраны незначительно, в то же время прослеживается заметное улучшение характеристик при увеличении количества введённого гидроксида.
.4 Исследование каталитической активности гидроксида железа(III) при длительном использовании модифицированной биполярной мембраны
Длительное использование для получения кислот и щелочей из солей биполярных мембран, содержащих в качестве модифицирующей добавки гидроксиды металлов, возможно в том случае, если гидроксиды металлов, находящиеся в биполярной области, не растворяются в кислой среде, которая создается в катионообменном слое биполярной мембраны, около которого находится раствор кислоты. Гидроксид железа(III) является перспективной каталитической добавкой, так как позволяет существенно снизить напряжение на биполярной мембране (рисунок 13, 15, 16), кроме того, в отличие от соединений других тяжёлых металлов, соединения железа(III) представляют наименьшую опасность для человека. Именно поэтому в данной работе была исследована устойчивость гидроксида железа(III) при длительном использовании модифицированной им биполярной мембраны в кислотно-щелочной системе.
Установлено, что в системе 0,5 М HCl - 0,5 М NaOH при плотности тока 1,1 А/дм2 сопротивление биполярной области
такой мембраны практически постоянно в течение 9 часов (рисунок 17), что
свидетельствует о стабильности гидроксида железа(III) в биполярной области в процессе получения соляной
кислоты и гидроксида натрия из хлорида натрия.
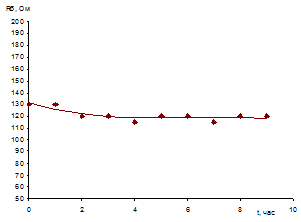
Рисунок 17 - Зависимость сопротивления биполярной области биполярной мембраны, содержащей 25 мг/дм2 гидроксида железа(III) при плотности тока 1,1 А/дм2 от времени в системе 0,5 М HCl - 0,5 М NaOH
Таблица 3
Эффективные константы скорости диссоциации молекулы воды в биполярных мембранах, модифицированных различным количеством гидроксида железа (III)
|
Тип мембраны |
k∑, 1/с |
β, м/В |
|
Аналог МБ -2 |
6,0 |
3,6 |
|
Fe(OH)3 6,25 мг/дм2 |
17,0 |
2,3 |
|
Fe(OH)3 12,5 мг/дм2 |
47,5 |
1,8 |
|
Fe(OH)3 25мг/дм2 |
53,5 |
2,0 |
|
Fe(OH)3 37,5 мг/дм2 |
62,1 |
2,0 |
|
Fe(OH)3 75 мг/дм2 |
134 |
2,0 |
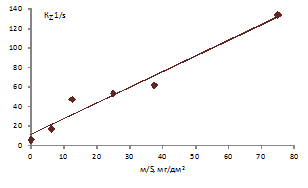
Рисунок 18 Зависимость эффективной константы диссоциации молекулы воды в биполярной мембране от количества внесённого гидроксида железа (III)
Таблица 4
Эффективных констант скорости диссоциации молекулы воды в биполярных мембранах, модифицированных гидроксидами разной природы
|
Тип мембраны |
k∑, 1/с |
β·109, м/В |
|
Аналог МБ -2 |
6,0 |
3,6 |
|
Fe(OH)3 25мг/дм2 |
53,5 |
2,0 |
|
Co(OH)3 25мг/дм2 |
48,9 |
2,0 |
|
Ni(OH)2 25мг/дм2 |
42,3 |
2,0 |
|
Cr(OH)3 25мг/дм2 |
38,9 |
2,1 |
ЗАКЛЮЧЕНИЕ
Разработан метод и изготовлена лабораторная установка для разделения порошков на фракции по размерам частиц и равномерного нанесения частиц на мембраны. Метод и установка использованы для получения фракций гидроксидов тяжёлых металлов с диаметром частиц в диапазоне 0-5 мкм и нанесения их на катионообменную мембрану, которая использовалась для получения модифицированных биполярных мембран.
Обнаружено, что введение малорастворимых гидроксидов d-металлов (хрома (III), кобальта (III), железа (III), никеля(II)) в виде порошка массой 25 мг/дм2 в область контакта катионообменной и анионообменной мембраны в биполярной мембране уменьшает перенапряжение на ней с 9,0 В на исходной мембране до 8,0-6,7 В при плотности тока 2 А/дм2. Показано, что введение малорастворимых гидроксидов хрома (III), кобальта (III), железа (III), никеля(II) в биполярную область мембран примерно на порядок (с 6 с-1 до 39-54 с-1) увеличивает эффективную константу скорости диссоциации молекул воды.
Показано, что эффективная константа скорости диссоциации молекул воды в биполярных мембранах, модифицированных гидроксидом железа (III) линейно возрастает с увеличением количества нанесённого порошка гидроксида железа.
Установлено, что в системе 0,5М HCl - 0,5М NaOH при плотности тока 1,1А/дм2
сопротивление биполярной области такой мембраны практически постоянно в течение
9 часов, что свидетельствует о стабильности гидроксида железа(III) в биполярной области в процессе
получения соляной кислоты и гидроксида натрия из хлорида натрия.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
1. Ганыч В.В. Электролитическая диссоциация молекул воды в системе раствор - анионообменная мембрана МА-40 , модифицированная ионами переходных металлов / В.В. Ганыч, Н.В. Шельдешов, В.И. Заболоцкий // Электрохимия. 1992. Т. 28, №9. С. 1390-1396.
2. Гельферих Ф. Иониты. - М.: ИЛ. 1962. С. 490.
3. Графов Б.М. Электрохимические цепи переменного тока / М.Б.М. Графов, Е.А Укше: «Наука». 1973. 128с.
4. Гребень В.П. Влияние природы ионита на числа переноса ионов через биполярные ионообменные мембраны / В.П. Гребень, И.Г Косякова, Пивоваров Н.Я. // Журн. прикл. химии. 1981. №2. С. 288-292.
5. Гребень В.П. Влияние природы ионита на физико-химические свойства биполярных ионообменных мембран / В.П. Гребень, Н.Я. Пивоваров, Н.Я. Коварский, Г.З. Нефедова // Журн. физич. химии. - 1978.Т.52. Вып. 10. - С. 2641 - 2645.
6. Гребенюк В.Д. Исследование биполярных мембран при высоких плотностях тока // В кн. Физико-химическая механика и лиофильность дисперсных систем. В.Д. Гребенюк, С.И. Муха, Л.И. Кошечкина. Киев: Наукова Думка, 1971. №2. С.133-136.
7. Гнусин Н.П. Фрейдлин Ю.Г. Исследование электрохимических свойств промышленных биполярных мембран / Н.П. Гнусин, В.И. Заболоцкий, Н.В. Шельдешов // Журн. прикл. хим. 1980. Т.53. №5. С.1069-1072.
8. Заболоцкий В.И. Импеданс биполярной мембраны МБ-1 / В.И. Заболоцкий, Н.В. Шельдешов, Н.П. Гнусин // Электрохимия. 1979. Т.15. С.1488-1493.
9. Заболоцкий В.И., Шельдешов Н.В., Гнусин Н.П. // Успехи химии. 1988. Т. 57. №8. С. 1403.
10. Заболоцкий В.И. Перенос ионов в мембранах/ В.И Заболоцкий, В.В. Никоненко. М.: «Наука». 1996. С. 392.
11. Заболоцкий В.И. Влияние природы ионогенных групп на константу диссоциации воды в биполярных ионообменных мембранах / В.И Заболоцкий, Н.В. Шельдешов, Н.П. Гнусин // Электрохимия 1986. Т.22. №12. С.1676-1679.
12. Заболоцкий В.И. Исследование процесса коррекции pH разбавленных растворов электролитов электродиализом с биполярными мембранами / В.И. Заболоцкий, С.В. Утин, Н.В. Шельдешов, К.А. Лебедев, П.А. Василенко // Электрохимия 2011. Т.47. №3. С.1-6.
13. Зубкова Л.Б. Синтетические ионообменные материалы / Л.Б. Зубкова, А.С. Тевлина, А.Б. Даванков. М. Химия. 1978. С. 184.
14. Кестинг Р.Е. Синтетические полимерные мембраны. М.: Химия, 1991. С.336.
15. Ковальчук В.И. Ионный транспорт в биполярных мембранах // Химия и технол. воды 1993. Т.15. №7-8. С.484-501.
16. Корякин Ю.В.Чистые химические вещества //Химия. 1974.
17. Ласкорин Б.Н. Ионообменные мембраны и их примрнение / Б.Н. Ласкорин, Н.М Смирнова. М.Н. Гантман С. 163. «ГосАтомИздат» 1961.
18. Мельников С.С. Влияние гидроксидов d-металлов на диссоциацию воды в биполярных мембранах С.С.Мельников, О.В. Шаповалова, Н.В. Шельдешов, В.И. Заболоцкий // Мембраны и мембранные технологии. 2011. Т. 1, №2. С. 149-156.
19. Методы измерения в электрохимии, т.1 и т.2 / Под ред. Егер Э., Залкинд А. М.: «Мир» 1977.
20. Пивоваров Н.Я. Влияние гетерогенности биполярных мембран на их вольт-амперные характеристики / Н.Я. Пивоваров, А.П. Голиков, В.П. Гребень // Электрохимия. 1997. Т.33 №5. С.582-589.
21. Пивоваров Н.Я. Обратный электродиализ с использованием биполярных мембран как источник электрической энергии / Н.Я. Пивоваров, В.П. Гребень, Н.Я. Коварский // Электрохимия 1994. Т.30. №6. С.785-789.
23. Раузен Ф.В. Использование ионитовых мембран для получения кислоты и щёлочи из засоленных сточных вод / Ф.В. Раузен, С.С. Дудник // Водоснабжение и сан. техн. - 1974. - №8. - С. 12-15.
24. Тимашев С.Ф. О механизме электролитического разложения молекул воды в биполярных мембранах / С.Ф Тимашев, Е.В. Кирганова // Электрохимия, 1981. Т. 17. С.440-443.
25. Фролов Ю.Г. Курс коллоидной химии, поверхностные явления и дисперсные системы // Наука, 2009. С.452
26. Шаповалова О.В. Исследование чисел переноса ионов водорода и гидроксила через модифицированные биполярные ионообменные мембраны / О.В. Шаповалова, Н.В. Шельдешов, В.И. Заболоцкий // Тезисы Всероссийской научной конференции с международным участием «МЕМБРАНЫ-2013». 1-4 октября 2013 г. г. Владимир, Россия. С. 342-343.
27. Шельдешов Н.В. Перенос ионов и диссоциация молекул воды в биполярных ионообменных мебранах: дис. … канд. хим. наук: 02.00.05. Шельдешов Николай Викторович. - Краснодар, 1985. - 204 с.
28. Шельдешов Н.В. Установка для комплексного электрохимического исследования ионообменных мембран / Н.В. Шельдешов, Н.П. Гнусин, В.И. Заболоцкий // Электрохимия. - 1978. - Т. 14, №6. - С. 898-900.
29. Шельдешов Н.В. Катализ реакции диссоциации воды фосфорнокислотными группами мембраны МБ-3 / Н.В. Шельдешов, В.И. Заболоцкий, Н.Д. Письменская, Н.П. Гнусин // Электрохимия. - 1986. - Т. 22. - №6. - С. 791 - 795.