Материал: Влияние соединений d-металлов на скорость диссоциации молекулы воды в биполярной мембране
Наиболее простым методом изучения зависимости падения напряжения на мембране в целом от плотности тока является изучение статических и динамических вольтамперных характеристик [5, 7].
.4.2 Метод частотного спектра электрохимического импеданса
Применение метода связано с измерением отклика объекта исследования на действие переменного электрического тока, в некоторых случаях наложенного на постоянный электрический ток.
В электрохимии развитие метод получил как инструмент для изучения механизма и кинетики электродных реакций [3, 19]. Для описания частотных спектров импеданса наиболее простых электрохимических систем был разработан подход для описания кинетики различных реакций - метод эквивалентных схем. Простота такого описания позволила применить импеданс для исследования кинетики различных электрохимических процессов. Этот подход был использован и при исследовании биполярных мембран [8] для выделения из общего импеданса и перенапряжения на мембране импеданса и перенапряжения биполярной области.
Подход, изложенный в работах [3, 5] позволяет исследовать гетерогенную химическую реакцию, которая протекает на биполярной границе, а также определить парциальные вольтамперные характеристики монополярной и биполярных областей [7, 8]. Выделение перенапряжения биполярной области позволило развить теорию строения реакционной области биполярной мембраны - ОПЗ [34].
Метод импеданса позволил оценить сверху толщину слоя (£ 1 нм), который предположительно разделяет катионообменный и анионообменный слои в двухслойной биполярной мембране, толщину модифицирующего слоя в перфторированных мембранах, геометрию пор, радиус, глубину и число пор, удельную поверхность пористой угольной мембраны и пористого титанового электрода, а также истинную площадь поверхности твердых тел.
С помощью данного метода можно рассчитать кинетические константы реакции диссоциации молекул воды, релаксация которой в реакционном слое вносит свой вклад в частотный спектр, однако этот расчет возможен при условии корректной расшифровки эквивалентной схемы мембранной системы с учетом всех основных процессов, протекающих на мембране, и структурных особенностей межфазной границы.
Несмотря на успешное моделирование отдельных процессов, до сих пор
отсутствует описание системы мембрана/раствор, достаточно полное как для
расчета кинетических констант реакции диссоциации воды, так и для расчета
параметров, характеризующих область пространственного заряда и реакционный слой
из-за большого числа параметров, от которых зависит частотный спектр импеданса
[27].
Заключение по аналитическому обзору:
Анализ литературных данных показывает, что способность ионообменных БПМ к генерации ионов Н+ и ОН- находит многочисленные применения в технологических процессах. Однако внедрение биполярного электродиализа часто ограничивается высокой себестоимостью мембран.
Выходом могло бы служить использование относительно не дорогих, по сравнению с гомогенными, гетерогенных мембран. Но их практическое применение ограничивается несбалансированными электрохимическими характеристиками: перенапряжением биполярной области, общим падением потенциала на мембране, выходом по току Н+ и ОН- и числами переноса ионов соли. Так промышленная гетерогенная биполярная мембрана МБ-2 имеет высокое напряжение даже при небольшой плотности тока, делающее невозможным её практическое применение, хотя и высокие числа переноса ионов водорода и гидроксила. Мембрана МБ-3, напротив, имеет низкое рабочее напряжение, однако низкие числа переноса ионов водорода и гидроксила в растворах кислоты и щелочи с концентрацией выше 0,5 М даже при высоких плотностях электрического тока (выше 2 А/дм2). Кроме того при производстве этой мембраны используется катионит КФ-1, который имеет высокую стоимость и сложен в синтезе.
Таким образом, задача получения новых биполярных мембраны с улучшенными электрохимическими характеристиками является актуальной. Для её решения необходим поиск недорогих исходных материалов, пригодных для использования в качестве катионообменного и анионообменного слоя биполярной мембраны, а также материалов, обладающих высокой каталитической активностью по отношению к реакции диссоциации молекул воды на межфазной границе катионообменник - анионообменник.
Согласно известным теоретическим представлениям, для повышения чисел переноса ионов водорода и гидроксила в биполярных мембранах они должны содержать в составе монополярных слоев сильнокислотные и сильноосновные ионогенные группы. Эффективным способом улучшения электрохимических характеристик гетерогенных биполярных мембран, а именно снижения их рабочего напряжения является введение в их биполярную области каталитических добавок таких как малорастворимые гидроксиды d-металлов, а также катионита с фосфорнокислотными группами. Константа скорости реакции диссоциации молекул воды в биполярных мембранах может возрастать на несколько порядков, по сравнению с исходными мембранами и для мембран, содержащих каталитическую добавку.
Анализ имеющейся научно-технической литературы показывает, что для исследования электрохимических характеристик получаемых биполярных мембран необходимо применять:
метод вольт-амперометрии, позволяющий определить и выбрать наименьшее общее напряжение на биполярной мембране, знание которого позволяет получать кислоту и щелочь с наименьшими энергозатратами;
метод частотного спектра электрохимического импеданса, с помощью которого можно измерить сопротивление биполярной области и перенапряжение на ней, что позволяет оценить эффективность использованной при получении биполярной мембраны каталитической добавки.
Электрохимические характеристики мембран с каталитическими добавками в виде малорастворимых гидроксидов и их влияние на скорость диссоциации молекулы воды исследовались многими авторами. Однако количество и размер частиц этих соединений в известных работах не учитывался, или не мог быть определён.
Поэтому целью данной работы являлось:
исследовать влияние малорастворимых гидроксидов d-металлов различной природы, при условии, что количества внесённых гидроксидов и гранулометрический состав порошков одинаковы, на электрохимические характеристики биполярных мембран: на частотные спектры электрохимического импеданса, парциальные вольт-амперные характеристики биполярных областей мембран и эффективные скорости диссоциации молекул воды в биполярных мембранах;
исследовать влияние количества внесённого гидроксида железа (III) заданного гранулометрического состава на электрохимические характеристики биполярных мембран.
Задачей работы являлась разработка метода выделения заданной фракции из исходного порошка гидроксида металла, а также разработка способа нанесения этого гидроксида на поверхность мембраны.
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
.1 Объекты исследования
Объектами исследования являлись аналоги биполярной мембраны МБ-2 полученные
прессованием катионообменных и анионообменных мембран Ralex CMH и Ralex AMH,
произведённые в Чехии, с предварительным модифицированием соединениями
переходных металлов Fe+3, Cu2+, Cr2+, Ni2+.

Рисунок 3 - Оптическое изображение среза БПМ, модифицированной
гидроксидом железа (III)
В качестве мембраны для модифицирования была выбран аналог биполярной мембраны МБ-2 (рисунок 3), как имеющая наиболее высокие числа переноса ионов водорода и гидроксила вследствие присутствия в ее катионообменном слое сильнокислотного катионообменника КУ-2, а в анионообменном слое - сильноосновного анионообменника АВ-17, диссоциация которых не подавляется в растворах сильных кислот и оснований соответственно. Выбор исходных катионообменных и анионообменных мембран в настоящее время крайне ограничен.
.2 Методика синтеза гидроксидов переходных металлов
Гидроксиды d-металлов получали химическим осаждением из 0,5 М и растворов соответствующих хлоридов металлов и 1,5 М растворов гидроксида натрия, при этом протекала реакция MeCln + nNaOH = Me(OH)n↓ + nNaCl. Затем полученный осадок отфильтровывали и промывали дистиллированной водой до pH≈7 по универсальной индикаторной бумаге [16]. Затем осадок высушивался, измельчался в фарфоровой ступке, далее из него выделялась фракция 0-5 мкм.
.3 Методика фракционирования порошков гидроксидов переходных металлов
Для выделения частиц гидроксидов переходных металлов из полидисперсного
порошка, полученного измельчением в фарфоровой ступке, использовалась разработанная
при выполнении данной работы лабораторная установка (рисунок 4), в которой
разделение происходило в восходящем потоке воздуха.
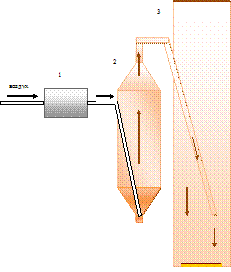
Рисунок 4 - Схема установки для фракционирования гидроксидов переходных
металлов: 1 - компрессор, 2 - разделительная колонна, 3 - седиментационная
колонна
Воздух подаётся компрессором в нижнюю часть разделительной колонны, в
которой находится полидисперсный порошок гидроксида переходного металла. В
нижней узкой части разделительной колонны скорость воздуха велика и в ней
образуется взвешенный слой порошка. При движении воздуха вверх в расширяющейся
конусной части разделительной колонны скорость воздуха постепенно уменьшается и
становится постоянной в средней цилиндрической части колонны. При этом вместе с
потоком воздуха вверх будут уноситься частицы порошка, имеющие радиус меньше
критического. Для расчёта этого радиуса учтём, что частицы порошка, имеющие
радиус равный критическому rкр, находятся во взвешенном состоянии,
так как их скорость седиментации ![]() равна скорости восходящего потока
воздуха
равна скорости восходящего потока
воздуха ![]()
![]() . (9)
. (9)
Такое состояние возможно при равенстве гравитационной силы ![]() и силы трения
и силы трения ![]() , действующих на частицу порошка [25]:
, действующих на частицу порошка [25]:
![]() . (10)
. (10)
Выражая обе силы через параметры воздуха и частиц порошка, получим:
![]() , (11)
, (11)
где h - динамическая вязкость воздуха;
![]() - линейная скорость движения воздуха;
- линейная скорость движения воздуха;
r - плотность частицы гидроксида металла;
r0 - плотность воздуха;
g - ускорение свободного падения.
Из уравнения (11) следует, что критический радиус частицы равен
а линейная скорость, при которой частицы порошка, имеющие радиус, равный
критическому, находятся во взвешенном состоянии, равна:
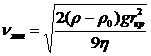 . (13)
. (13)
Рассчитанные таким образом линейные скорости использовались для расчёта объемной скорости воздуха, подаваемого в установку компрессором.
.4 Методика определения гистограммы распределения числа частиц порошка по диаметрам
Для определения гистограммы распределения числа частиц порошка по диаметрам на предметном стекле для микроскопии в капле дистиллированной воды готовили разбавленную суспензию порошка, настолько разбавленную, чтобы частицы порошка в ней практически не образовывали конгломератов. Каплю суспензии накрывали покровным стеклом.
Оптические изображения частиц исходной суспензии, полученной измельчением в фарфоровой ступке, и после фракционирования получали в проходящем свете с помощью микроскопа Альтами БИО2 при увеличениях объектива ´4, ´10, ´40, с использованием цифровой окулярной 5.1 Мпикс USB камеры UCMOS05100KPA-U-NA-N-C-SQ-NA.
Диаметры частиц и их число в заданных интервалах диаметров находили по изображениям вручную. Гистограммы распределения числа частиц порошка по диаметрам (рисунок 12) строили в программе Statistica 6.0.
.5 Методика получения биполярных мембран
Биполярные мембраны, исследованные в работе, получались горячим прессованием катионообменного и анионообменного слоёв. Температура прессования составляла 120°С, давление - 15 атм. При этом уменьшение толщины мембраны по сравнению с суммой толщин исходных катионообменной и анионообменной мембраны не превышало 1%.
.6 Методика измерения электрохимического импеданса
Для измерения частотного спектра электрохимического импеданса образцов использовался виртуальный измеритель-анализатор импеданса, сопряженный с компьютером (Рисунок 5).
Измерения действительной и мнимой части импеданса проводились в диапазоне частот переменного тока 5-1МГц на фиксированных частотах, распределенных равномерно в логарифмическом масштабе. Амплитуда измерительного переменного тока составляла 200 мВ. Относительная погрешность измерения модуля импеданса составляла не более 5%.
В данной работе частотный спектр импеданса биполярной мембраны измерялся при температуре 25ºС в проточной электрохимической ячейке с концентрацией соляной кислоты и гидроксида натрия 0,5 моль/л.
Растворы располагались таким образом, чтобы со стороны катионообменной мембраны в биполярной мембране находился раствор кислоты, а со стороны анионообменной мембраны щёлочь.
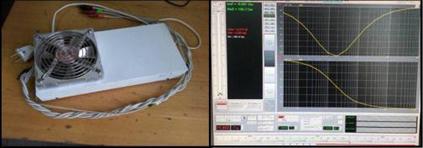
Рисунок 5 - Виртуальный измеритель-анализатор частотных спектров
импеданса, сопряженный с компьютером
На рисунке 6 показано взаимное расположение мембран, электродов и
растворов.
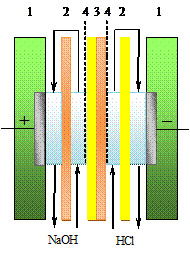
Рисунок 6 - Схема проточной четырёхэлектродной ячейки ивзаимное расположение в ней мембран: 1 - поляризующие электроды, 2 - вспомогательные мембраны, 3 - измерительные электроды, 4 - исследуемая мембрана
.7 Методика расчета парциальных по перенапряжению вольт-амперных характеристик биполярных мембран
Частотный спектр импеданса мембраны позволяет выделить из общего
сопротивления мембраны дифференциальное сопротивление биполярной области и дифференциальное
сопротивление монополярных областей [28]. Для этого экстраполяцией каждого
частотного спектра импеданса на «нулевую» и «бесконечную» частоту находят
сопротивление монополярных областей R¥ и биполярной области Rб = R0 - R¥ (рисунок 7).
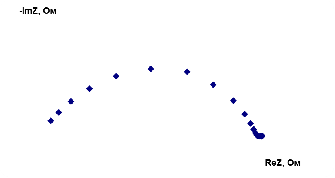

Рисунок 7 - Типичный спектр электрохимического импеданса биполярной
мембраны
Далее по зависимости дифференциальных сопротивлений биполярной области,
монополярных областей и всей мембраны от плотности тока (рисунок 8а) по формуле
(14) рассчитывают парциальные вольт-амерные характеристики биполярной области,
монополярных областей и всей мембраны (рисунок 8б).
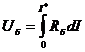 (14)
(14)
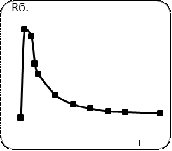

а б
Рисунок 8 - Расчёт парциальной вольт-амперной характеристики биполярной области мембраны - аналога МБ-2
а - зависимость сопротивление биполярной области от силы тока;
б - парциальная вольтамперная характеристика по перенапряжению биполярной области мембраны
.4 Методика расчёта эффективных констант скорости диссоциации молекул воды биполярной мембране
Для расчёта парциальной вольт-амперной характеристики биполярной области
в координатах «плотность тока по ионам H+, OH-» -
«перенапряжение биполярной области» использовались значения чисел перенос
биполярной мембраны - аналога МБ-2, полученные в работе [26]. Эта зависимость
позволяет корректно рассчитать эффективную константу скорости диссоциации
молекул воды в биполярной области исследуемой мембраны (рисунок 9). Для расчета
константы использовали уравнение вольт-амперной характеристики биполярной
области, предложенное в [34]: