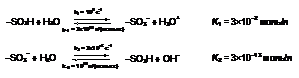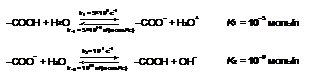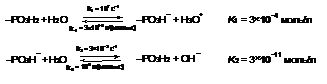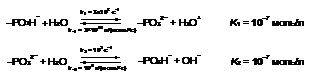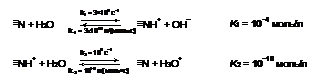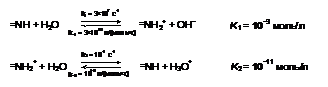Материал: Влияние соединений d-металлов на скорость диссоциации молекулы воды в биполярной мембране
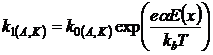 ,(3)
,(3)
или
![]() ,(4)
,(4)
где kb - постоянная Больцмана;- абсолютная температура;
a и b - характерные параметры.
Уравнение для вольт-амперной характеристики, полученное в работе [24] в предположении, что лимитирующей стадией является разложение молекул воды на активных центрах, хорошо совпадает с экспериментальными данными для МБ-1 в области высоких плотностей тока. Однако при средних и малых плотностях тока совпадение неудовлетворительное. Это вызвано тем, что исследования в [24] проводились при высоких концентрациях электролита и вклад ионов соли в перенос через мембрану был велик. Кроме того, перенапряжение на биполярной области отождествлялось с перенапряжением на всей мембране, так как метод измерения статической ВАХ мембраны в целом не позволяет выделить падение потенциала в ОПЗ. При описании биполярной области мембраны авторы пренебрегают в ней рекомбинацией ионов H+ и OH- , вследствие чего при отсутствии внешнего поля на мембране (перенапряжение на мембране равно нулю), получим отличную от нуля плотность тока, т.к. Dj0 имеет конечное значение.
Модель [24] позволяет рассчитать значения a и k0, для чего необходимо построить график в координатах «логарифм плотности тока» - «корень квадратный из разности потенциалов в переходной области». Однако данная зависимость является прямолинейной лишь при высоких значениях плотности тока.
Более общим и точным в широком диапазоне плотностей тока является
уравнение вольт-амперной характеристики, выведенное в работе Умнова, Шельдешова
и Заболоцкого [34]:
![]() ,(5)
,(5)
где Em - максимальная напряженность электрического поля в
месте контакта катионообменника и анионообменника:
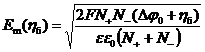 .(6)
.(6)
Уравнение, выведенное в [34] отличается от уравнения, предложенного в [24], тем, что учитывает протекание реакции рекомбинации ионов водорода и гидроксила в ОПЗ биполярной мембраны и поэтому одинаково хорошо применимо как к области больших, так и малых плотностей тока.
Модель гетерогенного биполярного контакта описывает существование в мембране каналов проводимости, образованные контактирующими друг с другом ионопроводящими участками [20]. Часть каналов не соединены между собой и поэтому не являются ионопроводящими участками, поэтому появление проводящих каналов подчиняется некоторому распределению вероятности. Вероятность образования проводящего канала связана с вероятностью выхода зерен на поверхность и определяется степенью наполнения мембран.
.2 Катализ диссоциации воды в биполярных мембранах
Большие величины плотностей тока по ионам водорода и гидроксила,
наблюдаемые на биполярных мембранах, невозможно объяснить протеканием реакции
автопротолиза воды
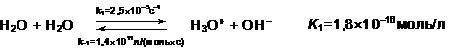
так как ток, обеспечиваемый такой реакцией, на много порядков меньше, чем наблюдаемый.
.2.1 Катализ диссоциации воды ионогенными группами в биполярных мембранах
В.П. Гребень и соавторы [5] предположили, что ионогенные группы могут
непосредственно участвовать в реакции диссоциации воды, ускоряя ее. Они
исследовали методом вольтамперометрии биполярные мембраны, содержащие
сульфоновые, карбоксильные и фосфоновые группы, и сделали вывод, что уменьшение
разности потенциалов на мембранах в ряду
- SO3H > - COOH > - PO(OH)2
pKa 1 ¸ 2 4 ¸ 6 3,5; 7
Dj (4 А/дм2), В 4 ¸ 18 2,0 ¸ 3,2 1,1 ¸ 1,7
можно объяснить снижением энергетического барьера взаимодействия
ионогенных групп с молекулами воды при увеличении в том же ряду значений pKa
катионообменных групп за счет протекания реакций в катионообменном слое
RAH + H2O ![]() RА-…Н3О+↔ RА- + Н3О+
RА-…Н3О+↔ RА- + Н3О+
RA- + H2O ![]() RАН…ОН- ↔ RАН + ОН-
RАН…ОН- ↔ RАН + ОН-
и в анионообменном слое
RKOH ![]() RKН+…ОН-
↔ RKН+ + ОН-
RKН+…ОН-
↔ RKН+ + ОН-
RK+ + 2H2O ![]() RKOH …Н3О+↔ RKOH + Н3О+
RKOH …Н3О+↔ RKOH + Н3О+
где RA- и RK+ - заряженные формы ионогенных групп соответственно в катионообменном и анионообменном слоях.
Ионогенная группа и молекула воды образует активированный комплекс, за счет образования которого энергетический барьер диссоциации воды понижается
На роль ионогенных групп мембран в диссоциации воды впервые было указано в [5] (таблица 2), где было объяснено различное поведение катионо- и анионообменных мембран.
Расчетом по известным константам диссоциации ионогенных групп и
константам скоростей было показано, что константа скорости диссоциации воды на
третичных аминогруппах на несколько порядков больше, чем в чистой воде, в то
время как на четвертичных аммониевых группах диссоциация воды невозможна.
Таблица 2
Реакции между ионогенной группой и водой, протекающие в ОПЗ [11]
|
|
Вид реакции и равновесные константы диссоциации |
|
Вода |
|
|
Сульфокислотные ионогенные группы |
|
|
Карбоксильные ионогенные группы |
|
|
Фосфорнокислотные ионогенные группы |
|
|
|
|
|
Третичные аминогруппы |
|
|
Вторичные аминогруппы |
|
|
Первичные аминогруппы |
Сульфокислотные группы катионообменных мембран не обеспечивают заметного ускорения реакции диссоциации воды [5, 7]. Так в ОПЗ биполярных мембран возможны каталитические реакции диссоциации воды с участием ионогенных групп, содержащихся в мембране, (таблица 2).
Сравнение констант лимитирующих стадий этих реакций с константой скорости автопротолиза молекул воды показывает, что ионогенные группы обеспечивают ускорение реакции диссоциации на 4 - 7 порядков.
Среди катионообменных групп фосфорнокислотные группы, а среди анионообменных - третичные аминогруппы способны наиболее эффективно ускорять реакцию диссоциации воды, снижая тем самым сопротивление биполярной мембраны.
.2.2 Катализ диссоциации воды малорастворимыми гидроксидами d-металлов
Как было сказано выше, константа скорости диссоциации молекулы воды определяет напряжение на биполярной мембране, чем она больше, тем меньше напряжение на мембране [34]. В работе [40] было впервые предложено введение малорастворимых гидроксидов d-металлов в БПМ для снижения напряжения на ней. В дальнейшим изучение влияния малорастворимых гидроксидов на монополярные и на биполярные мембраны было исследовано многими авторами как иностранными, так и российскими.
Образующийся в процессе электродиализа природной, в частности морской воды на поверхности мембраны осадок гидроксидов тяжёлых металлов может изменять условия, в которых протекает реакция диссоциации молекулы воды. Это явление было изучено автором [35, 36]. Результаты исследований влияния гидроксидов различных металлов на процесс диссоциации воды показали, что такие гидроксиды как Mg(OH)2, Ni(OH)2, Fe(OH)3, Co(OH)2, Al(OH)3, осаждающиеся на поверхности катионообменной мембраны, вызывают ускорение реакции диссоциации воды. Причиной этого явления, по мнению авторов, является взаимодействие ионов OH-, генерируемых в реакционном слое между мембраной и слоем осадка. Но сам механизм реакции в [35, 36] так и не был установлен.
В работах Шельдешова Н.В., Заболоцкого В.И. и Ганыч В.В. было изучено влияние
малорастворимых гидроксидов на катионообменную мембрану МК-40 и влияние
соединений d-металлов в системе раствор - анионообменная мембрана МА-40 на
реакцию диссоциации молекулы воды [1, 30]. Был также предложен механизм, по
которому происходит увеличение скорости диссоциации молекулы воды, включающего
каталитическое действие частиц гидроксидов металлов [30]:
![]()
![]()
![]() (7)
(7)
![]()
![]()
![]() (8)
(8)
В работе Мельникова С.С. и соавторов [18] было исследовано влияние гидроксидов переходных металлов Cu2+, Fe3+, Cr3+, Ni2+ на скорость диссоциации молекулы воды в ассиметричной биполярной мембране, полученных электрохимическим методом. Авторы расширили каталитический ряд ионогенных групп мембран, предложенный в [9], дополнив его гидроксидами металлов [18]:
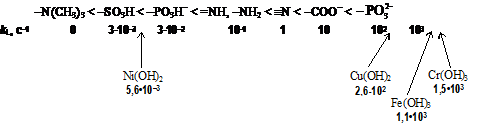
.3 Процессы с применением биполярных мембран
Электромембранные способы получения кислот, щелочей и оснований с применением биполярных мембран из соответствующих солей и воды по реакции:
+ H2O ®
KOH + HA
имеют ряд преимуществ по сравнению с классическими электрохимическими. Типичная последовательность мембран в электродиализных аппаратах, реализующих эти способы (рисунок 1). При наложении электрического поля на такой аппарат биполярная мембрана генерирует ионы водорода и гидроксила
2O
® H+ + ОH-.
Анионы соли, мигрирующие из камеры 3 через анионообменную мембрану, и ионы водорода, мигрирующие через катионообменную область биполярной мембраны, в камере 4 образуют кислоту. Аналогичный процесс, но с участием ионов гидроксила и катионов соли приводит к образованию щёлочи в камере 5 и 7.
Отвод образующихся растворов кислоты и щёлочи из аппарата осуществляется
промывкой камер 4, 5, 7 дистиллятом или разбавленным раствором кислоты и
щёлочи. Через камеры 2, 3, 6 циркулирует раствор исходной соли. В процессе
работы электродиализного аппарата концентрация соли и объём воды в камерах 2,
3, 6 уменьшается и для поддержания стационарного режима работы в эти растворы
необходимо добавлять новые порции соли и воды. Вода из камеры 3 и 6 удаляется в
виде гидратной воды вместе с ионами, уходящими через катионообменную и
анионообменную мембрану, и электроосмотически.
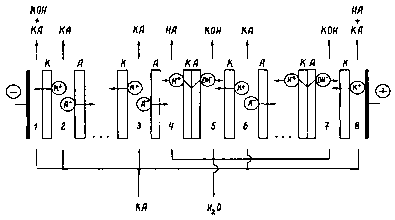
Рисунок 1 - Схема мембранного пакета электродиализного аппарата для
получения сильнодиссоциирующих кислот и щелочей
Главное преимущество электродиализного способа получения кислот и щелочей заключается в том, что в элементарной ячейке (3-6) нет металлических электродов, а значит, растворы не загрязняются продуктами их разрушения. Газовыделение, которое особенно опасно в случае образования на аноде таких окислителей, как хлор к кислород, также отсутствует. В растворах 3, 4, 5, 6 сохраняются ионы, которые могли бы окислиться или восстановиться на электродах. Элементарная ячейка 3-6 может повторяться в пакете электродиализатора неограниченное число раз, при этом пакет содержит только один катод и анод.
Для получения слабодиссоциирующих кислот и оснований в основном
применяются более простые схемы электродиализного пакета, имеющие двухкамерную
элементарную ячейку (рисунок 2).
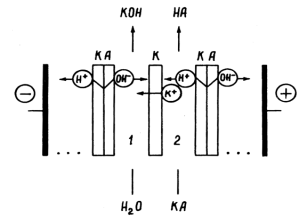
Рисунок 2 - Схема мембранного пакета электродиализного аппарата для
получения слабодиссоциирующих оснований из солей
При работе такой ячейки ионы водорода, поступающие в камеру 2, связываются в слабодиссоциирующую кислоту и не проникают в камеру 1. Выход по току и концентрация слабодиссоциирующей кислоты в этом случае значительно выше, чем сильнодиссоциирующей кислоты, получаемой в aппаpaтe, изображённом на рисунке 2. Концентрация слабодиссоциирующей кислоты ограничена только её растворимостью. В этих способах синтеза кислот и оснований предъявляются повышенные требования к числам переноса органических ионов через мембраны, так как их утечка через мембраны приводит к потере продукта.
Исследованы процессы получения слабодиссоциирующих кислот: уксусной кислоты из ацетата натрия, щавелевой кислоты из оксалата натрия, борной кислоты из тетрабората калия, лимонной, салициловой, глюколивой, молочной, аскорбиновой.
Ряд оснований, полученных с помощью электродиализа с биполярными мембранами несколько уже, чем ряд кислот: исследованы процессы получения пиридина и триэтаноламина, этилендиамина и полиэтиленполиаминов из их солей.
Применение биполярных мембран позволяет обессоливать растворы и получать деионизованную воду, а также одновременно с обессоливанием раствора корректировать рН обрабатываемых растворов.
1.4 Методы исследования биполярных мембран
В процессе синтеза новых БПМ большое внимание должно быть уделено исследованию свойств полученных образцов для последующего выбора условий синтеза, обеспечивающих улучшение электрохимических характеристик синтезируемых мембран. Актуальной задачей является выбор среди известных методов исследования тех, которые позволяют получить необходимую и достаточную информацию о свойствах мембран при минимальных затратах времени. Принципы изучения основных электрохимических свойств достаточно подробно описаны в литературе [2, 7, 24]. диссоциация биполярный электрохимический импеданс
БПМ должны обладать следующими электрохимическими свойствами: низким сопротивлением в режиме генерации ионов, низкими числами переноса коионов соли и способностью сохранять свойства при контакте с концентрированными растворами кислот и щелочей.
.4.1 Метод вольт-амперометрии
Метод вольт-амперометрии, широко применяемый в классической электрохимии [19], применяется и в мембранной электрохимии, в частности для исследования биполярных мембран. Вид вольт-амперной характеристики (ВАХ) определяется структурой мембраны и природой процессов, протекающих в ней при поляризации электрическим током. Падение потенциала на мембране представляет собой сумму нескольких составляющих: потенциалов Доннана на границах мембрана - раствор, омического падения напряжения на монополярных слоях, которое определяется структурой слоёв и типом носителя заряда; падением потенциала на биполярной границе.
При поляризации БПМ током в переносе участвуют главным образом ионы Н+ и ОН-. Скорость реакции диссоциации, протекающей в области пространственного заряда, определяет количество переносчиков тока, что отражается на виде ВАХ. Измерение ВАХ позволяет исследовать лимитирующие стадии процесса диссоциации воды, которые связаны с: переносом воды из объема раствора к биполярной границе; реакцией диссоциации молекул воды; миграционным выносом продуктов реакции под действием электрического поля. При высоких плотностях тока, либо высоких скоростях развертки ВАХ (0,943 А/(дм2·с)) достигается предельный ток, связанный замедленной доставкой воды в зону реакции. Измерение ВАХ биполярной области позволяет исследовать реакцию диссоциации воды, которая протекает на активных центрах в ОПЗ [10, 24].