Материал: Влияние соединений d-металлов на скорость диссоциации молекулы воды в биполярной мембране
Влияние соединений d-металлов на скорость диссоциации молекулы воды в биполярной мембране
Министерство образования и науки российской федерации
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Кубанский государственный университет
Факультет химии и высоких технологий
Кафедра физической химии
Направление
бакалаврской подготовки 020100.62 Химия
Выпускная квалификационная работа бакалавра
Влияние соединений d-металлов на скорость диссоциации
молекулы воды в биполярной мембране
Работу выполнила Н.В. Алпатова
Научный руководитель, проф.,
д-р хим.
наук, доц. Н.В. Шельдешов
Краснодар 2014
РЕФЕРАТ
Дипломная работа содержит 51 страниц, 18 рисунков, 4 таблицы, 44 литературных источников.
Гетерогенная биполярная мембрана, вольтамперная характеристика, малорастворимые гидроксиды металлов электрохимический импеданс, эффективная константа скорости диссоциации молекулы воды
Объектами исследования является аналог биполярной мембраны МБ-2, модифицированный гидроксидами d-металлов - Fe+3, Cо3+, Cr3+, Ni2+.
Цель данной работы - изучение влияния малорастворимых гидроксидов d-металлов на электрохимические характеристики, а также на скорость диссоциации молекулы воды в биполярной мембране.
Сопротивление биполярных областей измерялись методом электрохимического импеданса. Парциальные по перенапряжению вольтамперные характеристики этих областей рассчитывались по зависимости их сопротивления от плотности тока. Эффективные константы скорости диссоциации молекулы воды рассчитывались по парциальной вольтамперной характеристики биполярной области, которая измерялась с помощью метода электрохимического импеданса.
Разработан метод и изготовлена лабораторная установка для разделения
порошков на фракции по размерам частиц и равномерного нанесения частиц на
мембраны. Обнаружено, что введение малорастворимых гидроксидов d-металлов в виде порошка массой 25
мг/дм2 в биполярную область уменьшает перенапряжение на ней с 9,0 В
на исходной мембране до 8,0 - 6,7 В при плотности тока 2 А/дм2.
Показано, что введение малорастворимых гидроксидов металлов в биполярную
область мембран примерно на порядок (с 6 с-1 до 39-54 с-1)
увеличивает эффективную константу скорости диссоциации молекул воды и линейно
зависит от количества нанесённого порошка гидроксида. Установлено, что в
системе 0,5М HCl-0,5М NaOH при плотности тока 1,1 А/дм2 сопротивление
биполярной области такой мембраны практически постоянно в течение 9 часов, что
свидетельствует о стабильности гидроксида железа(III) в биполярной области в процессе получения соляной
кислоты и гидроксида натрия из хлорида натрия.
СОДЕРЖАНИЕ
Введение
. Аналитический обзор
.1 Строение и свойства биполярных мембран
.1.1 Строение и свойства монополярных областей
.1.2. Механизм диссоциации воды в биполярных мембранах
.2 Катализ диссоциации воды в биполярных мембранах
.2.1 Катализ диссоциации воды ионогенными группами в биполярных мембранах
.2.2 Катализ диссоциации воды малорастворимыми гидроксидами d-металлов
.3 Процессы с применением биполярных мембран
.4 Методы исследования биполярных мембран
.4.1 Метод вольт-амперометрии
.4.2 Метод частотного спектра электрохимического импеданса
. Экспериментальная часть
.1 Объекты исследования
.2 Методика синтеза гидроксидов переходных металлов
.3 Методика фракционирования порошков гидроксидов переходных металлов
.4 Методика определения гистограммы распределения числа частиц порошка по диаметрам
.5 Методика получения биполярных мембран
.6 Методика измерения электрохимического импеданса
.7 Методика расчета парциальных по перенапряжению вольт-амперных характеристик биполярных мембран
.4 Методика расчёта эффективных констант скорости диссоциации молекул воды биполярной мембране
. Результаты и обсуждение
.1 Результаты определения размеров частиц порошков гидроксидов переходных металлов
.2 Зависимость электрохимических характеристик биполярных мембран от количества порошка гидроксида металла
.3 Влияние природы тяжёлого металла на электрохимические характеристики биполярной области мембран
.4 Исследование каталитической активности гидроксида железа (III) при длительном использовании модифицированной биполярной мембраны
.5 Расчёт эффективных констант скорости диссоциации молекул воды в биполярных мембранах
Заключение
Список
использованных источников
ВВЕДЕНИЕ
Биполярные гетерогенные мембраны (БПМ) - бислойные композиты, которые состоят из катионообменного и анионообменного слоёв. На границе этих слоёв возникает область пространственного заряда, в которой при прохождении электрического тока протекает реакция диссоциации молекул воды с образованием ионов водорода и гидроксила. На использовании этой реакции основаны многочисленные применения биполярных мембран: получение неорганических и органических кислот, оснований и щелочей из солей, коррекция рН водных растворов, получение деионизованной воды, удаление углекислого газа из воздуха.
Константа скорости диссоциации молекулы воды в области пространственного заряда определяет напряжение на БПМ: чем она больше, тем меньше напряжение на мембране. От величины рабочего напряжения на мембране зависит возможность применения БПМ в технологическом процессе. Известно, что снизить напряжение на мембране позволяют органические и неорганические соединения, введённые в её биполярную область. В настоящее время наиболее дешёвыми и доступными добавками являются гидроксиды металлов.
Изменение скорости диссоциации молекулы воды на границы мембрана - раствор по сравнению со скоростью диссоциации молекулы воды в водных растворах исследовалось многими авторами. При этом изучалось влияние на диссоциацию как ионогенных групп мембран, так и каталитических добавок органической и неорганической природы, введённых в биполярную область мембраны. Диссоциация молекул воды исследовались как в монополярных, так и в биполярных мембранах.
Многими авторами исследовались электрохимические характеристики мембран с каталитической добавкой в виде малорастворимых гидроксидов и их влияние на скорость диссоциации молекулы воды. Но количество и размер частиц этих соединений не учитывался или не мог быть определён.
Поэтому целью данной работы являлось:
исследовать влияние малорастворимых гидроксидов d-металлов различной природы, при условии, что количества внесённых гидроксидов и гранулометрический состав порошков одинаковы, на электрохимические характеристики биполярных мембран: на частотные спектры электрохимического импеданса, парциальные вольт-амперные характеристики биполярных областей мембран и эффективные скорости диссоциации молекул воды в биполярных мембранах;
исследовать влияние количества внесённого гидроксида железа (III) заданного гранулометрического состава на электрохимические характеристики биполярных мембран.
Задачей работы являлась разработка метода выделения заданной фракции из
исходного порошка гидроксида металла, а также разработка способа нанесения
этого гидроксида на поверхность мембраны.
1. АНАЛИТИЧЕСКИЙ ОБЗОР
.1 Строение и свойства биполярных мембран
Биполярные мембраны представляют собой бислойные композиты, состоящие из соединённых друг с другом катионообменной и анионообменной мембран. При наложении электрического поля в месте контакта этих слоёв возникает область пространственного заряда с высокой напряжённостью электрического поля. Такие мембраны способны генерировать ионы водорода и гидроксила из молекул воды в результате реакции диссоциации воды, на скорость которой влияет как напряженность электрического поля, так и природа ионогенных групп мембраны и каталитических добавок. Получившиеся ионы водорода и гидроксила мигрируют их области пространственного заряда в катионообменный слой (ионы водорода) и в анионообменный слой (ионы гидроксила). То есть биполярную мембрану можно представить как электрохимический реактор, способный разделять продукты реакции и выводить их за пределы реакционной зоны. На этом важном свойстве биполярных мембран основано их применение в установках для электродиализа и коррекции pH [12, 22, 31].
Но на практике при протекании электрического тока через биполярную мембрану кроме основного процесса - диссоциации молекул воды происходит еще и перенос ионов соли. Этот процесс является нежелательным процессом, так как он приводит к снижению выхода ионов Н+ и ОН- по току, а также к загрязнению получаемых кислот, щелочей и оснований [7]. Числа переноса ионов соли через биполярные мембраны зависят от природы и тощины катионообменного и анионообменного слоёв, из которых изготовлена мембрана.
.1.1 Строение и свойства монополярных областей
Для создания биполярных гетерогенных мембран могут использоваться
различные типы ионообменных монополярных мембран и их различное сочетание. Так
к гетерогенным биполярным мембранам относятся отечественные мембраны МБ-1,
МБ-2, МБ-3, монополярные слои которых идентичны выпускаемым монополярным
катионообменным (МК-40, МК-41) и анионообменным (МА-40, МА-41) мембранам в
различном сочетании таблица [1].
Таблица 1
Характеристики промышленных биполярных мембран
|
Марка БПМ |
КО мембрана АО мембрана |
Ионогенные группы |
|
МБ-1 |
МК-40 МА-40 |
-SO3H ºN,=NH,-NH2 |
|
МБ-2 |
МК-40 МА-41 |
|
|
МБ-3 |
МК-41 МА-41 |
-PO3H2,-PO3H-, -N+(CH3)3 |
Электрохимические свойства монополярных слоев БПМ обусловливают способность противоионов и коионов участвовать в процессах переноса. Присутствие в мембране коионов связано с поглощением электролита мембраной из раствора, как гелевыми участками (доннановское равновесие), так и межгелевыми промежутками. При протекании электрического тока коионы могут переноситься в гетерогенной мембране за счет миграции в электрическом поле, а также диффузией, в основном по межгелевым промежуткам, что и является причиной неселективного переноса ионов соли через монополярные слои БПМ.
Селективность монополярных слоев в значительной мере определяется степенью диссоциации фиксированных групп и их концентрацией [2]. Чтобы уменьшить перенос ионов соли через биполярную мембрану в качестве катионообменного и анионообменного слоев используются мембраны с сильнокислыми и сильноосновными группами. Диссоциация этих групп подавляется в меньшей степени, чем слабокислотных (карбоксильных) и слабоосновных (первичные, вторичные, третичные аминогруппы), когда биполярная мембрана находится в контакте с раствором кислоты и щелочи.
Использование монополярных слоев, содержащих в своем составе ионогенные группы с высокой степенью диссоциации, позволяет повысить числа переноса ионов Н+ и ОН- через биполярную мембрану, но приводит к высокому рабочему напряжению наней, что делает ее непригодной для практического применения. С другой стороны, рабочее напряжение на биполярной мембране мало в случае применения в катионообменном слое фосфоновых (слабокислотных) ионогенных групп или третичных аминогрупп (слабоосновных) в анионообменном слое, однако в этом случае возрастают числа переноса ионов соли через мембрану вследствие подавления степени диссоциации ионогенных групп, снижения обменной ёмкости катионообенного и анионообменного слоя и увеличения концентраций ионов соли за счёт их необменной сорбции в этих слоях. Таким образом, требования к составу катионообменного и анионообменного слоев биполярной мембраны с точки зрения чисел переноса ионов и рабочего напряжения на мембране являются взаимно противоположными [4].
Увеличение чисел переноса коионов соли при увеличении концентрации электролитов в прилегающих к мембране растворах можно объяснить тем, что при этом концентрация коионов на границе мембрана - раствор со стороны мембраны увеличивается, и в фазе мембраны увеличивается градиент концентрации коионов [4]. Таким образом, с увеличением концентрации внешних растворов увеличивается как миграционный, так и диффузионный поток.
Так как диффузионный поток слабо зависит от плотности тока, то при высоких плотностях тока числа переноса коионов становятся намного меньше, чем числа переноса ионов водорода и гидроксила [10]. Это связано с малым вкладом диффузионного потока вещества к биполярной границе в общий поток при больших плотностях тока. Дальнейшие исследования показали [6], что перенос коионов соли при поляризации БПМ происходит в основном по межгелевым промежуткам и порам. Уменьшение количества ионизированных групп (например, вследствие разогрева мембраны, как у МБ-2, и частичного дезаминирования) приводит к увеличению числа переноса коионов [6] вследствие увеличения доннановской (необменной) сорбции.
Перенос двухзарядных ионов через БПМ намного меньше однозарядных, вследствие их большего электростатического отталкивания от одноименно заряженных фиксированных ионов в тех слоях БПМ, где они являются коионами [2].
.1.2 Механизм диссоциации воды в биполярных мембранах
Существует несколько моделей строения биполярной области: модель «нейтрального» слоя, модель области пространственного заряда, модель гетерогенной биполярной границы.
Модель области пространственного заряда описывает область контакта
катионообменника и анионообменника как аналог p-n перехода на границе раздела
полупроводников р- и n-типа [24]. В этой области формируется двойной
электрический слой - область пространственного заряда - с высокой
напряжённостью электрического поля. Распределение электрического потенциала
Е(x) в ОПЗ в этой модели описывается системой уравнений Пуассона - Больцмана.
Решение этой системы уравнений в приближении Шоттки (ОПЗ рассматривается как
истощенный по носителям заряда слой, предполагается, что в ОПЗ отсутствуют
подвижные ионы и объемный электрический заряд обусловлен только фиксированными
ионогенными группами монополярных мембран) имеет вид
![]() (1)
(1)
где N± - концентрация ионогенных групп в анионообменном и катионообменном слоях БПМ;
lа,к - толщина анионообменной и катионообменной части ОПЗ;
е - заряд электрона;
e - диэлектрическая проницаемость ОПЗ;
e0 - диэлектрическая проницаемость вакуума.
Протяженность реакционного слоя находится по величине падения потенциала
(Dj = Dj0 +hb) в
биполярной области
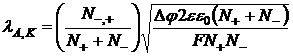 (2)
(2)
где Dj0 - падение потенциала в ОПЗ в отсутствии поляризации;
hb - перенапряжение биполярной области.
Влияние напряженности электрического поля в области пространственного заряда биполярных мембран на константу скорости диссоциации молекул воды было впервые учтено в работах Тимашева и сотр. [24]
Неявным образом модель включает катализ диссоциации воды ионогенными
группами, так как рассматривается гетеролитическая реакция на активных центрах.
Константа скорости прямой реакции k0 в анионо- и катионообменнике в
отсутствии поля превосходит константу скорости гомогенной диссоциации воды.
Зависимость k1 от напряженности E электрического поля описывается
уравнением