Материал: В-Л-Быков-Цитогогия_и_общая_гистология
компонентов. Содержание лизосом связано с функциональной активностью мьппцы и возрастом человека. Остаточные тельца лизосомального генеза, содержание липофусцин, становятся многочисленными при старении и, в особенности, при резком снижении функциональной активности мышцы.
Миосателлитоциты - мелкие уплощенные клетки, располагающиеся в неглубоких вдавлениях сарколеммы миосимпластической части мышечного волокна и покрытые вместе с ней общей базальной мембраной (см. рис. 13-3). Ядро миосателлитоцита - плотное, относительно крупное (занимает почти всю клетку), с более высоким содержанием гетерохроматина, чем в ядрах миосимпласта, органеллы мелкие и немногочисленные. Эти клетки представляют собой камбиальные элементы скелетной мышечной ткани. Они активируются при повреждении мышечных волокон и обеспечивают их репаративную регенерацию. Слипаясь с симпластической частью волокна при усиленной нагрузке, миосателлитоциты участвуют в его гипертрофии. В мышечных волокнах у плода и новорожденного доля ядер миосателлитоцитов достигает 30-35% от общего содержания ядер; после рождения она быстро снижается, составляя в детстве 7-10%, а у взрослого - около 5%. Содержание этих клеток выше красных волокнах, чем в белых (см. ниже).
Типы мышечных волокон
Мышечные волокна в скелетных мышцах позвоночных животных и человека обладают, несмотря на общий план строения, определенными структурными, биохимическими и функциональными различиями. Используемые классификации мышечных волокон основаны на учете их различных признаков и совпадают неполностью. В обобщенном виде можно условно выделить три основных тина мышечных волокон, между которыми существуют переходные варианты (рис. 13-9): тип I (красные), тип IIВ (белые) и тип IIА (промежуточные).
Тип I - красные, медленные, тонические, устойчивые к утомлению, с небольшой силой сокращения, окислительные. Характеризуются малым диаметром, относительно тонкими миофибриллами, высокой активностью окислительных ферментов (например, сукцинатдегидрогеназы - СДГ), низкой активностью гликолитических ферментов и миозиновой АТФазы, преобладанием аэробных процессов, высоким содержанием миоглобина (определяющим их красный цвет), крупных митохондрий (занимают около 15% объема саркоплазмы) с многочисленными кристами и липидных включений, широкой (50-100 нм)
- 421 -
Z-линией, высоким содержанием миосателлитоцитов, богатым кровоснабжением. Численно преобладают в мышцах, выполняющих длительные тонические нагрузки.
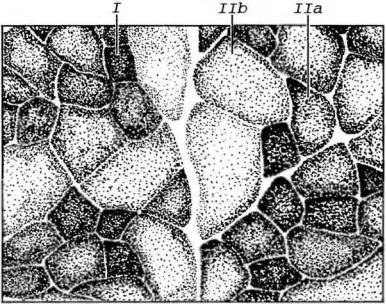
Рис. 13-9. Типы мышечных волокон в скелетной мышце. На препарате - поперечном срезе мышечных волокон - проведено гистохимическое выявление фермента сукцинатдегидрогеназы (СДГ). Плотность продукта гистохимической реакции пропорциональна активности СДГ. Представлены три основных типа мышечных волокон: тип I (I) - красные (с высокой активностью СДГ), тип IIВ (IIВ) - белые (с низкой активностью СДГ) и тип IIА (IIА) - промежуточные (с умеренной активностью СДГ).
Тип IIВ - белые, быстрые, тетанические, легко утомляющиеся, с большой силой сокращения, гликолитические. Характеризуются большим диаметром, крупными и сильными миофибриллами, высокой активностью глпколитических ферментов (например, лактатдегидрогеназы - ЛДГ) и АТФазы, низкой активностью окислительных ферментов, преобладанием анаэробных процессов, относительно низким содержанием митохондрий (более мелких и с менее развитыми кристами, чем в волокнах I типа и занимающих около 7% объема саркоплазмы), липидов и миоглобина (определяющим их светлый цвет), значительным количеством гликогена, узкой (30-40 нм) Z-линией, относительно небольшим числом миосателлитоцитов, сравнительно слабым кровоснабжением. Преобладают в мышцах, выполняющих быстрые движения, например, мышцах конечностей.
- 422 -
Тип IIА - промежуточные, быстрые, устойчивые к утомлению, с большой силой, оксилительно-гликолитические. На препаратах напоминают волокна типа I. В равной степени способны использовать энергию, получаемую путем окислительных и гликолитических реакций. По своим морфологическим и функциональным характеристикам занимают положение, промежуточное между волокнами типа I и IIВ.
Красные и белые волокна различаются также содержанием различных изоформ миозина и субъединиц тропонина. В частности, изоформы миозина, характерные для белых волокон, отличаются более быстрой циклической активностью миозиновых мостиков, а, следовательно, большей скоростью сокращения.
Соотношение числа волокон различных типов в мышце. Скелетные мышцы человека являются смешанными, т.е. содержат волокна различных типов, которые распределены в них мозаично. Соотношение красных и белых волокон в мышцах каждого человека индивидуально, предопределено генетически и почти не меняется с возрастом. В мышцах большинства людей белые и красные волокна содержатся примерно в равных количествах. Вместе с тем, у отдельных людей могут преобладать волокна того или иного типа, что что позволяет им более успешно справляться с длительной физической нагрузкой небольшой мощности или с кратковременной тяжелой нагрузкой.
Изменения в волокнах различных типов при тренировке мышц
неодинаковы и зависят от характера нагрузок. Нарастание массы мышц при этом связано с увеличением диаметра (гипертрофией) мышечных волокон (главным образом, белых); в последние годы вновь высказываются взгляды о возможности некоторого увеличения и числа волокон при очень высоких нагрузках.
РЕГЕНЕРАЦИЯ СКЕЛЕТНОЙ МЫШЕЧНОЙ ТКАНИ
Физиологическая регенерация волокон скелетной мышечной ткани
непрерывно осуществляется в нормальных условиях на ультраструктурном уровне и состоит в самообновлении их органелл и других структурных компонентов, обеспечивающем поддержание баланса между анаболическими и катаболическими процессами.
Гипертрофия мышечных волокон развивается в ответ на повышенные нагрузки в результате преобладания анаболических процес-
- 423 -
сов над катаболическими. Она проявляется увеличением содержания компонентов их саркоплазмы; при этом нагрузки, требующие выносливости, вызывают увеличение всего объема саркоплазмы и, особенно, митохондрий, а скоростно-силовые нагрузки - преимущественное нарастание массы миофибрилл (вследствие увеличения их числа и диаметра).
Атрофия мышечных волокон возникает вследствие бездействия (при денервации или гипокинезии), а также при голодании.
Денервация вызывает снижение массы мышцы на 50% и более, уменьшение диаметра волокон, дезорганизацию сократительного аппарата и элементов цитоскелета, сглаживание различий их типов. Наиболее быстро атрофируются белые волокна, красные изменяются в меньшей степени.
Гипокинезия обусловливает более выраженные изменения в красных волокнах, которые более чувствительны к снижению нагрузки, чем белые, которые вовлекаются в процесс атрофии позднее. Выраженные явления мышечной атрофии развивается у космонавтов; наибольшие изменения при этом отмечены в красных мышечных волокнах.
Голодание сопровождается распадом белков миофибриллярного аппарата и поражает в первую очередь белые волокна.
Репаративная регенерация мышечных волокон направлена на восстановление их целостности после повреждения и частично напоминает эмбриональный миогенез. При любых видах травмы процесс регенерации включает закономерную последовательность явлений:
(1)инфильтрацию области повреждения фагоцитами,
(2)восстановление целостности сосудов (реваскуляризацию),
(3)фагоцитоз некротизированных мышечных волокон,
(4)пролиферацию миогенных клеток-предшественников,
(5)их последующее слияние с образованием мышечных трубочек,
(6)дифференцировку трубочек с образованием зрелых мышечных волокон,
(7)восстановление иннервации.
Миграция фагоцитов (нейтрофилъных гранулоцитов и макрофагов) в
область повреждения происходит под хемотаксическим действием продуктов, выделяемых травмированными волокнами. Устремляясь к поврежденным волокнам, фагоциты активно поглощают тканевой детрит, часто сохраняя базальную мембрану разрушенных волокон. Вместе с тем, получены сведения, что чрезмерная активация инфильтрирующих фагоцитов в очаге повреждения может вызвать их дегрануляцию с выделением ряда токсических продуктов, воздействие которых способно усугубить начальное повреждение мышечных волокон.
- 424 -
Собственно регенерация мышечных волокон начинается одновременно с поглощением фрагментов некротизированной ткани фагоцитами и, очевидно, может осуществляться несколькими механизмами:
1.Путем роста утолщенных концов поврежденных волокон (мышечных почек) навстречу друг другу, который обеспечивается в результате формирования в их миофибриллах новых саркомеров, связывающихся с ранее образованными (подобно тому, как это происходит при физиологическом росте мышцы),
2.Путем активации системы миосателлитоцитов (вблизи участка травмы), которые усиленно размножаются, мигрируют в область повреждения, располагаясь внутри цилиндров, образованных базальной мембраной разрушенных волокон, и дифференцируются в миобласты. Миобласты в дальнейшем, по-видимому, могут:
(а) сливаться друг с другом и формировать мышечные трубочки (подобно тому, что происходит при эмбриональном развитии мышцы), превращающиеся
вновые мышечные волокна, которые соединяются с концами сохранившихся и постепенно замешают дефект между ними;
(б) включаться в мышечные почки, усиливая их рост навстречу друг другу.
Пролиферация миосателлитоцитов вблизи участка травмированной мышечной ткани происходит под митогенным влиянием веществ, выделяемых поврежденными волокнами. Этот процесс и последующая дифференцировка миосателлитоцитов регулируются рядом факторов роста (ФРФ, ТРФР. инсулиноподобный фактор роста и др.).
Использование миосателитоцитов для стимуляции регенерации мышечной ткани стало реальным в последние годы благодаря возможности выделения этих клеток из ткани. В настоящее время разрабатываются методы стимуляции восстановления структуры поврежденных скелетных мышц путем введения в них миосателлитоцитов. В экспериментальных условиях предприняты также попытки использования этих клеток для замещения погибшей сердечной мышечной ткани. Показано, в частности, что при введении в поврежденный миокард миосателлитоциты формируют волокна скелетной мышечной ткани, которые устанавливают связь с кардиомиоцитами.
Новые мышечные волокна, образовавшиеся в зонах повреждения в результате слияния миобластов, - тонкие, нередко с центрально расположенными (как в мышечных трубочках) ядрами. Неполностью сливаясь друг с другом или исходным регенерирующим волокном, они формируют так называемые расщепленные волокна. Такая картина, в част-
- 425 -