Материал: В-Л-Быков-Цитогогия_и_общая_гистология
Цитоплазма характеризуется уменьшением количества элементов грЭПС, рибосом, митохондрий, редукцией комплекса Гольджи. В ней появляются третичные гранулы (у нейтрофильных гранулоцитов); внутри специфических гранул образуются кристаллоиды (у эозинофильных гранулоцитов), отмечаются количественные и качественные изменения цитоскелета (обеспечивающие высокую подвижность, образование псевдоподий) и рецепторного аппарата плазмолеммьг (обусловливающие высокую способность к хемотаксису, фагоцитозу, адгезивным взаимодействиям и распознаванию различных сигнальных молекул).
Цикл развития гранулоцитов в миелоидной ткани включает:
(1)стадии, связанные с митотическим делением клеток, - от СКК до миелоцита включительно (длительность - 5-7 сут.);
(2)стадии созревания (дифференцировки) постмитотических клеток - начиная с метамиелоцита до сегментоядерных форм (длительность - около 3-4 сут.);
(3)накопление структурно зрелых гранулоцитов в костном мозге (длительность - около 4-5 сут.) - создает значительные запасы этих клеток, которые могут выбрасываться костным мозгом при возникновении острой потребности; за счет этой стадии общее количество гранулоцитов в миелоидной ткани в 10 раз превышает их содержание в крови;
(4)выделение зрелых клеток в кровь.
После циркуляции в крови в течение нескольких часов гранулоциты мигрируют в периферические ткани, где осуществляют свои функции (см. главу
7).
Повышение количества гранулоцитов в крови может осуществляться двумя механизмами:
1.При острой потребности гранулоциты (в особенности, нейтрофильные), быстро мобилизуются из очень обширного пула зрелых клеток, находящихся в миелоидной ткани.
2.При необходимости длительного поддержания высокого уровня этих клеток в крови (например, при бактериальной инфекции) происходит стимуляция пролиферации различных стадий развития гранулоцитов в костном мозге, которая регулируется системным и местным выделением цитокинов (гемопоэгпинов).
Регуляция развития гранулоцитов цитокинами осуществляется на различных уровнях и с участием большого количества разнообразных факторов. Наибольшее специфическое стимулирующее влияние оказывают на развитие:
- 266 -
нейтрофильных гранулоцитов - Г-КСФ и ГМ-КСФ; эозинофильных гранулоцитов - ИЛ-5 и ГМ-КСФ; базофильных гранулоцитов - ИЛ-3 и ИЛ-4.
МОНОЦИТОПОЭЗ
Моноцнтопоэз - процесс развития моноцитов - происходит в красном костном мозге и описывается последовательностью:
СКК -> КОЕ-ГЭММ -> КОЕ-ГМ -> КОЕ-М монобласт > промонопит -> моноцит.
Промоноцит - сравнительно крупная клетка (диаметром 12-18 мкм) с большим светлым слегка вогнутым ядром, в котором располагаются 1-2 ядрышка. Базофильная цитоплазма содержит умеренно развитую грЭПС, полисомы, митохондрии, центриоли и крупный комплекс Гольджи, от которого отделяются незрелые азурофильные гранулы. Промоноциты делятся и постепенно дифференцируются в моноциты.
Процесс преобразования монобластов в моноциты включает:
(1)дальнейшее увеличение размеров клетки преимущественно за счет нарастания объема цитоплазмы,
(2)снижение базофилии цитоплазмы,
(3)накопление в ней азурофильных гранул (лизосом),
(4)изменение формы ядра, которое становится бобовидным.
Моноциты покидают костный мозг вскоре после формирования, не образуя резервного костномозгового пула. Выделяясь в синусы красного костного мозга, они попадают в кровь, в которой циркулируют от 8 ч до 3-4 сут,
адалее через стенку сосудов мигрируют в ткани. Лишь около 5% моноцитов, имеющихся в организме, циркулирует в крови, остальные находятся во внесосудистом пуле. В тканях они превращаются в различные виды макрофагов (вместе с которыми образуют единую моноцитарно-макрофагальную систему),
атакже в дендритные антиген-представляющие клетки (см. главы 7 и 8). Развитие моноцитов стимулируется М-КСФ и ГМ-КСФ.
ЛИМФОЦИТОПОЭЗ
Лимфоцитопоэз - развитие лимфоцитов - происходит в красном костном мозге и различных лимфоидных органах и характеризуется их поэтапной миграцией (см. также главу 8).
- 267 -
Красный костный мозг содержит плюрипотентные СКК, которые дают начало частично детерминированным нолипотентным родоначальным клеткам лимфоцитопоэза (КОЕ-Л).
КОЕ-Л служит источником развития трех видов лимфоцитов – В- лимфоцитов, Т-лимфоцитов и NК-клеток, давая, соответственно, три вида унипотентных (коммитированных) родоначальных клеток - про- В-лимфоциты, протимоциты и (возможно) предшественник NK-клеток. Каждая из этих клеток детерминирована в направлении развития только одного вида лимфоцитов.
Последующее развитие Т- и В-лимфоцитов из родоначальных клеток связано с их пролиферацией и дифференцировкой и разделяется на две фазы: антиген-независимую и антиген-зависимую (см. главу 8).
1.Антиген-независимая фаза развития Т- и В-лимфоцитов
осуществляется в отсутствие антигенов в центральных органах кроветворения и иммуногенеза - тимусе и красном костном мозге (у птиц - фабрициевой сумке), соответственно. Ее наиболее важными этапами служат:
(1)миграция коммитированных предшественников из красно¬го костного мозга в центральные органы кроветворения и иммуногенеза. У
человека этот этап относится только к развитию Т-лимфоцитов, поскольку у него, как и всех млекопитающих, красный костный мозг одновременно выполняет роль центрального органа по отношению к В-лимфоцитам. Процесс миграции контролируется адгезивными взаи-модействиями между эндотелием сосудов тимуса и клетками-предшественниками, а также, возможно, секрецией клетками тимуса хемотаксических факторов.
(2)приобретение клетками набора рецепторов на плазмолемме: (а)
разнообразных специфических антиген-распознающих рецепторов (образуются
врезультате реаранжировки части генома, ответственной за антигенную специфичность); (б) ряда добавочных рецепторов, необходимых для взаимодействия с другими клетками;
(3)процесс отбора (селекции) клеток с необходимым набором рецепторов и гибель механизмом апоптоза лимфоцитов, не прошедших селекцию;
(4)выселение лимфоцитов (прошедших селекцию) в просвет сосудов и их миграция через кровоток из центральных органов крове –
- 268 -
творения и иммуногенеза в периферические с заселением их Т- и В- зависимых зон (содержащих преимущественно лимфоциты соответствующего вида). Поскольку мигрирующие клетки еще не встречались с антигенами, их называют наивными, или девственными. Направленной миграции способствуют специфические адгезивные взаимодействия между хоминг-рецепторами наивных Т- и В-лимфоцитов и лигандами (адрессинами) на поверхности эндотелия сосудов периферических лимфоидных органов (см. главу 7).
2. Антиген-зависимая фаза развития лимфоцитов происходит в периферических органах кроветворения и иммуногенеза (лимфатических узлах, селезенке, миндалинах, пейеровых бляшках, аппендиксе и др.). Она осуществляется в присутствии антигенов (представляемых АПК), сопровождается активацией и пролиферацией лимфоцитов и завершается формированием эффекторных и регуляторных Т-лимфоцитов, плазматических клеток, а также Т- и В-клеток памяти.
РАЗВИТИЕ В-ЛИМФОЦИТОВ
Последовательность стадий антиген-независимого развития В-
лимфоцитов представлена на рис. 9-6 (1). В ходе развития отмечается реаранжировка генома этих клеток, их выраженные функциональные и иммунофенотипические изменения, а также их некоторые морфологические преобразования.
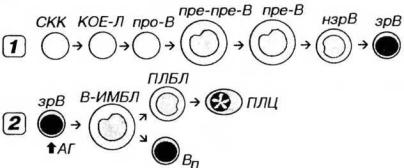
Рис. 9-6. Развитие В-лимфоцитов. 1 - антиген-независимое, 2 - антигензависимое. СКК - стволовая клетка крови, КОЕ-Л - колониеобразующая единица лимфоцитопоэза, про-В - про-В-лимфоцит, пре-пре-В - пре-пре-В- лимфоцит. пре-В - пре- В-лимфоцит, нзрВ - незрелый В-лимфоцит, зрВ - зрелый В-лимфоцит, АГ - антиген, В-ИМБЛ - В-иммунобласт, ПЛБЛ - плаэмобласт, ПЛЦ - плазмоцит, Вп - В-клетка памяти.
- 269 -
Про-В-лимфоцит соответствует стадии до реаранжировки генома, которая начинается на уровне пре-пре-В-лимфоцита. В цитоплазме пре-В- лимфоцита выявляется IgМ, но он отсутствует на его плазмолемме; для незрелого В-лимфоцита характерна экспрессия на плазмолемме. В зрелом В- лимфоците он экспрессируются совместно с IgD.
Развитие В-лимфоцитов сопровождается утратой одних клеточных маркеров и приобретением других, в частности, функционально важных в процессах адгезии, активации и рецепции цитокинов маркеров CD19, СD20, CD21, СD22, СD23 и СD40, рецепторов к комплементу, Fсфрагменту иммуноглобулинов (см.также главу 7). Развитие предшественников В- лимфоцитов протекает при контактных взаимодействиях со стромальными элементами и регулируется рядом цитокинов: ИЛ-1, -2, -3, -4, -5, -6 и -7.
Цитологические изменения на ранних стадиях лимфоцитопоэза не столь значительны, как функциональные и иммунофенотипические. Морфологически клетки, находящиеся на стадиях пре-пре- и пре-В- лимфоцита, соответствуют лимфобласту (большому лимфоциту), на стадии незрелого В-лимфоцита - среднему лимфоциту и на стадии зрелого В-лимфоцита - малому лимфоциту.
Последовательность стадий антиген-зависимого развития В-
лимфоцитов показана на рис. 9-6 (2). Покидая красный костный мозг, наивные (зрелые) В-лимфоциты, на поверхности которых экспрес-сируются IgM и IgD циркулируют в крови и попадают в периферические органы кроветворения и иммуногенеза. В этих органах они взаимодействуют с антигеном, соответствующим по специфичности их рецепторам, а также с Т-хелперами и активируются, подвергаясь бласттрансформации и превращаясь в течение 1-2 сут. в В-иммунобласты (см. главу 8). Последние спустя 3-4 сут. дают начало плазмобластам (далее дифференцирующимся в плазматические клетки) и В- клет кам памяти.
Созревание аффинности и соматические гипермутации. В особых структурах периферических органов кроветворения и иммуногенеза (герминативных центрах лимфатических узелков) с антигеном начально взаимодействуют В-лимфоциты, специфические иммуноглобулиновые рецепторы которых обладают по отношению к нему неодинаковой аффинностью (сродством). В дальнейшем, однако, происходит селекция В- лимфоцитов с высокоаффинными рецепторами, которые активно пролиферируют, тогда как клетки с низкоаффинными ре-
- 270 -