Материал: В-Л-Быков-Цитогогия_и_общая_гистология
Соотношение содержания в крови Т-лимфоцитов с маркерами CD4+ и
CD8+ оценивает общую активность иммунных реакций. При ВИЧ-инфекции, например, оно является важным диагностическим и прогностическим показателем. Снижение величины этого показателя с 2-3 (в норме) до 1 указывает на опасность иммуннодефицита (с вероятным развитием инфекций), а его падение ниже 0.5 обычно соответствует развернутой клинической картине СПИДа, осложненной тяжелыми инфекциями.
Т-киллеры (Тк), или Т-цитотоксические лимфоциты (ЦТЛ)
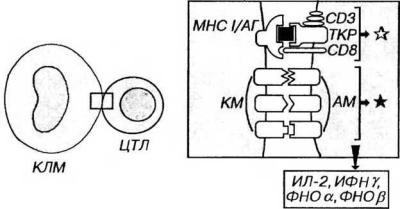
посредством ТКР и молекулы CD8 распознают эпитопы антигенов в комбинации с молекулами МНС I класса (рис. 8-4). Этот комплекс распознается Тк на АПК или на клетках-мишенях (зараженных вирусом или опухолевых). Тк живут меньше, чем Тх.
Рис. 8-4. Распознавание антигенов и активация Тк. Эпитоп антигена (АГ) в комплексе с молекулами МНС I класса (МНС I). который находится на поверхности клетки-мишени (КЛМ), распознается посредством ТКР и СD8 на мембране Тк, обеспечивая главный активационный сигнал (светлая звездочка). Дополнительная активация Тк достигается костимулирующим сигналом (черная звездочка) в результате взаимодействия костимулирующих молекул (КМ) на поверхности КЛМ с адгезионными молекулами (АМ) на поверхности Тк. При активации Тк выделяет ряд цитокинов.
Распознавание антигенов и активация Тк происходит под влиянием двух основных сигналов: (1) взаимодействия ТКР-СD8 на Тк с комплексом МНС I класса/эпитоп антигена на АПК или клетке-мишени; (2) воздействия цитокинов, выделяемых Тх, макрофагами и дендритными АПК.
- 231 -
Активированные Тк продуцируют ИФНγ и ИЛ-2, стимулируют представление антигенов, активируют клетки, участвующие в воспалении и, уничтожают клетки-мишени (зараженные вирусами, патогенными грибами и некоторыми бактериями), очищая от них организм. Их деятельность лежит также в основе противоопухолевого и трансплантационного иммунитета. Вещества, необходимые для уничтожения клеток-мишеней (перфорин, гранзимы и др.), накапливаются в образующихся 30-50 крупных (диаметром 0.5-2.0 мкм) цитоплазматических гранулах, покрытых мембраной и заполненных материалом, неоднородным по электронной плотности. По своему содержимому и морфологическим признакам эти гранулы сходны с гранулами NК-клеток.
При встрече с различными плетками Тк обследуют их поверхность в поисках антигенного эпитопа, который они способны распознать (в комплексе с молекулами МНС I класса). При обнаружении клетки-мишени зрелый Тк связывается с ней и оказывает на нее летальное цитотоксическое воздействие. После этого воздействия ("смертельного удара", или "смертельного поцелуя"), осуществляемого строго прицельно и не повреждающего соседние клетки. Тк отсоединяется от гибнущей клетки-мишени и ищет следующую жертву. Активность Тк находится под совместным контролем Тх и Тс; предполагают, что Тх действуют на Тк непосредственно, а Тс - косвенно (угнетая Тх).
Механизмы контактного цитотоксического действия Тк
("смертельного удара”), вызывающего гибель клетки-мишени, разрушают ее снаружи и изнутри (рис. 8-5):
1.Образование пор в плазмолемме клеток-мишеней. Тк вступает в контакт
склеткой-мишенью и в присутствии ионов Са2+ направленно (векторно) секретирует в межклеточное пространство особые белки перфорины, накопленные ранее в его цитоплазматических гранулах. Мономеры перфоринов встраиваются в качестве трансмембранных белков в плазмолемму клетокмишеней, а в дальнейшем образуют в ней агрегата в виде трансмембранных пор (рис. 8-6). Вследствие постоянного включения новых мономеров в агрегаты размеры пор растут, достигая 5-20 нм (внутренний диаметр наиболее крупных равен 10 нм). Поры, возникающие в плазмолемме при атаке Тк, очень сходны с образующимися при воздействии мембраyоатакуюшего комплекса компонентов комплемента. Формирование пор в плазмолемме приводит к нарушению осмотического равновесия клетки-мишени, ее набуханию и гибели. Образующиеся поры служат также проводниками веществ, вызывающих разрушение клеток-мишеней изнутри (см. ниже).
-232 -
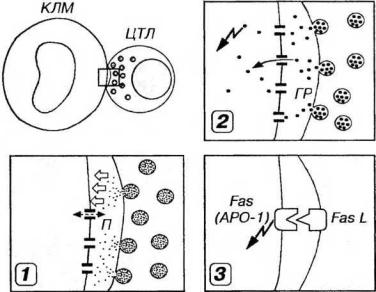
Рис. 8-5. Механизмы контактного действия цитотоксическогс лимфоцита (ЦТЛ) на клетку мишень (КЛМ). 1 - ЦТЛ секретирует в межклеточное пространство белки перфорины (П), которые встраиваются в плазмолемму КЛМ (белые стрелки) и образуют в ней трансмембранные поры, вызывающие нарушение осмотического равновесия КЛМ (пунктирная стрелка) и ее гибель (подробнее механизм образования пор показан на рис. 8-6). 2 - апоптоз КЛМ (стрелка в виде ’’молнии”) индуцируется в результате введения в ее цитоплазму через ранее образованные поры в плазмолемме ферментов гранзимое (ГР), синтезируемых и выделяемых ЦТЛ (стрелка) 3 - индук¬ия апоптоза КЛМ (стрелка в виде ’’молнии") в результате взаимодействия Fasлиганда (Fas-L) на поверхности Тк с антигеном Fas (АРО-1) на плазмолемме КЛМ. Указанные варианты взаимодействия не являются взаимоисключающими и осуществляются после того, как ЦТЛ посредством TKP и CD8 распознает комплекс антиген/ МНС I класса на поверхности КЛМ (механизм этого взаимодействия показан на рис. 8- 4).
2. Индукция апоптоза клеток-мишеней ферментами, введенными в их цитоплазму через поры в плазмолемме. Тк синтезируют и накапливают в гранулах ряд ферментов (из которых наиболее важна группа сериновых протеаз - гранзимов). Направленно выделяясь в межклеточное пространство при Са2+ - зависимом экзоцитозе гранул Тк, эти ферменты через образующиеся перфориновые поры проникают в цитоплазму клеток-мишеней и запускают программу апоптоза, вызывающую гибель этих клеток. При этом гранзимы действуют как прямо - на субстраты, расшепление которых непосредственно вызывает гибель клетки, так и косвенно, активируя цистеиновые протеазы семейства ICE (IL-1 Converting Enzyme - фермент, конвертирующий ИЛ-1), обусловливающие апоптоз.
- 233 -
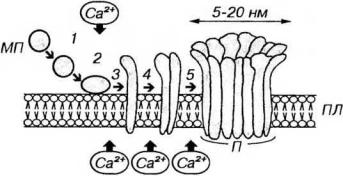
Рис. 8-6. Механизм образования пор в плазмолемме клетки-мишени при атаке Тк. 1 - мономеры перфорина (МП), выделяются Тх в пространство между ним и клеткой-мишенью; 2 - МП связываются с фосфолипидными головками плазмолеммы (ПЛ) клетки-мишени; 3 - МП претерпевают конформационные изменения и внедряются в липидный бислой; 4-5 - полимеризация МП с образованием поры (П) - агрегата МП цилиндрической формы, с просветом в центре. Все процессы, начиная со связывании МП с ПЛ и кончая образованием П, являются Са2+-зависимыми.
3. Индукция апоптоза клеток-мишеней, опосредованная поверхностными рецепторами на их плазмолемме. Происходит в результате Са2+-независимого взаимодействия антигена Fas (АРО-1, CD95) на плазмолемме клеток-мишеней с Fas-L (Fcis-лигандом - литическим эффектором из семейства ФИО) на поверхности Тк. Механизмы передачи сигнала с поверхности клетки на систему протеолитических ферментов семейства ICE, реализующих программу апоптоза, остаются неясными.
Взаимодействие Fas и Fas-L способствует также регуляции численности популяции самих Т-лимфоцитов. Активированные Т-лимфоциты резко усиливают выработку и экспрессию белка Fas (сначала неактивного) и Fas-L. По прошествии нескольких дней Fas активируется, связывается с Fas-L на этих же или других активировагнных лимфоцитах, вызывая запуск программы их апоптоза. Тем самым ограничивается срок существования активированных Тк, что предотвращает возможность избыточных повреждений тканей и развития хроническог о воспаления.
Гуморальное токсическое воздействие Тк может, наряду с описанными выше контактными взаимодействиями, вызывать гибель клетокмишеней. Оно осуществляется путем секреции Тк токсических меди-
- 234 -
аторов - лимфотоксина (ФНОР), ФНОα, ИЛ-1, ИФНγ, повышения концентрации активных радикалов кислорода, простагландина Е2, подавления выработки рецепторов.
Т-клетки ГЗТ (Тгзт) являются эффекторными клетками иммунных реакций гиперчувствительности замедленного типа. Они обладают поверхностным антигеном CD4 и экспрессируют ТКР совместно с молекулами МНС II класса. Тгзт распознают чужеродные антигены, преимущественно продуцируемые внутриклеточными микроорганизмами. В последние годы накоплены данные, свидетельствующие о том, что роль Тгзт фактически исполняют Тх1, которые и обеспечивают течение указанных реакций.
Активация Тгзт сходна с таковой Тх (происходит в результате взаимодействия с АПК) и сопровождается секрецией ИФНγ, (активирующею макрофаги), МИФ (фактора, ингибирующего миграцию), МХФ (хемотаксического фактора макрофагов), и других лимфокинов, которые воздействуют на макрофаги, клетки Лангерганса (а также другие АПК), Тк и нейтрофилы. Таким образом, Тгзт, в отличие от другого класса эффекторов клеточного иммунитета (Тк) сами не обладают непосредственным цитотоксическнм действием, однако обеспечивают защитные реакции, активно вовлекая в них клетки других типов
.
Проявлением реакций ГЗТ служат очаги хронического воспаления, состоящие преимущественно из макрофагов и лимфоцитов, часто формирующих характерные компактные структуры - гранулемы. Их основу образуют скопления макрофагов (возникающие под действием МХФ и МИФ), которые находятся в активироваггном состоянии (эффект ИФНγ).
В-ЛИМФОЦИТЫ И ПЛАЗМАТИЧЕСКИЕ КЛЕТКИ
Функция В-лимфоцитов:
1)распознавание антигенов иммуноглобулиновыми рецепторами,
2)обеспечение реакций гуморального иммунитета,
3)дифференцировка в плазмоциты - клетки, вырабатывающие иммуноглобулины.
Развитие В-лимфоцитов в красном костном мозге
В-лимфоциты у птиц (у которых они впервые были выявлены) развиваются из клеток-предшественнпков в особом лимфоидном органе –
- 235 -