Материал: В-Л-Быков-Цитогогия_и_общая_гистология
пептидных цепочек длиной 8-11 аминокислот, определяющих специфичность реакции антигена с антителом;
3)синтез гликопротеиновых молекул главного комплекса гистосовместимости, или МНС (от англ. Major Histocompatibility Complex),
называемого у человека также системой HLA (от англ. Human Leukocyte Antigens - антигены лейкоцитов человека); связывание синтезированных молекул МНС с эпитопами антигенов;
4)транспорт комплексов молекулы МНС/эпитоп антигена на поверхность АПК, где они представляются распознающим их лимфоцитам;
5)экспрессию на поверхности клетки (наряду с комплексом молекулы МНС/антиген) ряда добавочных (костимулирующих) молекул, усиливающих процесс взаимодействия с лимфоцитами; наиболее важной из них является В7;
6)секрецию растворимых медиаторов (преимущественно ИЛ-1), которые вызывают активацию лимфоцитов.
Синтез молекул МНС, процессинг и представление антигенов
Молекулы МНС I класса синтезируются в грЭПС (рис. 8-1), где они формируют комплексы с антигенами, являющимися эндогенно синтезированными молекулами (например, вирусными белками в инфицироваиных клетках или белками опухолевых клеток). Эти антигены, находящиеся в гиалоплазме, предварительно подвергаются расщеплению на короткие пептидные фрагменты (8-11 аминокислот) в особом протеолитическом АТФ-зависимом крупном белковом комплексе - протеасоме. Затем они транспортируются в просвет грЭПС с помощью специальных переносчиков в мембране - TAP-белков (от англ. Transporter for Antigen Presentation -
переносчик для представления антигена), где связываются с молекулами МНС I класса. Образованные комплексы транспортируется через комплекс Гольджи к плазмолемме и экспрессируются на ее поверхности.
- 221 -
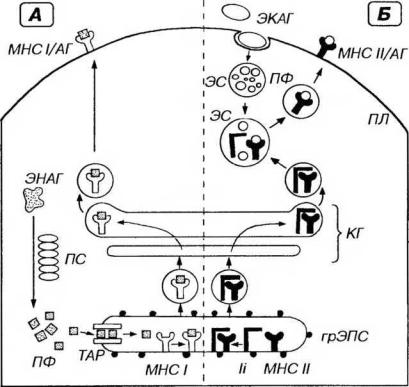
Рис. 8-1. Пути процессинга и представления антигенов. Антигены (АГ) - эндогенные (ЭНАГ) или экзогенные (ЭКАГ) - в цитоплазме АПК подвергаются процессингу, связываются с молекулами главного комплекса гистосовместимости (МНС) и экспрессируются на плазмолемме (ПЛ) в виде комплекса МНС/АГ. А. ЭНАГ в гиалоплазме расщепляются в протеасоме (ПС) на пептидные фрагменты (ПФ), которые с помощью TAP-белков (ТАР) переносятся в просвет грЭПС. Здесь они связываются с молекулами МНС I класса (МНС I), образуя комплексы МНС 1/АГ, транспортируемые через комплекс Гольджи (КГ) к ПЛ. Б. ЭКАГ захватываются механизмом эндоцитоза и подвергаются процессингу в эндосомах (ЭС) или лизосомах до ПФ. В грЭПС молекулы МНС II класса (МНС II) и инвариантные цепи (li) связываются с образованием комплекса МНС II/ li, который через КГ направляется к ЭС, содержащим ПФ. Комплекс МНС ll/li в ЭС диссоциирует, освобождая МНС II, связывающиеся с ПФ в комплекс МНС ll/АГ, который переносится к ПЛ.
Распределение молекул МНС I класса. Молекулы МНС I класса обнаруживаются на поверхности всех клеток и тромбоцитов (благодаря чему распознающие их цитотоксические лимфоциты имеют возможность уничтожения любых зараженных или опухолевых клеток).
- 222 -
Молекулы МНС II класса также образуются в грЭПС (см. рис. 8-1), где они формируют комплекс с так называемой инвариантной пептидной цепью (Ii). Предполагают, что она (1) препятствует связыванию молекул МНС II класса с эндогенными пептидами, (2) является переносчиком молекул МНС II класса и
(3) содержит кодирующие сигналы для последующего направления образованного комплекса в эндосому. Комплекс молекулы МНС II класса/цепь Ii через сеть транс-Гольджи в транспортных пузырьках направляется к эндосоме, содержащей экзогенные (например, бактериальные) антигены, предварительно подвергнутые процессингу. Пузырьки сливаются с эндосомой, внутри которой цепь Ii отсоединяется от молекул МНС II класса. Последние тут же образуют комплекс с антигенными пептидами, далее транспортируемый на поверхность клетки.
Распределение молекул МНС II класса. Гликопротеины МНС II класса экспрессируются на "профессиональных" АПК (макрофагах, дендритных АПК и В-лимфоцитах), что обеспечивает их взаимодействие с Т-хелперами (см. ниже). Изредка их экспрессия может индуцироваться на клетках других типов ("непрофессиональных" АПК).
Способность молекул МНС образовывать комплексы с антигенными пептидами различается у отдельных людей, что может оказывать влияние на особенности их иммунных реакций, в частности, на устойчивость к инфекциям.
Миграция дендритных АПК и их взаимодействия с другими клетками
1.Дендритные АПК, захватившие антиген, мигрируют из тканей в лимфатические капилляры, а оттуда - в Т-зависимые зоны регионарных лимфатических узлов, где они окончательно созревают и приобретают способность к представлению антигенов (в комплексе с молекулами МНС) лимфоцитам.
2.При встрече с Т-лимфоцитом, обладающим рецепторами к соответствующему антигену, дендритная АПК контактно взаимодействует с ним, активируя его и инициируя развитие иммунной реакции. Характер этой реакции зависит от природы молекул МНС, связанных с антигеном. Антигены, образующие комплекс с молекулами МНС I класса, распознаются лимфоцитами
споверхностными маркерами CD8 (см. ниже), а антигены, связанные с белками МНС II класса - лимфоцитами с фенотипом CD4 Особенности архитектоники лимфоидной ткани
- 223 -
и путей циркуляции лимфоцитов обеспечивают максимальное количество контактов лимфоцитов с потенциальным антигеном на поверхности АПК. Более того, установлено, что дендритные АПК вырабатывают хемокин, привлекающий Т-лимфоциты.
Полноценная функция дендритных АПК способствует эффективному и своевременному распознаванию микробных и опухолевых антигенов, что препятствует развитию инфекций и новообразований. Последние часто протекают на фоне сниженной активности АПК, поэтому стимуляция функции АПК рассматривается как перспективный метод иммунотерапии таких заболеваний.
Т-ЛИМФОЦИТЫ
Функции Т-лимфоцитов:
1)распознавание антигенных детерминант (эпитопов) - обеспечивается благодаря наличию на их плазмолемме Т-клеточных рецепторов (ТКР);
2)элиминация антигенов - осуществляется сенсибилизированными лимфоцитами (киллерами);
3)регуляция иммунного ответа - обеспечивается специальными субпопуляциями клеток, активирующих и угнетающих иммунные реакции;
4)регуляция гемопоэза (путем выделения гемопоэтических факторов);
5)регуляция пролиферации нелимфоидных клеток, участие в поддержании структурного гомеостаза (путем секреции цитокинов).
Цитофизиология Т-лимфоцитов и их участие в иммунных реакциях
Развитие Т-лимфоцитов в тимусе
Т-лимфоциты развиваются в пишу се (откуда и произошло их название) из предшественников (претимоцитов), поступающих в него из красного костного мозга. В тимусе Т-лимфониты (тимоциты) пролиферируют и дифференцируются, приобретая: (1) специфические Т-клеточные рецепторы (ТКР), распознающие разнообразные антигены; (2) поверхностные маркеры, которые характерны для субпопуляций лимфоцитов с определенными функциями.
- 224 -
Т-клеточные рецепторы обладают исключительным разнообразием, которое обусловлено относительной нестабильностью генома лимфоидных клеток-предшественников, в результате которой происходит постоянная перестройка (реаранжировка) их генетического аппарата, кодирующего специфичность ТКР (порядка 109 вариантов).
Поверхностные функциональные маркеры в соответствии с принятой международной номенклатурой обозначаются аббревиатурой CD (от англ. Cluster of Differentiation - группа дифференцировки) с добавлением цифровых и буквенных символов. С ТКР в мембране всех Т-лимфоцитов связан молекулярный комплекс CD3, который обеспечивает передачу сигнала в цитоплазму лимфоцита с ТКР после его взаимодействия с антигеном.
Незрелые Т-клетки составляют лишь несколько процентов от общего числа клеток тимуса и характеризуются фенотипом CD4- CD8-. Созревая, они превращаются в клетки с ТКР и поверхностным маркером CD4 или CD8. Такие клетки, наиболее многочисленные в тимусе, занимают его кору, в которой они подвергаются положительной и отрицательной селекции.
Процесс отбора (селекции) Т-лимфоцитов внутри тимуса приводит к гибели большей части (более 90%) образовавшихся в нем клеток механизмом апоптоза. При этом погибают тимоциты, не обладающие необходимыми рецепторами (и поэтому бесполезные) или имеющие рецепторы к антигенам собственного организма (и поэтому опасные).
Миграция Т-лимфоцитов из тимуса и их циркуляция в организме
Прошедшие селекцию Т-лимфоциты из тимуса поступают в кровь, где они составляют 70-80% всех лимфоцитов и циркулируют в ней в течение различного времени. Покидая сосудистое русло через стенку его особого участка (посткапиллярных венул с высоким эндотелием), они заселяют так называемые Т-зависимые зоны периферических органов иммунной системы - лимфатических узлов, селезенки, миндалин, аппендикса, пейеровых бляшек и др. (см. главу "Иммунная система" в курсе частной гистологии), откуда через лимфу могут вновь попадать в кровь. Лимфоцита из сосудистого русла направляются также в ткани органов, не относящихся к иммунной системе. При этом они мигрируют через стенку мелких кровеносных сосудов (посткапиллярных венул) с обычным (плоским) эндотелием. До встречи с антигенами лимфоциты называют "наивными" (не имевшими "опыта" взаимодействия с антигеном), или виргильными (девственными, от лат. virgo - дева).
- 225 -