Материал: Учебное пособие ЭТМ
|
|
|
|
|
|
|
Таблица 5.3 |
|
|
Химический состав некоторых марок меди |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
Содержание, % |
|
|
Марка |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
М00б |
М0 |
|
М1 |
… |
|
М4 |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
Cu |
|
> 99,97 |
> 99,95 |
|
> 99,9 |
… |
|
> 99,0 |
|
|
|
|
|
|
|
|
|
O |
|
< 0,001 |
< 0,02 |
|
< 0,05 |
… |
|
< 0,15 |
|
|
|
|
|
|
|
|
|
Для получения высокой электропроводности и пластичности меди ее необходимо отжечь в среде водорода. После такого отжига медь охрупчивается («водородная болезнь меди»), что является следствием взаимодействия водорода с кислородом, содержащимся в меди. Поэтому отжиг надо производить в средах, не содержащих водород или углеводороды, лучше всего в инертной атмосфере. Из меди, отожженной в бескислородной среде, можно вытянуть провод диаметром несколько мкм.
Электропроводность неотожженной меди меньше, чем отожженной.
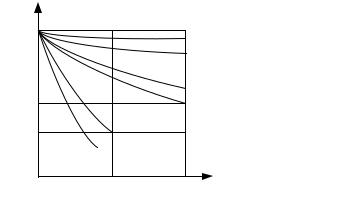
Электропроводность меди изменяется в зависимости от примесей и от их количества (рис. 5.10).
Рис. 5.10. Зависимость удельной электропроводности γ меди от содержания примесей (% масс.):
1 − Ag; 2 − Cd; 3 − Ni; 4 − Al; 5 − Fe; 6 − P
Таким образом, к достоинствам меди относятся:
высокая электропроводность и теплопроводность: 406 Вт/(м·К);
128

высокая стойкость к окислению (в 3 раза выше, чем у железа) и
к воде; |
|
|
|
относительно |
высокая |
механическая |
прочность |
(σр МТ ≈ 500 МПа);
технологичность (легко подается ковке и вытягиванию); легко поддается пайке обычными оловянно-свинцовыми при-
поями.
Недостатки меди:
дефицитность: в Земной коре порядка 0,01 %, следовательно, высокая и постоянно растущая стоимость;
медь взаимодействует с кремнием, поэтому ее следует ограниченно применять в интегральных схемах;
медь реагирует с газообразной серой, имеющейся в атмосфере больших городов (следствие работы промышленности и автотранспорта).
Применение меди:
для монтажных проводов; для радиочастотных, телевизионных и телефонных кабелей;
для изготовления генераторов, излучающих СВЧ колебания (клистрон, магнетрон);
для изготовления анодов в рентгеновских трубках.
Сплавы меди. Цель создания сплавов из меди, в первую очередь, повышение механической прочности. Наиболее распространенными сплавами меди являются:
бронза; латунь;
медно-никелевый сплав.
Современная литейная бронза имеет следующий состав:
Cu + ≤ 5 % Sn + ≤ 10 % Zn + 2 % Pb. Механические свойства
бронзы: |
предел |
механической |
прочности |
|
при |
разрыве |
|
σр = 800 – 1100 |
МПа; относительное удлинение ( l |
) бронзы меньше, |
|||||
|
|
|
|
l |
|
|
|
чем меди. |
Электрические свойства: удельное |
электрическое |
|||||
129
сопротивление при 20 ° С равно (10 – 26)·10 - 8 Ом·м, т. е. больше, чем у меди.
Бронза бывает по химическому составу разных типов. Некоторые из бронз перечислены ниже:
оловянная бронза (Cu + Sn);
бериллиевая бронза (Cu + Be) применяется для изготовления электрических контактов, так как хорошо пружинит и не искрит;
кадмиевая бронза (Cu + Cd). Эта бронза так же, как и бериллиевая, используется в электрических контактах.
Применение бронзы:
изготовление конструкционных изделий с высокой механической прочностью, в том числе коллекторных пластин для электрических машин и пружинящих электрических контактов;
изготовление скульптур, колоколов и различных предметов интерьера.
Латунь — сплав, состоящий из Cu и (10 - 40) % Zn (обычно меди в латуни содержится порядка 65 %). Когда меди в соединении больше 80 %, то такой сплав называется «томпáк».
В латунь вводят следующие добавки: порядка 1 – 2 % алюминия (алюминиевая или морская латунь), олово, свинец и др.
Механические свойства латуни: предел механической прочности на разрыв σр = 800 – 900 МПа.
Электрические свойства: удельное электрическое сопротивление при 20 ° С равно (4 – 33)·10 - 8 Ом·м.
Латунь, несмотря на высокую прочность, обладает относительно высокой пластичностью, поэтому из нее делают фасонные изделия (изделия сложной конфигурации), например, СВЧ волноводы, предназначенные для передачи электромагнитной энергии сверхвысокой частоты. СВЧ волноводы могут быть прямоугольной, круглой и Н-образной формы.
Медно-никелевые сплавы обладают высокой коррозионной стойкостью. В то же время их удельное электрическое сопротивление
130
много больше, чем у меди, бронзы и латуни. Медно-никелевые сплавы применяются для изготовления: резисторов, термопар, сплавов с нулевым коэффициентом термического расширения, медицинских инструментов и посуды.
Медь и никель входят в состав таких широко известных соединений, как:
Cu + Zn + (10 – 20) % Ni — « нейзильбер» (от немецких слов «но-
вое серебро»);
Cu + (18 – 20) % Ni — « мельхиор» (производное от имени двух французских изобретателей, создавших этот сплав).
К другим сплавам меди относятся:
Медно-вольфрамовый сплав (27 % Сu + 70 % W + 3 % Ni). Этот сплав применяется в высоковольтных и сильноточных коммутирующих устройствах, при разрыве таких цепей возникает электрическая дуга. Здесь медь обеспечивает высокую электропроводность и совместно с никелем стойкость к воздействию кислорода, а вольфрам высокую стойкость к электрической дуге.
Сплав, состоящий из меди и серебра, а также из меди, серебра и золота. Эти сплавы применяются для слаботочных контактов. В этих сплавах медь обеспечивает высокую механическую прочность, а серебро и золото — высокую электропроводность и стойкость к воздействию кислорода.
Сплавы для пайки при повышенных температурах («твердые припои»), например, сплав марки ПСр70, содержащий 70 % Ag, 16 %
Cu и 4 % Zn.
Алюминий. В таблице Д. И. Менделеева алюминий (Al) находится под № 13 в III группе.
Физические свойства: температура плавления 657 ° С, плотность 2,7 г/см3 (в 3,3 раза меньше, чем у меди). Чистый алюминий — металл голубоватого цвета, алюминий с примесями имеет белый цвет.
По распространенности элементов в Земной коре занимает третье место (порядка 8 %), среди металлов — первое место. Минералы,
131

содержащие алюминий — бокситы, каолины, нефелины, глины (Al2O3 + SiO2 + R2O + H2O + примеси, где R — щелочноземельные металлы, такие как: литий, натрий, калий и т. д.). В настоящее время наиболее широко в качестве исходного сырья при производстве алюминия используют бокситы.
Впервые чистый алюминий выделил Х. Эрстед в 1825 году. Промышленное производство было начато в 1886 году при помощи электролиза. В СССР алюминий впервые был получен на заводе «Красный Выборжец» в 1928 году из бокситов Бокситогорского месторождения по технологическому процессу, разработанному учеными металлургического факультета Политехнического института.
Технология получения алюминия включает следующие стадии: Первая стадия — получение «технического глинозема» из бок-
ситов.
Боксит  Al2O3 («технический глинозем»).
Al2O3 («технический глинозем»).
Боксит содержит 40 – 60 % Al 2O3, а также оксиды кремния, железа и титана. Начальный этап процесса химического обогащения боксита — нагрев его в автоклаве совместно с едким натром (NaOH). Затем охлаждение и осаждение гидрооксида алюминия, из которого при прокаливании получают «технический глинозем» (Al2O3).
Вторая стадия — получение чистого алюминия. Al2O3 + Na3AlF6 (криолит)  расплав
расплав
 Al↓ (осажденный на графитовом электроде).
Al↓ (осажденный на графитовом электроде).
В РФ выпускают тринадцать марок алюминия, подразделяемых на три класса (алюминий — особо чистый, химически чистый и технически чистый) и содержащих от 99,999 % до 99,0 % Al. Алюминиевая фольга содержит более 99,95 % алюминия, алюминиевый провод — более 99,5 %, при этом диаметр провода лежит в интервале от 80 мкм до 10 мм. Алюминий, подвергнутый зонной плавке и используемый в полупроводниковой технике, имеет чистоту 99,9999 %.
132