Материал: Учебное пособие ЭТМ
Электропроводность неотожженного алюминия меньше, чем отожженного. При 20 ° С ρ отожженного алюминия равно 2,6·10- 8 Ом·м и 2,8·10- 8 Ом·м при содержании Al не менее 99,997 % и 99,5 % соответственно. При температуре плавления Тпл = 657 ° С величина ρ возрастает приблизительно на один порядок. Особенности температурной зависимости электропроводности алюминия:
при 20 ° С электропроводность алюминия меньше, чем электропроводность меди, но при Т менее 80 К, наоборот, γAl больше γCu;
алюминий в отличие от меди имеет сверхпроводимость при Тс
меньше 1,2 К (рис. 5.11).
ρ
Рис. 5.11. Температурная зависимость удельного сопротивления алюминия
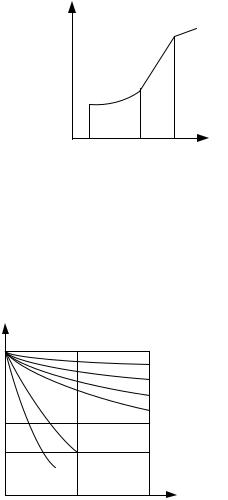
Зависимость электропроводности алюминия от содержания примесей приведена на рис. 5.12.
γ
100%
1
2
3
4
50%
30%
5
6
Содержание примесей
0,25% 0,5%
Рис. 5.12. Зависимость удельной электропроводности γ алюминия от содержания примесей (% масс.):
1 − Ni; 2 − Fe; 3 −Cu; 4 − Ag; 5 − Ti; 6 −Mn
133
Алюминий на воздухе сразу окисляется и на его поверхности образуется тонкий оксидный слой (Al2O3). Пленка очень плотная и дальнейшее окисление не происходит, т. е. практически, можно считать, что, алюминий устойчив к кислороду. Толщина пленки Al2O3 может быть искусственно увеличена до 30 – 40 мкм. Искусственное увеличение толщины пленки производится методом электролитического анодирования в слабом растворе серной и щавелевой кислоты (Н2С2О4) при 20 ° С и напряжении 10 – 15 В. Этот способ используется для изготовления оксидных конденсаторов.
Алюминий практически не реагирует с водой и серой, но реагирует с серной кислотой.
К достоинствам алюминия относятся:
высокая электропроводность и теплопроводность (218 Вт/(м·К)); высокая стойкость к окислению; низкая плотность, в 3,3 раза меньше, чем у меди (масса медного
провода будет в два раза выше, чем масса алюминиевого при одном и том же сопротивлении, но диаметр алюминиевого провода будет в 1,3 раза больше, чем диаметр медного провода);
легко подвергается анодированию (используется для создания оксидных конденсаторов и цветных покрытий на алюминиевых конструкциях в строительстве);
недефицитность. Недостатки алюминия:
низкая механическая прочность; алюминий нельзя подвергнуть пайке и сварке обычными спосо-
бами (с помощью оловянно-свинцовых припоев); алюминиевые провода требуют большого количества электри-
ческой изоляции, (при одном и том же токе диаметр алюминиевого провода в 1,3 раза больше медного).
Применение алюминия: для монтажных проводов;
для силовых электрических кабелей;
134
для изготовления оксидных конденсаторов; для изготовления CD- и DVD-дисков;
в ЛЭП в композиции со стальным проводом.
Сплавы алюминия. Цель создания сплавов из алюминия это, как и в случае сплавов меди, повышение механической прочности. Сплавы делятся на литейные и деформируемые (способные растягиваться). Ассортимент алюминиевых сплавов достаточно обширный. Поэтому ниже приведены только два наиболее используемых сплава.
Дюралюминий (дюраль). Название сплава произошло от лат. «durus» — твердый. Дюраль состоит из Al, меньше 5 % Cu и меньше 2,5 % Mn. Предел механической прочности на разрыв дюраля составляет 300 МПа, но электропроводность дюраля много меньше, чем алюминия.
Алдрей. Данный сплав состоит из Al, 1 %(Mg + Si) и (0,2 – 0,3) %Fe. Предел механической прочности на разрыв алдрея составляет 350 МПа. Удельное электрическое сопротивление при 20 ° С равно 3,2·10- 8 Ом·м, то есть этот сплав имеет относительно высокую электропроводность при относительно высокой механической прочности.
Применение алюминиевых сплавов: авиастроение; судостроение;
автомобильная промышленность; строительство;
емкости для жидкостей (например, канистры для бензина). Серебро. В таблице Д. И. Менделеева серебро (Ag) находится
под № 47 в Iб группе. Серебро входит в группу «благородных метал- лов», то есть таких металлов, которые характеризуются высокой коррозионной устойчивостью (в первую очередь, к кислороду и воде). Распространенность серебра в Земной коре порядка 10- 5 %. Этот металл встречается в виде самородков, поэтому известен очень давно
135
(например, в 7 веке до н. э. из серебра делали монеты). Кроме самородков, серебро встречается в виде сульфидных соединений (Ag + S).
В настоящее время технология получения серебра из сульфидных материалов основана на обработке минералов цианидами (растворение в водном растворе синильной кислоты) с последующим электролизом. Физические свойства серебра: температура плавления — 961 ° С, плотность — 10,4 г/см3. Серебро — металл серебристого цвета, обладающий высокой отражательной способностью.
Электрические и теплофизические свойства серебра (при 20 ºС): удельное электрическое сопротивление равно 1,6·10- 8 Ом·м; коэффициент теплопроводности равен 453 Вт/(м·К). По электропроводности и теплопроводности серебро занимает первое место среди металлов.
Предел механической прочности серебра на разрыв равен 200 МПа. Брусок серебра можно раскатать до толщины 0,25 мкм.
При температуре плавления 961 ° С удельное электрическое сопротивление равно 15·10-8 Ом·м.
Серебро до 250 ° С не реагирует с кислородом, при бó льшей температуре наблюдается слабое взаимодействие. С водой серебро не реагирует. С серой серебро взаимодействует, образуя сульфид серебра (Ag2S). Также серебро взаимодействует с концентрированными кислотами (серной и азотной).
К достоинствам серебра относятся:
самая высокая электропроводность и теплопроводность; высокая стойкость к окислению и к воде; высокая отражательная способность.
Недостатки серебра:
дефицитность, предопределяющая относительно высокую стоимость;
взаимодействует с серой (на поверхности серебра образуется темный налет — слой Ag2S);
относительно невысокая механическая прочность.
136
Серебро широко используется в электротехнике и радиотехнике, а также и в других областях техники:
электрические контакты, выполненные из сплавов серебра (Ag + Cu и Ag + Cu + Au), в которых медь обеспечивает высокую механическую прочность, а серебро и золото высокую электропроводность и стойкость к воздействию кислорода;
серебряный припой (относится к группе твердых припоев, у которых рабочая температура превышает 500 ° С). Эти пропои содержат серебро, медь и цинк. Существуют, например, следующие марки припоев (ПСр12, ПСр30, ПСр70), где цифрами обозначается процентное содержание серебра;
серебряные пасты для металлизации керамики, слюды, стекол с целью создания металлических электродов, в частности, для изготовления резисторов;
проводники в интегральных схемах; микропровод (диаметром более 0,25 мкм); рефлекторы и зеркала; фотография; медицина; ювелирные изделия.
Золото. В таблице Д. И. Менделеева золото (Au) находится под № 79 в Iб группе.
Распространенность золота в Земной коре порядка 5·10- 7 %. Этот металл встречается в виде самородков в горных породах (прожилки в кварце), а также в океанской и морской воде. В одной тонне морской воды содержится в среднем около 0,02 мг золота. Общее количество золота в океанской и морской воде в виде хлористых и бромистых соединений составляет 27 млн. тонн. Золото попадает в мировой океан, в первую очередь, с помощью рек, размывающих сушу. Например, воды реки Амур выносят в океан примерно 8 тонн золота в год. Однако, добыча золота из морской (океанской) воды в настоящее время является нерентабельной.
137