Материал: Теоретические основы теплотехники 1
21
|
v v R |
T |
R |
T |
, |
|
|
p |
p |
||||
|
|
|
|
|
||
где R R 8314 |
Дж/(кмоль К) – универсальная газовая постоянная. |
|||||
|
|
|
||||
Уравнения состояния для 1 кмоля и для G кмолей идеального газа |
||||||
имеют следующий вид: |
|
|
|
|
|
|
для 1 кмоля газа |
pv RT ; |
|
|
|||
(31)
(32)
для
G
кмолей газа
|
|
|
|
|
|
||
pV GRT . |
(32а) |
||||||
Эти уравнения называются уравнениями Клапейрона – Менделеева.
Закон Джоуля определяет, что внутренняя энергия идеального газа за-
висит только от температуры
u u( T ) ;
Реальные газы
|
u |
|
|
|
|
|
v |
T |
|
|
0
.
(33)
Отсутствие теоретически обоснованного единого уравнения состояния реального газа привело к выводу большого количества эмпирических и полу-
эмпирических уравнений состояния, справедливых для отдельных газов в ограниченном диапазоне изменения параметров их состояния.
Чем точнее уравнение, тем больше (как правило) оно содержит инди-
видуальных констант. Так, в известном уравнении состояния Ван-дер-Ваальса содержится две константы, а в более точных уравнениях число констант доходит до десяти и более.
В инженерных расчетах часто пользуются уравнением состояния иде-
ального газа с введением в него поправочного коэффициента (z), называемо-
го коэффициентом сжимаемости
22
pv zRT .
(34)
Коэффициент сжимаемости (z) учитывает различие между идеальным и реальными газами (для идеального газа z = 1).
Коэффициент сжимаемости является функцией давления, температуры и зависит от природы газа.
Для обобщения данных по коэффициентам сжимаемости различных газов был использован принцип «соответственных» состояний, сформулиро-
ванный Ван-дер-Ваальсом. Принцип «соответственных» состояний утвер-
ждает, что критическое состояние действительно является одинаковым для всех веществ.
|
|
|
|
|
|
|
|
|
2 |
p |
|
|
|
|
p |
|
|
|
|
|
|
|
|
В критической точке для всех веществ r = 0, |
|
|
|
|
|
0 |
, |
|
0 |
, |
|||||
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
T |
2 |
v |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
v |
|
v |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
p |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
0 |
. Вещества находятся в соответственных состояниях при одина- |
|||||||||||||
|
v |
2 |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
ковом удалении от критической точки.
Степень удаления от критической точки определяется с помощью приведенных параметров:
|
приведенного давления |
|
p |
; |
|
||
p |
|
||||||
|
|
|
|
|
|
||
|
|
|
|
к |
|
|
|
|
приведенной температуры |
|
T |
; |
|||
T |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
к |
|
|
|
приведенного объема w |
|
v |
. |
|
|
|
v |
|
|
|||||
|
|
|
|
|
|||
|
|
|
к |
|
|
|
|
Уравнение состояния, записанное в виде F ( w, , ) = 0, называется при-
веденным уравнением состояния. Оно не содержит индивидуальных кон-
стант вещества.
Состояния вещества, в которых они имеют одинаковые и называ-
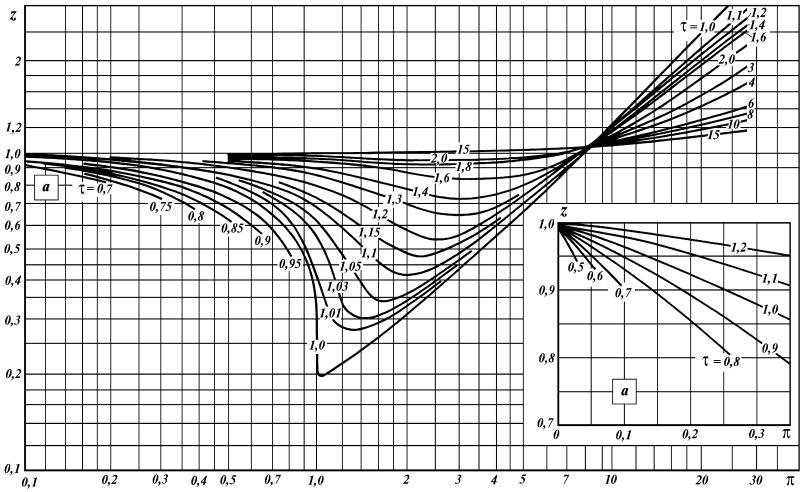
ются соответственными. Зная параметры и по данным рис. 4 определя-
ется коэффициент сжимаемости z.
23
Рис. 4. Зависимость коэффициента сжимаемости углеводородных газов от приведенных параметров
24
4. Первое начало термодинамики
Первое начало термодинамики – это количественное выражение закона сохранения и превращения энергии.
Закон сохранения и превращения энергии является универсальным за-
коном природы и применим ко всем явлениям. Он гласит: «запас энергии изолированной системы остается неизменным при любых происходящих в системе процессах; энергия не уничтожается и не создается, а только пе-
реходит из одного вида в другой».
При построении термодинамики принимается, что все возможные энергетические взаимодействия между телами сводятся лишь к передаче теплоты и работы. При этом необходимо отметить, что в отличие от тепло-
обмена, работа как форма энергетического взаимодействия в условиях обра-
тимого течения явлений допускает возможность своего полного превраще-
ния в другие виды энергии.
Первое начало термодинамики как математическое выражение закона сохранения и превращения энергии
В силу того, что теплообмен и передача работы являются единствен-
ными формами передачи энергии, исходное выражение первого начала тер-
модинамики по внешнему балансу теплоты и работы формулируется следу-
|
|
|
ющим образом: «количество теплоты, полученной системой извне ( Q1,2 ), |
||
идет на изменение внутренней энергии системы ( U1,2 |
U2 U1 ) и на вы- |
|
полнение внешней работы ( L1,2 )» |
|
|
|
* |
(35) |
Q1,2 U2 U1 |
L 1,2 , |
|
U1,2 Q1,2 |
L*1,2 . |
(36) |
В дифференциальной форме уравнение (35) может быть представлено следующим образом:
25
|
|
L |
|
* |
= dU + |
* |
. |
Q |
|
(37)
Уравнения (35), (36), (37) являются математическим выражением пер-
вого начала термодинамики по внешнему балансу теплоты и работы.
В термодинамике приняты следущие знаки при определении работы и теплоты в уравнениях первого начала термодинамики: если работа выполняется телом, то она положительная; если работа подводится к телу, то она отрицательная. Если теплота сообщается телу, она имеет положительное
значение; если теплота отводится от тела, она имеет отрицательное значение.
|
L |
|
Работа необратимых потерь |
** |
, связанная с затратами энергии на |
|
преодоление сил трения, удары, завихрения превращается в теплоту внут-
реннего теплообмена ( Q |
|
) |
|
Q**
|
L |
= |
** |
|
.
(38)
Следовательно, полное количество равно сумме теплоты, подведенной извне обмена Q**
теплоты |
Q , полученное телом, |
|
* |
, и теплоты внутреннего тепло- |
|
Q |
||
Q
= Q*
+ Q**
.
(39)
Подставив значение следующие соотношения:
L*
и
Q*
в исходное уравнение (37), получим
Q Q Q dU L ; |
(40) |
Q1,2 Q1*,2 Q1**,2 U 2 U1 L1,2 . |
(41) |