Материал: Теоретические основы теплотехники 1
16
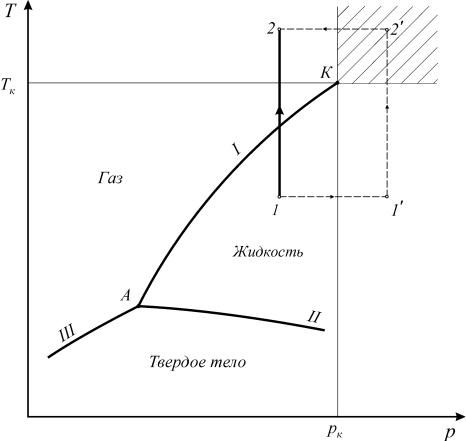
яний чистого вещества (рис.3).
Рис. 3. Диаграмма фазовых состояний чистого вещества
Линии фазовых превращений (испарение - I, плавление - II,
сублимации - III) отображают термодинамическое равновесие двухфазных систем и делят диаграмму на области различных агрегатных состояний.
Фазами системы называются области, ограниченные поверхностями раздела. На линиях фазовых превращений существует однозначная зависи-
мость между давлением и температурой. Эти линии пересекаются в тройной точке, где вещество одновременно находится в трех агрегатных состояниях.
Параметры тройной точки принадлежат к термодинамическим константам вещества.
Энергетической границей между жидкостью и паром является тепло-
17
та испарения, а между твердым телом и жидкостью – теплота плавления.
Так как процессы испарения и плавления протекают при постоянной темпе-
ратуре, то теплоты испарения, плавления и сублимации есть теплоты изо-
термических превращений. Теплота фазового перехода обозначается симво-
лом r .
Наибольший интерес для проведения технических расчетов в термоди-
намике представляют газ и жидкость. При увеличении давления термодина-
мическое различие в их свойствах заметно уменьшается и в критической
точке исчезает полностью.
Критические параметры являются важнейшими термодинамическими
постоянными вещества. Понятие критической температуры введено
Д. И. Менделеевым. Критическая температура Tк – это температура, при ко-
торой и выше которой газ никаким сжатием не может быть переведен в жид-
кое состояние. Критическое давление pк – это такое давление, при котором и выше которого жидкость невозможно перевести в газообразное состояние,
а критический объем представляет собой максимальный объем данного ко-
личества вещества в жидком состоянии.
В закритической области ( p pк ; T Tк ) вещество может находиться только в однофазном состоянии. Переход из состояния 1 в состояние 2 воз-
можен кратчайшим путем по линии 1-2. Можно этот переход осуществить через закритическую область, то есть без изменения агрегатного состояния,
например по линии 1 1 2 2 (рис. 3).
Условным признаком непрерывности однофазного состояния вещества является возможность перехода его из любого однофазного исходного состо-
яния в другое однофазное состояние путем непрерывных изменений пара-
метров состояния, минуя фазовые энергетические барьеры.
Поэтому в принципе, для простых тел (однородных систем) должно существовать единое уравнение состояния F( p, v, T ) 0 , описывающее лю-
18
бое однофазное состояние вещества. Такого уравнения пока еще не получе-
но. Ниже рассмотрим уравнения состояния идеальных и реальных газов.

19
3. Законы и уравнение состояния идеальных газов. Уравнения состояния реального газа
Идеальные газы
Идеальными называются газы, у которых молекулы представляют со-
бой материальные точки и между молекулами отсутствуют силы взаимодей-
ствия.
При относительно низком давлении и высоких температурах реальные газы имеют малую плотность и, с известным допущением, могут рассматри-
ваться как газы идеальные.
Законы идеальных газов были установлены в XVII - XIX столетиях ис-
следователями, изучавшими экспериментальным путем поведение газов при давлениях, близких к атмосферному.
Закон Бойля (1662 г.) – Мариотта (1676 г.): произведение абсолютного давления на удельный объем идеального газа при неизменной температуре есть величина постоянная, т.е. произведение абсолютного давления на удельный объем идеального газа зависит только от температуры газа:
при t = idem |
рv= idem. |
(24) |
Закон Гей Люссака (1802 г.) – относительное расширение идеальных газов при неизменном давлении (p=idem) пропорционально повышению тем-
пературы
при
t |
0 C |
0 |
|
|
v v0 |
( t t |
|
), |
||||
|
|
0 |
||||||
|
v0 |
|
|
|
|
|||
|
|
|
|
|
|
|||
0 |
|
1 |
, К |
1 |
; |
v v0 ( 1 0t ) , |
||
|
|
|||||||
273,15 |
|
|||||||
|
|
|
|
|
|
|
||
(25)
(26)
где v – удельный объем газа при температуре t и давлении p; v0 – удельный объем газа при температуре t0 = 0 0C; 0 – температурный коэффициент объ-

20
емного расширения идеальных газов при t0 = 0 0C, сохраняющий одно и то же значение при всех давлениях и одинаковый для всех идеальных газов.
Из сопоставления этих законов выводится уравнение состояния иде-
альных газов - уравнение Клапейрона (1834 г.):
для
для
1 кг газа
G кг газа
pv RT ;
pV GRT
,
(27)
(28)
где
за
R
– характеристическая постоянная газа; Т – абсолютная температура га-
T |
pv |
t |
1 |
|
R |
|
|||
|
|
|||
|
|
|
0 |
( t 273,15
),
K
.
(29)
Продифференцировав уравнение Клапейрона при постоянном давле-
нии, получим: l p pdv RdT .
Отсюда
|
l |
|
|
|
R |
p |
. |
(30) |
|
dT |
||||
|
|
|
Это значит, что характеристическая газовая постоянная (R) – это тер-
модинамическая работа 1 кг газа в изобарном процессе (p= idem) при измене-
нии температуры газа на один градус.
Закон Авогадро (1811 г.) – объем одного киломоля идеального газа не зависит от его природы и вполне определяется параметрами состояния газа
v f ( p,t ) .
Молярный объем идеального газа с использованием уравнения Кла-
пейрона определяется из соотношения