Материал: Теоретические основы теплотехники 1
11
Удельная потенциальная работа в элементарном процессе
ляется по формуле
w |
W |
vdp |
|
||
|
G |
. |
|
|
w
опреде-
(12)
Для определения интегральных значений полной (W1,2 ) или удельной
( w1,2 ) работы надо знать уравнение процесса изменения состояния рабочего тела ( p,V ) 0 или его графическое изображение в диаграммах состояния
р–V или р–v.
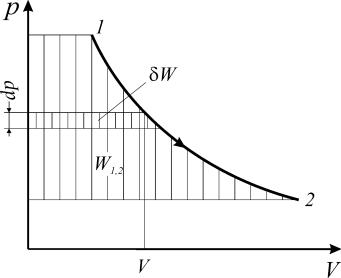
Как следует из соотношений (11), (12), работа определяется в коорди-
натах р–V площадью между кривой процесса и осью абсцисс независимо от вида рабочего тела и его свойств (рис. 2).
Рис. 2. Потенциальная работа обратимого изменения давления
В частном случае для изохорного процесса (v = idem) интегральные значения полной и удельной потенциальной работы определяются по следу-
ющим соотношениям:

12
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
W |
|
|
Vdp V ( p p |
2 |
); |
|
|
|
|
|
|
|
|
|
|
|
1,2 |
|
|
1 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
w1,2 |
vdp v ( p1 |
p2 ). |
|
|
|
(13) |
|
|
|
||
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
Потенциальная работа считается положительной при снижении давле- |
|||||||||||||||
|
|
|||||||||||||||
ния ( p2 p1 ) и отрицательной – при повышении давления ( p2 |
p1 ). |
|
||||||||||||||
|
Потенциальная работа в обратимом процессе ( W ) есть сумма эффек- |
|||||||||||||||
тивной работы W |
* |
и необратимых потерь работы |
W |
** |
|
|
|
|||||||||
|
|
|
|
|
||||||||||||
W
= |
W |
|
|
||
|
|
|
W |
+ |
** |
|
.
(14)
|
|
|
|
|
|
|
|
|
|
W |
|
|
|
|
|
Необратимые потери потенциальной работы ( |
|
** |
) превращаются в |
||||||||||
|
|
|
||||||||||||
теплоту внутреннего теплообмена. |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
L |
|
|
|
|
|
|
|
|
Эффективная термодинамическая работа ( |
|
* |
) простого тела в замкну- |
||||||||||
|
|
|
||||||||||||
том пространстве и эффективная потенциальная работа ( W |
* |
) потока непо- |
||||||||||||
|
||||||||||||||
|
|
|
|
|
* |
|
или |
* |
|
|
||||
средственно передаются внешней системе ( Lcz |
Wcz ) и используются |
|||||||||||||
для изменения энергии внешнего положения тела (dEcz) |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
* |
* |
W |
* |
* |
|
|
|
|
|
(15) |
|
|
|
|
|
= Lcz + dEcz; |
|
= Wcz + dEcz . |
|
|
|
|
|
|
|
|||
В условиях механических процессов (dEcz=G cЕ dcЕ+G g dz) уравнение распределения термодинамической и потенциальной работ формулируется следующим образом:
|
c |
2 |
|
|
|
|
|
|
|
|
|
|
|
L Lcz G d |
|
|
E |
|
G g dz L |
; |
* |
|
|
|
** |
|
|
|
2 |
|
|
|||
|
|
|
|
|
||
* |
c2 |
|
|
** |
|
|
|
|
E |
|
G g dz W |
|
, |
|
|
|
||||
W Vdp Wcz G d |
2 |
|
|
|||
|
|
|
|
|
|
|
(16)
(17)
13
где cE – скорость движения тела, dz – изменение высоты центра тяжести тела в поле тяготения.
Внутренняя энергия тела
Внутренняя энергия представляет собой полный запас энергии тела и состоит из энергии поступательного и вращательного движения молекул,
энергии внутримолекулярных колебаний, потенциальной энергии сил сцеп-
ления между молекулами, внутримолекулярной энергии, внутриатомной энергии.
Внутренняя энергия U является функцией состояния, она не зависит от пути процесса, а ее элементарное изменение обозначается символом полного дифференциала (dU).
Внутренняя энергия измеряется в Джоулях (Дж), а удельная внутрен-
няя энергия (u) - в Дж/кг.
Для простых тел внутренняя энергия определяется как функция двух переменных (р,T; р,v или T,v).
Теплота
Теплота - количество энергии, передаваемой от одного тела к другому посредством теплопроводности, конвективного или лучистого теплообмена.
Процесс передачи теплоты называется теплообменом.
Количество теплоты Q , получаемое телом в результате теплообмена,
зависит от вида термодинамического процесса и аналогично работе является функцией процесса. Поэтому, элементарное количество теплоты не является полным дифференциалом ( Q ).
Количество теплоты Q измеряется в Джоулях (Дж), а удельное коли-
чество теплоты q = Q / G в Дж/кг.
Теплоемкость
14
Теплоемкостью называется количество теплоты, которое надо сооб-
щить единице массы, количества или объема вещества, чтобы его темпера-
тура повысилась на 1 градус.
Различают массовую теплоемкость с, измеряемую в Дж/(кг К), моляр-
ную c – Дж/(кмоль К) и объемную с' – Дж/(м3 К).
Связь между массовой, молярной и объемной теплоемкостью пред-
ставлена следующими соотношениями:
c c ; |
c |
|
c . |
(18) |
|
||||
Теплоемкость газов зависит от термодинамического процесса, в кото- |
||||
ром подводится или отводится теплота. Если процесс задан |
условием |
|||
z = idem, то теплоемкость в этом процессе будет определяться следующим образом:
cz
qz dt
.
(19)
Эта теплоемкость называется истинной.
Экспериментальное определение теплоемкости обычно проводится в двух процессах: при постоянном объеме (изохорная теплоемкость cv ) и по-
стоянном давлении (изобарная теплоемкость cp).
Теплоемкость реального газа зависит от температуры и давления. Теп-
лоемкость идеального газа зависит только от температуры.
Для практических расчетов вводится понятие средней теплоемкости в интервале температур от t1 до t2, значение которой принимается неизменной для всего рассматриваемого интервала температур (сzm).
Из уравнения (19) следует, что количество теплоты, подведенной к те-
лу (или отведенной от него) в процессе 1–2 (изобарном или изохорном),
определяется соотношением

15
2 q1,2 cz dt czm ( t2 t1 ) . 1
Отсюда следует выражение средней теплоемкости газа
(20)
c |
|
|
|
q |
|
|
|
|
|
|
|
t |
|
1,2 |
|
|
t |
|
|||
|
|
|
|
|
|
|
||||
|
zm |
|
|
t |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
1 |
|
|
|
2 |
1
t |
1 |
|
|
|
2 cz dt 1
.
(21)
Для большинства газов значения средней теплоемкости в интервале температур от t1 до t2 приведены в специальных термодинамических табли-
цах.
Для некоторых газов в определенном интервале температур истинная теплоемкость изменяется по линейному закону
cz az bz t .
Подставив это выражение (22) в уравнение (21), получим
|
2 |
|
|
|
|
|
|
|
|
|
|
|
( az |
bzt ) dt |
( t |
|
t |
|
) |
|
|||
czm |
1 |
|
|
|
az bz |
1 |
2 |
, |
|||
|
|
|
|
|
|
||||||
( t |
|
t |
|
|
|
2 |
|
|
|||
|
2 |
1 |
) |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
||
(22)
(23)
называется первой средней теплоемкостью. Она численно равна ис-
тинной теплоемкости при среднеарифметической температуре процесса.
2. Физическое состояние вещества, фазовая диаграмма чистого вещества
Различают три агрегатных состояния простых систем: твердое, жидкое и газовое.
С помощью фазовой диаграммы можно проследить переход тела из од-
ного агрегатного состояния в другое. Рассмотрим диаграмму фазовых состо-