Материал: Теоретические основы теплотехники 1
56
подводимой и отводимой теплоты, можно получить математическое условие обратимости цикла
|
|
|
Q |
|
|
|
|
2обр |
|
обр |
L |
|||
|
|
|||
|
|
|
||
|
|
|
ц .обр |
или
=
Q |
|
L |
|
|
1обр |
ц .обр |
|
||
|
L |
|
|
|
|
|
ц .обр |
|
|
|
обр |
|
обр |
|
|
|
|
||
|
Q |
|
|
= |
1обр |
1 |
|
L |
|||
|
|
||
|
ц .обр |
|
|
1 1 . |
|
||
=
1 |
1 |
|
|
||
|
||
обр |
|
(145)
(145а)
Особое значение в термодинамике играет цикл Карно, являющийся ос-
новой теории тепловых машин.
Цикл Карно
Французский инженер Сади Карно в 1824 г. предложил обратимый цикл тепловой машины, рабочим телом в котором является идеальный газ.
Цикл Карно осуществляется между двумя внешними источниками постоян-
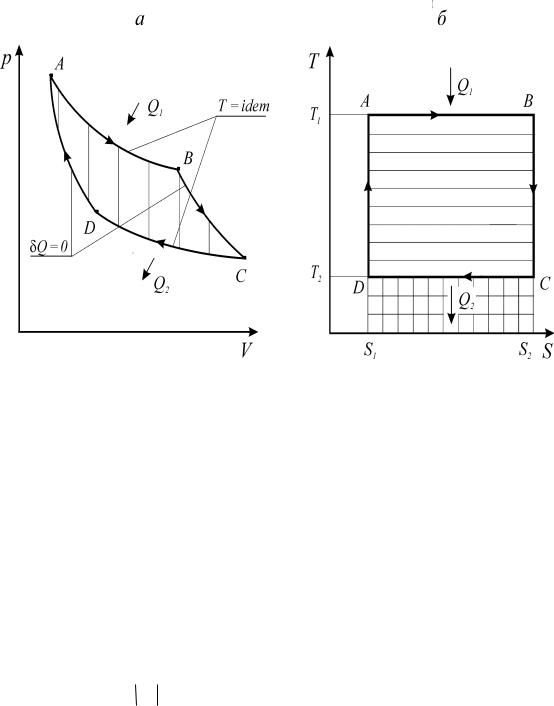
ных температур Т1 и Т2 и состоит из двух адиабат и двух изотерм (рис. 12).
Подвод теплоты от горячего источника производится на изотерме А-В
при температуре Т1, при этом рабочее тело - идеальный газ расширяется и совершается полезная работа. В процессе дальнейшего расширения по адиа-
бате В-С до температуры Т2 также совершается полезная работа. Для осу-
ществления последующих процессов - сжатия C-D по изотерме Т2 с отводом теплоты к холодному источнику и адиабатного сжатия D-A до начальной температуры Т1 работа затрачивается.
В силу того, что в цикле используется идеальный газ, для которого ра-
нее было установлен принцип существования энтропии, этот цикл можно также изобразить и в координатах T-S (рис. 12б).
57
Рис. 12. Цикл Карно для теплового двигателя
Графически цикл Карно в T-S координатах представляет собой прямо-
угольник, так как изотермы и адиабаты в этих координатах изображаются прямыми линиями.
Согласно принципу существования энтропии для идеальных газов
( Q TdS ) (75) интегральные количество подведенной и отведенной тепло-
ты в цикле Карно может быть определено из следующих соотношений:
1 |
|
B |
1 |
|
|
||
Q |
|
|
T dS |
|
|
A |
|
|
|
C |
|
 Q1
Q1  T2dS
T2dS
D
B = T1 dS A
C = T2 dS D
= T1 SB
= T2 SC
S A ;
SD
.
(146)
(147)
Для замыкания цикла необходимо, чтобы итоговое изменение энтро-
пии (как функции состояния) в цикле было равно нулю

следовательно
SB
58
dS = 0,
SA SC SD S2 S1 S .
(148)
(149)
Количества подведенной и отведенной теплоты равны соответственно:
Q1
 Q2
Q2 
T1 S
T2 S
,
,
(150)
(151)
а работа цикла составляет
 Lц
Lц 
Q |
Q |
1 |
2 |
T1
T |
S |
2 |
|
(152)
Согласно определению КПД термодинамического цикла тепловых двигателей (141) выражение коэффициента полезного действия цикла Карно можно представить в следующем виде:
K t
|
L |
|
( T T |
) S |
|
|
ц |
|
|||
|
1 |
2 |
|
||
|
|
|
|
||
|
Q |
|
T |
S |
|
|
1 |
|
1 |
|
|
1 |
T |
|
2 |
||
|
||
|
T |
|
|
1 |
.
(153)
Соответственно, холодильный коэффициент обратного цикла Карно для холодильной машины определяется соотношением
|
K |
|
T |
|
2 |
||||
|
|
|||
|
t |
T |
T |
|
|
|
|||
|
|
1 |
2 |
.
(154)
Полученные соотношения (153) и (154) свидетельствуют о том, что КПД и холодильный коэффициент обратимого цикла Карно зависят только от соотношения абсолютных температур горячего Т1 и холодного Т2 источ-
59
ников теплоты.
Анализ соотношения (153) показывает, что КПД цикла Карно возрас-
тает с увеличением температуры горячего и при понижении температуры холодного источников.
Цикл Карно для теплотехники имеет большое значение. Он позволяет определить наивысшее значение термодинамического КПД теплового двига-
теля, работающего в диапазоне значений температуры рабочего тела в про-
цессах подвода (Т1) и отвода (T2 ) теплоты. При этом цикл Карно является эталоном: с КПД цикла Карно сравнивают КПД циклов реальных тепловых двигателей и определяют их термодинамическое совершенство.
7.Второе начало термодинамики
Как отмечалось выше, первое начало термодинамики представляет со-
бой количественное выражение закона сохранения и превращения энергии,
оно позволяет составить энергетический баланс исследуемых процессов, но не определяет направление их протекания. Условия осуществления и направленности протекания процессов определяются на основании второго начала термодинамики.
В совокупности первое и второе начало термодинамики являются фун-
даментом в построении теории тепловых машин и технической термодина-
мики в целом.
Второе начало классической термодинамики обычно формулируется как объединенный принцип существования и возрастания некоторой функ-
ции состояния тел и сложных систем, названной энтропией (термин энтро-
пия предложен Р. Клаузиусом: еn – в, внутрь и trope или tropos – обращение,
путь; в целом – обращение внутрь, мера обесценения энергии).
Математическое выражение второго начала классической термодина-
мики может быть представлено в виде следующего выражения:
60
dSизол |
Q |
0 . |
|
T |
|||
|
|
(155)
Н.И. Белоконь справедливо заметил, что принципы существования и возрастании энтропии различны по содержанию и значимости и предложил рассматривать эти принципы раздельно.
Принцип существования энтропии справедлив для равновесных термо-
динамических систем и распространяется на любые процессы – обратимые и необратимые. Принцип существования энтропии и абсолютной температуры как термодинамических функций состояния равновесных систем, по терми-
нологии проф. Н.И. Белоконь, был назван вторым началом термостатики.
Принцип возрастания энтропии характеризует только наиболее веро-
ятное направление течения реальных процессов и, следовательно, имеет несомненно меньшую область применения, чем принцип существования эн-
тропии. Принцип возрастания энтропии изолированных систем при протека-
нии в них реальных процессов Н.И. Белоконь назвал вторым началом тер-
модинамики.
Второе начало термостатики
В качестве постулата второго начала термостатики используется утверждение, что «температура есть единственная функция состояния,
определяющая направление самопроизвольного теплообмена».
Для вывода математического выражения второго начала термостатики рассмотрим адиабатно изолированную систему, состоящую из термически сопряженных тел (рис. 13). Первое тело (I) - любое тело (например,
реальный газ), совершает произвольные процессы - обратимые и необрати-
мые, второе тело (II) - контрольное тело - идеальный газ, совершает обрати-
мый круговой процесс. Оба тела в каждый момент имеют одинаковую температуру (tI = tII = t).