Материал: Теоретические основы теплотехники 1
|
|
61 |
|
. |
|
. |
|
A |
A |
II |
|
|
I |
|
|
. |
|
. |
|
|
. |
|
. |
II
t |
I |
t |
II |
|
|
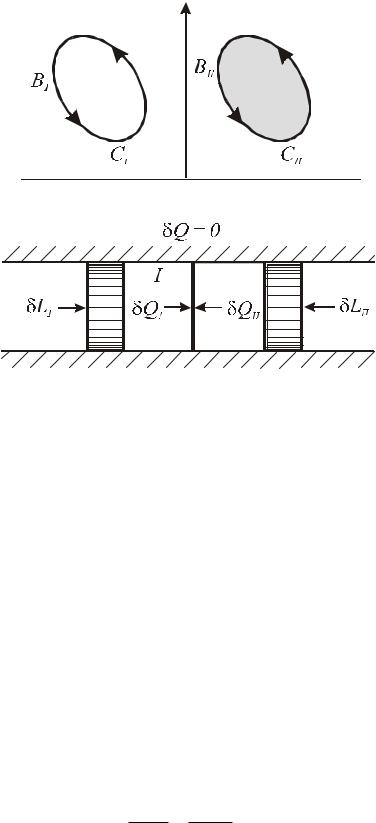
Рис. 13. Адиабатно изолированная система двух термически сопряженных тел
Первое и второе тело осуществляют разнообразные процессы измене-
ния состояния, к ним извне подводится (или отводится) работа, между тела-
ми происходит теплообмен, но для адиабатно изолированной системы вы-
полняется обязательное условие
Q Q |
Q |
I |
II |
0
.
(156)
Разделим уравнение (156) на некоторую функцию, зависящую только от температуры (t). Для идеального газа эта функция равна абсолютной температуре (tII) = TII . С учетом равенства температур двух тел получаем
Q |
I |
|
|
|
|
||
|
|
|
|
( t |
I |
|
) |
|
|
|
|
Q |
|
|
|
II |
|
( t |
II |
) |
|
|
|
0
.
(157)
Так как тела I и II возвращаются в исходное состояние одновременно
(согласно теореме теплового равновесия тел в равновесных круговых про-

62
цессах) последнее уравнение можно интегрировать по замкнутому контуру
|
Q |
|
|
Q |
|
||
|
|
I |
|
II |
|
||
|
|
|
|
|
|
||
|
( t |
I |
) |
|
( t |
II |
) |
|
|
|
|
|
|
||
0
.
(158)
Второй интеграл по замкнутому контуру для идеального газа, как ин-
теграл функции состояния, равен нулю
|
Q |
II |
dSII |
|
|
|
|||
|
|
|
|
|
|
( t |
II |
) |
|
|
|
|
||
0
.
(159)
Поэтому и первый круговой
нулю
интеграл
Q |
I |
0 . |
|
|
|
||
|
|
|
|
( t |
I |
|
) |
|
|
|
|
в уравнении (158) также равен
(160)
Если круговой интеграл равен нулю, то это значит, что подынтеграль-
ное выражение представляет из себя полный дифференциал некоторой функции состояния, названной энтропией ( S ), а функция (tI) является инте-
грирующим делителем
Q |
I |
|
Q |
I |
|
|
|
|
|||
|
|
|
|
||
( t |
I |
) |
|
T |
|
|
|
|
I |
|
|
dSI
.
(161)
Так как тело I - любое тело и свойства тел I и II независимы, получен-
ное выражение (161) распространяется на все равновесные процессы изме-
нения состояния любых систем. Выбранная функция (t), которая не зависит от вида тел, называется абсолютной температурой (t)= Т, а температурная шкала называется абсолютной термодинамической.
Таким образом, получаем математическое выражение второго начала термостатики - принципа существования энтропии и абсолютной темпера-

63
туры для любых равновесных систем
dS |
Q |
|
Q* Q** |
(162) |
|
T |
|
T |
|
и для 1 кг системы
|
q |
|
q |
|
|
|
* |
ds |
T |
|
|
|
|
|
q** T
.
(163)
Второе начало термостатики утверждает принцип существования эн-
тропии и абсолютной температуры как функции состояния любой равновес-
ной термодинамической системы, совершающей обратимые или необрати-
мые процессы.
Следствия второго начала термостатики
Следствия второго начала термостатики широко применяются в термо-
динамических расчетах и формулируются на основе анализа его математиче-
ского выражения (162), (163).
Следствие I. Совместное выражение первого начала термодинамики и второго начала термостатики позволяет получить дифференциальное урав-
нение термодинамики, которое связывает между собой все термодинамиче-
ские свойства веществ
T ds= c dT + du v dv T
p dv
|
|
dh |
|
= cp dT + |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
dP |
||
|
|
|
T |
v dp . (164)
Следствие II. Координаты Т - S являются универсальными координа-
тами термодинамического теплообмена.
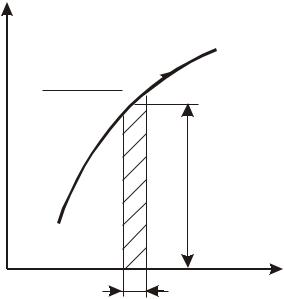
Рассмотрим процесс 1-2 в координатах Т-S и выделим на нем элемен-
тарный участок с температурой Т и изменением энтропии dS (рис. 14).
64
T
Q = T dS
 .
.
. 1
. |
2 |
|
T
d S |
S |
|
Рис. 14. Термодинамический процесс в координатах T-S
Исходя из математического выражения второго начала термостатики площадь под кривой элементарного участка процесса равна подводимому
(отводимому) количеству теплоты
Q = T dS. |
(165) |
При этом полное количество теплоты, подведенной или отведенной от системы в процессе 1-2, определяется следующим образом:
Q1,2 =
2 T
1
dS
.
(166)
Если из-под знака интеграла в соотношении (166) вынести среднюю температуру конечного процесса Tm , то количество теплоты в процессе мо-
жет быть определено по соотношению
Q1,2 = Tm (S2 - S1). |
(167) |
65
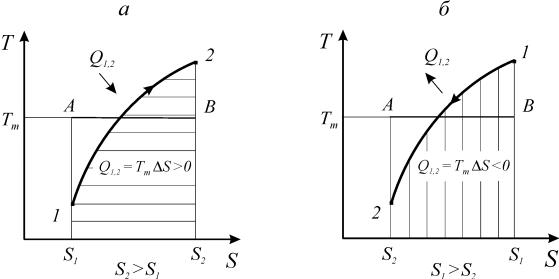
Как видно из выражения (166) и рис. 15, знак теплообмена определяет-
ся знаком изменения энтропии. Процессы, протекающие с увеличением эн-
тропии, сопровождаются подводом теплоты. Процессы, протекающие с уменьшением энтропии - отводом теплоты. Независимо от природы рабочего тела площадь под кривой процесса в координатах Т-S равна количеству под-
веденной или отведенной теплоты.
Рис. 15. Теплообмен в термодинамических процессах
Следствие III. Адиабатный процесс является процессом изоэнтропий-
ным.
Так как в адиабатном процессе теплообмен отсутствует ( Q = 0), то,
согласно второму началу термостатики (162), в таком процессе изменение энтропии dS = 0 (S = idem). Согласно этому следствию, показатель адиабат-
ного процесса ( k ) равен показателю изоэнтропийного процесса ( |
n |
s ) |
|
|
|
k ns . |
|
(168) |
Следствие IV. Коэффициент полезного действия и холодильный коэф-
фициент термодинамических циклов тепловых машин не зависят от вида