Материал: Теоретические основы теплотехники 1
|
46 |
|
|
q1,2 |
k n |
l1,2 . |
|
k n |
|||
|
|
||
|
u |
|
(121)
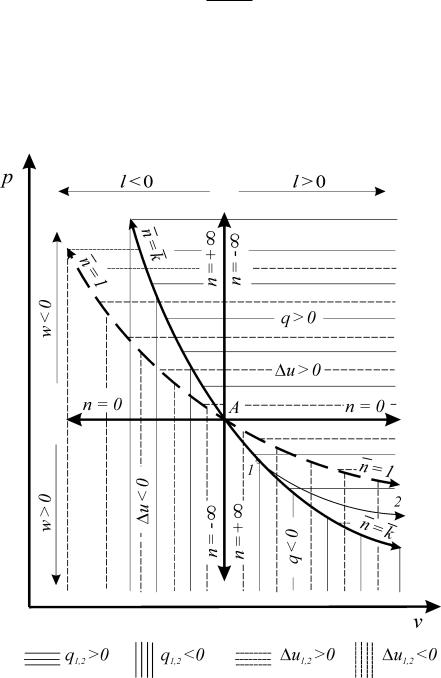
Полученные соотношения (120), (121) позволяют в координатах p-v по-
строить области подвода и отвода теплоты (рис. 9).
Рис. 9. Процессы изменения состояния идеального газа
Некоторые характеристики важнейших термодинамических процессов приведены в табл. 1
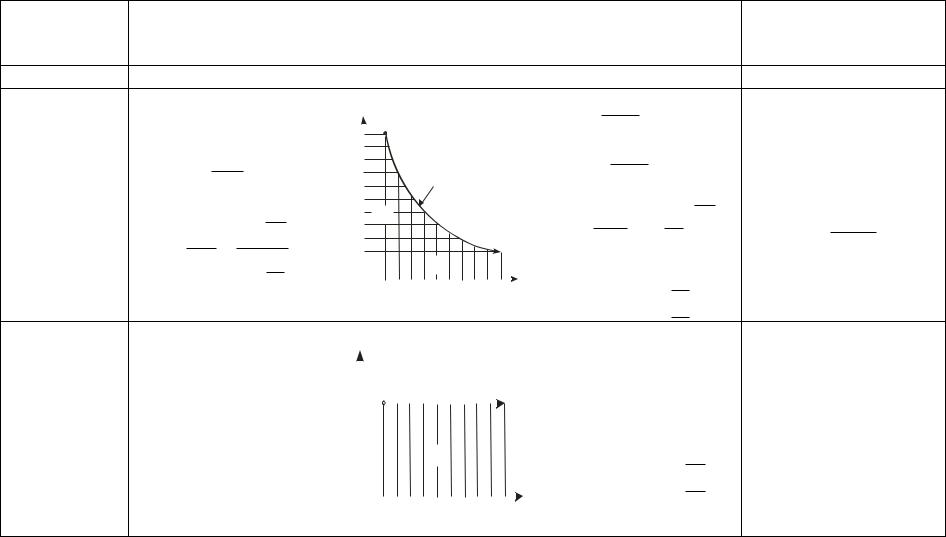
Название и уравнение
процесса
1
Политропный pvn = idem
Изобарный p = idem, dp = 0
47
Термодинамические процессы изменения состояния простого тела
|
Показатель |
|
|
|
|
|
Графическое |
|
|
|
|
|
|
|
|
|
|
|
|
Работа |
|
||||||||||||
|
политропы |
|
|
|
|
|
изображение |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
2 |
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P v |
1 |
|
1 1,2 , |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
l1,2 = |
|
1 |
|
|
|
||||||||||||
|
- n + , |
|
|
P |
|
|
|
n |
1 |
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
P v |
|
|
|
|
|
|
|
||||||
|
|
|
|
vdp |
|
w |
|
|
|
|
|
|
|
|
|
|
|
|
1 |
1,2 , |
|||||||||||||
n = |
|
|
|
|
|
|
|
|
|
w1,2 |
= n |
|
|
1 |
|
|
1 |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
n |
|
|
n |
|
1 |
||||||||||||||||||||
|
|
|
|
|
pdv |
|
|
|
|
|
Pv = idem |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n 1 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
p |
|
|
w |
|
|
|
|
|
P v |
|
|
|
|
|
|
|
P |
|
n |
|||||||
|
|
|
|
|
log |
|
|
1 |
|
|
|
1,2 |
|
|
|
|
2 |
|
|
|
|
|
|||||||||||
|
w |
|
|
|
|
|
|
|
|
|
|
|
1,2 = |
|
|
2 |
|
|
|
= |
|
|
2 |
|
= |
||||||||
|
|
|
|
|
p |
|
|
|
|
|
2 |
|
P v |
|
|
|
|
|
P |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
1,2 |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
l |
|
|
|
|
|
v |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
log |
|
|
|
2 |
|
1,2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
1,2 |
|
|
2 |
|
|
|
|
|
|
|
v |
|
|
|
n |
1 |
|
T |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
v |
|
|
|
|
|
|
|
= |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
1 |
2 |
|
= |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
v |
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
2 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
v |
v |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
v |
2 |
|
|
|
|
|
|
T |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
||||
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P= idem |
|
|
|
l1,2 = p (v2 - v1), |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
1 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
P1 |
|
|
|
|
|
|
|
|
w1,2 |
= 0, |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
n = 0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n 1 |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
1,2 |
|
|
1,2 |
|
|
v1 |
|
T2 |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= |
T |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
v |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= |
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
1 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
v1 |
v2 v |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 1
Количество
теплоты
5
q1,2 = u1,2 + l1,2 =
= h1,2 + w1,2 ,
q1,2 = |
k n |
l1,2 |
|
k n |
|||
|
|
||
|
u |
|
q1,2 = u1,2 + l1,2 =
= h1,2
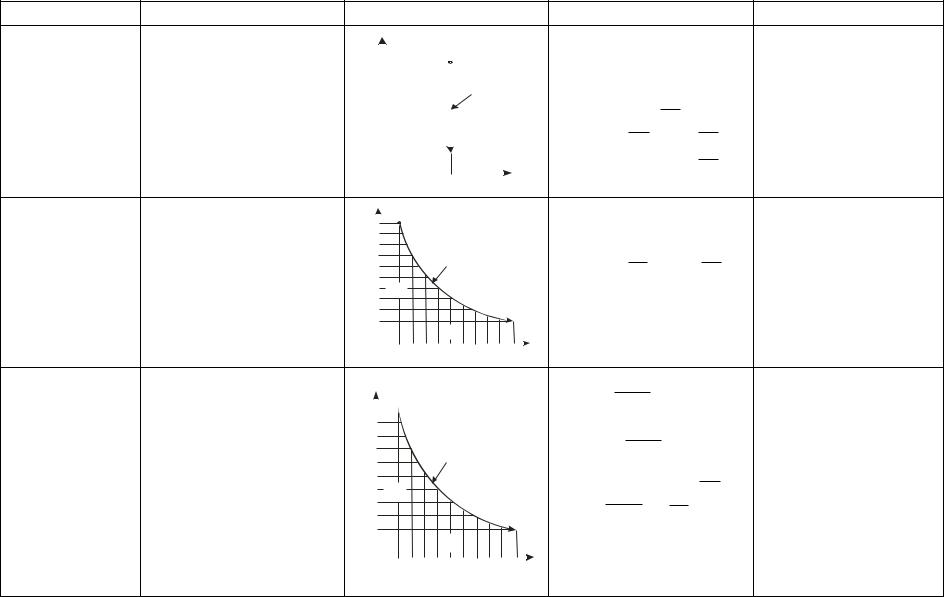
1 |
2 |
Изохорный
v = idem, n = ± ∞ dv = 0
Изопотенциаль- |
n = 1 |
|
ный pv = idem |
||
|
Адиабатный |
n = k = ns = |
||||||
|
|
|
|
|
|||
δq = 0, |
vdp |
|
h |
||||
|
k |
|
|
|
|
|
|
|
|
|
|||||
pv |
= idem |
|
|
|
u s |
||
|
|
pdv s |
|||||
48
|
|
|
3 |
|
|
||||
P |
|
|
|
|
|
|
|
||
P1 |
|
|
1 |
|
|
|
|||
|
|
|
|
|
|
|
v = idem |
||
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
w1,2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P2 |
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
||||
|
|
|
|
|
|
||||
|
|
|
|
v1 = v2 |
v |
|
|
||
P |
1 |
|
|
|
|
|
|
||
P |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|||
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Pv = idem |
|
|
|||
|
w |
|
|
|
|
|
|
|
|
1,2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
P |
|
|
|
|
|
|
|
||
2 |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|||
|
|
|
1, 2 |
|
|
|
|||
|
v |
|
|
|
|
v |
v |
||
1 |
|
|
|
|
2 |
||||
P
P1  1
1
Pvk = idem
w1,2
2
P2
1,2
v1 |
v2 v |
4
l1,2 = 0,
w1,2 = v (p1 - p2),
|
|
P |
|
n 1 |
|
T |
|
|
|
|
n |
|
|
||||
1,2 |
= |
|
2 |
|
= |
|
2 |
|
|
|
|||||||
|
P |
|
|
T |
||||
|
|
|
|
|||||
|
|
|
|
|
|
|||
|
|
1 |
|
|
|
1 |
||
l1,2 = w1,2 = |
|
|
|||
|
v |
2 |
|
P |
|
= pv ln |
|
= pv ln |
1 |
, |
|
v |
|
P |
|||
|
1 |
|
|
||
|
|
|
2 |
|
|
1,2 = 1 |
|
|
|||
|
|
p v |
|
1 1,2 , |
|||||||||||
l1,2 = |
|
|
1 |
1 |
|||||||||||
k |
1 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
p v |
1 |
1,2 , |
||||||||||
w1,2 = k |
|
|
1 |
|
1 |
||||||||||
k |
|
||||||||||||||
|
|
|
1 |
|
|
|
|
|
|
||||||
|
P v |
|
|
|
|
P |
|
|
k 1 |
||||||
|
|
|
|
|
|
|
k |
||||||||
|
2 |
|
2 |
|
|
|
2 |
|
|
||||||
1,2 = |
|
= |
= |
||||||||||||
|
|
|
|||||||||||||
P v |
|
|
P |
|
|||||||||||
|
|
|
|
|
|
|
|
||||||||
|
1 |
|
|
|
|
|
|
|
|||||||
|
1 |
|
|
|
1 |
|
|
||||||||
|
v |
|
k 1 |
|
T |
2 |
|
|
|||||||
= |
|
|
1 |
|
|
|
|
|
= |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
v |
|
|
|
|
|
|
|
T |
|
|
||||
|
|
2 |
|
|
|
|
|
|
1 |
|
|
||||
Продолжение табл. 1
5
q1,2 = u1,2 =
= h1,2 + w1,2
q1,2 = u1,2 + l1,2 =
=h1,2 + w1,2
q1,2 = 0

|
|
|
49 |
|
|
|
Процессы изменения состояния идеального газа |
|
|||
|
При изучении процессов изменения состояния идеальных газов, наряду |
||||
с |
общими |
соотношениями |
по |
расчету |
термодинамических |
процессов (79) |
– (121), следует |
использовать уравнение Клапейрона (27) |
|||
и закон Джоуля (33), в соответствии с которыми для идеального газа спра-
ведливы следующие выражения:
если
h
pv idem , то T idem;
u pv u RT h T ; du cv dT ;
dh c p dT .
(122)
(123)
(124)
(125)
Из уравнений (122) (125) следует, что для идеального газа процессы изопотенциальный (pv =idem), изотермический (T = idem), изоэнергетиче-
ский (u= idem) и изоэнталыпийный (h = idem) тождественны и, следователь-
но, показатели этих процеcсов равны
n |
pv |
n |
|
T |
nu
nh
1
.
(126)
Характеристика расширения или сжатия процессов, в которых рабочим телом является идеальный газ, с учетом уравнения Клапейрона может быть определена по соотношению температур
|
|
|
p |
2 |
v |
2 |
|
|
|
||||
|
|
|
|
|
||
|
1,2 |
|
p v |
|
||
|
|
|
|
|||
|
|
|
|
1 |
1 |
|
=
T2 T1
.
(127)
Изменения удельных значений внутренней энергии и энтальпии иде-
ального газа в процессе в соответствии с законом Джоуля находится по сле-
дующим формулам:
u1,2 cvm T2 T1 ; |
(128) |
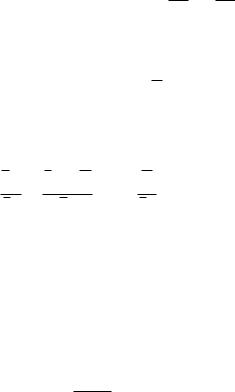
50
h1,2 cpm T2 T1 .
(129)
Показатель адиабатного процесса для идеального газа определяется как соотношение изобарной и изохорной теплоемкостей
k = ns =
|
w |
|
|
|
l |
q 0
|
h |
= |
|
|
u |
q 0
=
c c
p v
=
c c
p v
.
(130)
На основании закона Майера ( cp cv R ) показатель адиабаты для идеального газа может быть определен из следующего соотношения:
k =
c c
p v
=
cv R |
1 |
|
R |
|
cv |
cv |
|||
|
|
>1.
(131)
Для идеального газа показатель изоэнергетического процесса |
nu |
поэтому удельное количество теплоты в элементарном процессе может определено по формуле
q |
k n |
l . |
|
k 1 |
|||
|
|
1 |
и |
быть
(132)
На примере идеального газа произведем анализ термодинамических процессов (рис.9).
Адиабата ( q 0 ) является линией перемены знака теплообмена. При расширении газа термодинамическая работа l 0 и тогда любая политропа,
расположенная правее адиабаты (n < k), находится в области подвода тепло-
ты ( q > 0). Если политропа расширения будет находиться слева от адиабаты
(n > k), то этот процесс будет характеризоваться отводом теплоты ( q < 0).
Таким образом, все термодинамические процессы, проходящие выше адиабаты осуществляются с подводом теплоты и наоборот.