Материал: Теоретические основы теплотехники 1

36 |
|
|
|
|
|
|
|
T |
|
p |
4 |
|
|
порционально температуре рабочего тела |
4 |
|
|
. |
||
T |
p |
|||||
|
|
|
||||
|
1 |
|
|
1 |
|
|
Удельная термодинамическая и потенциальная работы в изохорном процессе определяются из соотношений
w1,4
|
|
4 |
l1,4 |
p |
|
|
|
1 |
|
4 |
vdp |
|
||
1 |
|
|
dv
v
0 |
, |
p |
|
1 |
|
p4
.
(82)
(83)
Количество теплоты, подведенной к рабочему телу или отведенной от него в изохорном процессе, определяется из выражения первого начала тер-
модинамики
q |
h |
w |
1,2 |
1,2 |
1,2 |
u1,2
.
(84)
Изопотенциальный процесс – термодинамический процесс изменения
состояния |
системы, |
при |
котором |
значение |
потенциальной |
функции |
( П pv idem; d( pv ) 0 ) сохраняет неизменное значение |
||||
(процессы 1-6, 1-7) (рис. 5).
Для идеального газа, согласно уравнению Клапейрона ( pv RT ), изо-
потенциальный процесс ( pv idem ) является и изотермическим (T idem).
Удельная термодинамическая и потенциальная работы в изопотенци-
альном процессе (1-6) определяются из следующих соотношений:
|
|
6 |
|
6 |
|
dv |
|
|
|
|
v6 |
|
|
|
|
||
|
|
l1,6 p dv = pv |
= pv ln |
; |
|
|
(85) |
||||||||||
|
|
|
|
|
|
||||||||||||
|
|
1 |
|
|
1 |
|
v |
|
|
|
|
v1 |
|
|
|
||
|
6 |
|
6 |
|
|
dp |
|
|
|
1 |
dp |
|
|
|
p |
|
|
|
|
|
|
|
|
p |
|
|
|
|
p |
|
|
|
p |
|
|
w |
|
v dp = |
|
vp |
|
|
= pv |
|
|
= pv ln |
1 |
. |
(86) |
||||
1,6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
1 |
|
|
|
|
|
|
6 |
|
|
|
|
6 |
|
|

37
(
pv
Нетрудно заметить, что постоянство потенциальной функции idem ) приводит к равенству логарифмов в выражениях (85) и (86) в си-
лу того, что соблюдается условие
p1 p6
v6 v1
. Поэтому, в изопотенциальном
процессе численные значения термодинамической и потенциальной работ равны между собой.
Количество теплоты, подведенной к рабочему телу или отведенной от него в изопотенциальном процессе определяется из выражения первого нача-
ла термодинамики по балансу рабочего тела
q |
u |
l |
h |
1,2 |
1,2 |
1,2 |
1,2 |
w1,2
.
(87)
Уравнения перечисленных простейших и любых других термодинами-
ческих процессов могут быть представлены одним уравнением. Это уравне-
ние называется уравнением политропы, а термодинамические процессы, опи-
сываемые этим уравнением, называются политропными.
Политропные процессы
Термин «политропа» представляет собой сочетание двух греческих слов «поли» - много и «тропос» - путь, направление. Поэтому в политропном процессе предполагается многообразие путей изменения параметров состоя-
ния системы.
Политропным процессом с постоянным показателем называется обра-
тимый термодинамический процесс изменения состояния простого тела, под-
чиняющийся уравнению, которое может быть представлено в следующих формах:
pvn idem C ; |
(88) |
p1 / n v idem C ; |
(89) |
1 |
|

38
n |
n |
p1v1 |
= p2v2 . |
(90)
где п – показатель политропы, являющий в рассматриваемом процессе по-
стоянной величиной, которая может иметь любые частные значения - поло-
жительные и отрицательные (- n + ).
Физический смысл показателя политропы п определяется после диф-
ференцирования выражения (88)
v |
n |
dp n v |
n 1 |
pdv 0 . |
|
|
Из соотношения непосредственно следует
n |
vdp |
|
w |
|
w |
. |
|
|
1,2 |
||||
|
|
|
|
|
|
|
|
pdv |
|
l |
|
l |
|
|
|
|
|
|
1,2 |
|
(91)
(92)
Это значит, что постоянный показатель политропы определяется со-
отношением потенциальной и термодинамической работ в элементарном или конечном процессах. Значения этих работ могут быть определены графиче-
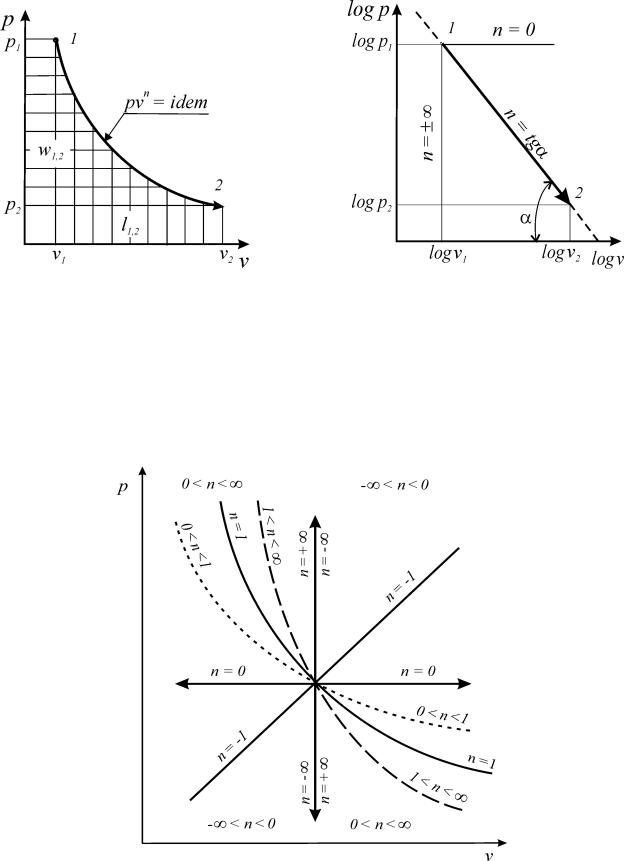
ски в координатах p v (рис. 6а).
В логарифмических координатах политропный процесс (политропа) с
постоянным показателем представляет собой прямую линию (рис. 6б)
log
p n log
v
log
C
.
(93)
При этом, постоянный показатель политропы определяется как тангенс угла наклона линии процесса к оси абсцисс ( ) (рис. 6б)
n =
log p |
1 |
log p |
2 |
|
|
||
log v |
2 |
log v |
|
|
1 |
||
=log( p1 / p2 ) . log( v2 / v1 )
(94)
39
а |
б |
Рис. 6. Политропа с постоянным показателем
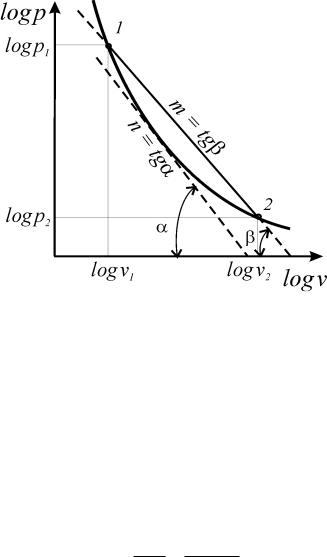
Из соотношения (92) следует, что для изобарного процесса n = 0,
для изохорного процесса - n = ± ∞, для изопотенциального процесса - n = 1 (рис. 7).
Рис. 7. Политропные процессы изменения состояния простого тела
40
Следует отметить, что не все термодинамические процессы в коорди-
натах logv – logp описываются прямой линией, т.е. подчиняются уравнению политропы с постоянным показателем. Любой термодинамический процесс можно описать уравнением политропы с переменным показателем (рис. 8).
Расчет политропного процесса с переменным показателем вызывает необходимость ввести в рассмотрение три показателя процесса: истинный показатель процесса (n); первый средний показатель n и второй средний показатель (m).
Рис. 8. Политропа с переменным показателем
Истинный показатель процесса (n) определяется как соотношение эле-
ментарной потенциальной работы w к элементарной термодинамической работе l , что соответствует тангенсу угла наклона касательной, проведен-
ной к кривой процесса в точке процесса, к оси абсцисс ( ) в логарифмиче-
ской сетке координат
n =
w |
|
vdp |
|
|
l |
pdv |
|||
|
|
d log p d log v
= tg .
(95)
Для конкретных процессов, характеризующихся неизменным значени-