Материал: t1_struktura_immunnoy_sistemy
Поскольку в синтезе иммуноглобулина M не принимают участия Т-лимфоциты, он является резистентным к облучению и воздействию иммунодепрессантов.
Продолжительный синтез преимущественно (либо исключительно) иммуноглобулина M свидетельствует о нарушениях в регуляторных функциях Т-лимфоцитов-хелперов. Гипериммуноглобулинемия М является первичным иммунодефицитом, спровоцированным отсутствием CD40 лиганда на Т-лимфоцитах-хелперах, что приводит к невозможности передачи костимуляционных сигналов В-лимфоцитам, без чего невозможно переключение синтеза иммуноглобулина M на синтез иного класса.
Некоторая часть иммуноглобулинов M способна продуцироваться локально, ее относят к секреторным иммуноглобулинам.
IgA.
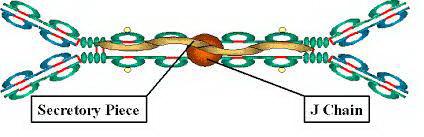
Иммуноглобулины А (IgA) циркулируют в сыворотке крови (составляет 15-20% от всех Ig), а также секретируются на поверхность зпителиев. Присутствуют в слюне, слёзной жидкости, молоке и на поверхности слизистых оболочек.
Молекулы IgA участвуют в реакциях нейтрализации и агглютинации возбудителей. Кроме того, после образования комплекса Аг-АТ они участвуют в активации комплемента по альтернативному пути.
Дефицит IgA является одним из некорригируемых первичных дефектов иммунитета. Исправление данного дефекта состоит в лечении вторичных осложнений аллергической, аутоиммунной, либо инфекционной природы в совокупности с активацией сохранных элементов иммунитета с целью перекрытия недостатка продукции IgA (компенсации). Показаниями к проведению подобной иммуностимуляции являются преимущественно клинические проявления сниженной противоинфекционной сопротивляемости.
Известно, что уровень защиты от локальной вирусной инфекции желудочно-кишечного и респираторного трактов зависит не столько от наличия в организме сывороточного IgG к пневмотропным энтеропатогенным вирусам, сколько от содержания секреторного специфического иммуноглобулина A.
Отчетливый аффинитет к поверхностям слизистой оболочки, преобладание в секрете молочных желез, стабильная структура определяют биологическую значимость секреторного иммуноглобулина A в процессах защиты организма от агрессивного воздействия всевозможных патогенных агентов, в частности, вирусов.
Иммуноглобулин A в димерном виде синтезируют в lamina propria-клетках, а после связывания IgA с синтезированным в клетках эпителия иммуноглобулиновым рецептором транспортируют к поверхности слизистой оболочки. В момент появления IgA в просвете кишечника происходит частичное расщепление рецептора, вследствие чего IgA обогащается его фрагментом, именуемым секреторным компонентом. Очевидно, что секреторный IgA – совместный продукт клеток двух типов – эпителиальных и плазматических.
Способность секреторного иммуноглобулина А образовываться как в димерной, так и в тетрамерной формах значительно повышает его вирусонейтрализирующие свойства. Секреторный компонент защищает иммуноглобулин А от расщепления протеолитическим ферментом, что является его существенным преимуществом перед другими антителами. Секреторный IgA способен нейтрализовать вирус, как в просвете кишечника, так и во время транспортировки его внутрь клетки. Сначала димер иммуноглобулина А нейтрализует вирус в подслизистой кишечника, затем связывается с рецептором и транспортирует вирус в просвет кишечника.
Единая структура секреторного компонента и димерных иммуноглобулинов класса А, соединенная j-цепью является уникальным примером эволюционной адаптации иммуноглобулина на слизистых покровах, следствием чего является эффективное функционирование при постоянном воздействии антигенов разнообразной природы.
В различные внешние секреты, в том числе в молоко, молекулы иммуноглобулина A проникают из двух основных источников. IgA, выделяемый респираторным и пищеварительным трактами, секретами молочной и слезной желез, а также слюной, образуют плазматические клетки. Однако иммуноглобулин A, обнаруженный во внешних секретах может иметь происхождение и системного характера. Такой IgA продуцируется в клетках слизистой оболочки одного органа, поступает в кровь и переносится ею к слизистым покровам другого органа.
Проникнув в пейерову бляшку антиген активирует В- и Т-лимфоциты, используя лимфатический проток, те проникают сначала в мезентериальный лимфоузел, после чего в кровь, затем в селезенку и опять в кровь. Происходит их селективная локализация в лимфообразованиях слизистых оболочек, а также в секреторных железах экзокринной природы: слезных, молочных и слюнных. При этом локализация лимфоцитов происходит по большей части между клетками эпителия слизистой оболочки, что обеспечивает иммунный ответ клетки. Локализация В-лимфоцитов наблюдается преимущественно в lamina propria, где происходит их дифференциация в плазматические клетки, а также синтезируется иммуноглобулин A.
IgE.
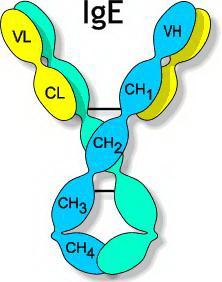
Иммуноглобулин Е (IgE) - класс иммуноглобулинов, обнаруживаемый в норме в незначительных количествах в сыворотке крови и секретах. Впервые IgE был изолирован в 1960-х годах из сывороток больных атопией и множественной миеломой. В 1968 г. ВОЗ выделила IgE как самостоятельный класс иммуноглобулинов. Согласно ВОЗ 1 МЕ/мл (МЕ - международная единица) соответствует 2,4 нг. Обычно концентрация IgE выражается в МЕ/мл или кЕ/л (кЕ - килоединица).
В норме IgE составляет менее 0,001% от всех иммуноглобулинов сыворотки крови.
Структура IgE подобна структуре других иммуноглобулинов и состоит из двух тяжёлых и двух лёгких полипептидных цепей. Они сгруппированы в комплексы, называемые доменами. Каждый домен содержит приблизительно 110 аминокислот. IgE имеет пять таких доменов в отличие от IgG, который имеет только четыре домена. IgE имеет самую короткую продолжительность существования (время полувыведения из сыворотки крови 2 - 3 суток), самую высокую скорость катаболизма и наименьшую скорость синтеза из всех иммуноглобулинов (2,3 мкг/кг в сутки). IgE синтезируется главным образом плазматическими клетками, локализующимися в слизистых оболочках. Основная биологическая роль IgE - уникальная способность связываться с поверхностью тучных клеток и базофилов человека. На поверхности одного базофила присутствует примерно 40000 - 100000 рецепторов, которые связывают от 5000 до 40000 молекул IgE.
Дегрануляция тучных клеток и базофилов происходит, когда две связанные с мембраной клеток молекулы IgE соединяются с антигеном, что, в свою очередь, «включает» последовательные события, ведущие к выбросу медиаторов воспаления.
Помимо участия в аллергических реакциях I (немедленного) типа, IgE принимает участие в защитном противогельминтном иммунитете, что обусловлено существованием перекрёстного связывания между IgE и антигеном гельминтов. Последний проникает через мембрану слизистой и садится на тучные клетки, вызывая их дегрануляцию. Медиаторы воспаления повышают проницаемость капилляров и слизистой, в результате чего IgG и лейкоциты выходят из кровотока. К гельминтам покрытым IgG присоединяются эозинофилы, которые выбрасывают содержимое своих гранул и таким образом убивают гельминтов.
IgE можно обнаружить в организме человека уже на 11-й неделе внутриутробного развития. Содержание IgE в сыворотке крови возрастает постепенно с момента рождения человека до подросткового возраста. В пожилом возрасте уровень IgE может снижаться.
В практике клинико-диагностических лабораторий определение общего и специфического IgE проводится с целью их использования в качестве самостоятельных диагностических показателей.
Болезни и состояния, сопровождающиеся изменением содержания общего IgE сыворотки крови
|
Болезни и состояния |
Возможные причины |
|
I. Повышенное содержание IgE |
|
|
Аллергические болезни, обусловленные IgE антителами: а) Атопические болезни · Аллергический ринит · Атопическая бронхиальная астма · Атопический дерматит · Аллергическая гастроэнтеропатия б) Анафилактические болезни · Системная анафилаксия · Крапивница - ангионевротический отек |
Множественные аллергены: · пыльцевые · пылевые · эпидермальные · пищевые · лекарственные препараты · химические вещества · металлы · чужеродный белок |
|
Аллергический бронхопульмональный аспергиллез |
Неизвестны |
|
Гельминтозы |
IgE антитела, связанные с защитным иммунитетом |
|
Гипер-IgE синдром (синдром Джоба) |
Дефект Т-супрессоров |
|
Селективный IgA дефицит |
Дефект Т-супрессоров |
|
Синдром Вискотт-Олдриджа |
Неизвестны |
|
Тимусная аплазия (синдром Ди-Джорджи) |
Неизвестны |
|
IgE - миелома |
Неоплазия IgE-продуцирующих плазматических клеток |
|
Реакция "трансплантат против хозяина" |
Дефект Т-супрессоров |
|
II. Сниженное содержание общего IgE |
|
|
Атаксия - телеангиэктазия |
Дефекты Т-клеток |
IgD.
Иммуноглобулины D (Ig D) — иммуноглобулины с молекулярной массой 185 кД. На долю IgD приходится около 1% всех иммуноглобулинов. Период их полураспада 3 дня. Они мономеры. Экспрессируются в основном на мембране В-лимфоцитов. Молекула IgD состоит из двух тяжелых дельта-цепей и двух легких (лямбда или каппа).
Биологическая активность их изучена недостаточно. Установлено, что они принимают участие в дифференцировке В-клеток и совместно с мембранным IgM выполняют рецепторную функцию. Дельта-цепь имеет молекулярную массу 64 кД, состоит из 500 аминокислот, содержит три N — связанных олигосахарида, представляет собой полипептидную цепь с одним вариабельным (VH) и тремя константными (CH1, CH2, CH3) доменами. Кроме того, в ней есть 58 дополнительных аминокислотных последовательностей, составляющих шарнирную область (очень чувствительна к протеолитическим ферментам).
Динамика выработки антител. Первичный и вторичный иммунный ответ.
Первичный ответ- при первичном контакте с возбудителем (антигеном), вторичный- при повторном контакте. Основные отличия:
- продолжительность скрытого периода (больше- при первичном);
- скорость нарастания антител (быстрее- при вторичном);
- количество синтезируемых антител (больше- при повторном контакте);
- последовательность синтеза антител различных классов (при первичном более длительно преобладают IgM, при вторичном- быстро синтезируются и преобладают IgG- антитела).
Вторичный иммунный ответ обусловлен формированием клеток иммунной памяти. Пример вторичного иммунного ответа- встреча с возбудителем после вакцинации.
Роль антител в формировании иммунитета.
Антитела имеют важное значение в формировании приобретенного постинфекционного и поствакцинального иммунитета.
1. Связываясь с токсинами, антитела нейтрализуют их, обеспечивая антитоксический иммунитет.
2. Блокируя рецепторы вирусов, антитела препятствуют адсорбции вирусов на клетках, участвуют в противовирусном иммунитете.
3. Комплекс антиген- антитело запускает классический путь активации комплемента с его эффекторными функциями (лизис бактерий, опсонизация, воспаление, стимуляция макрофагов).
4. Антитела принимают участие в опсонизации бактерий, способствуя более эффективному фагоцитозу.
5. Антитела способствуют выведению из организма (с мочой, желчью) растворимых антигенов в виде циркулирующих иммунных комплексов.
IgG принадлежит наибольшая роль в антитоксическом иммунитете, IgM- в антимикробном иммунитете (фагоцитоз корпускулярных антигенов), особенно в отношении грамотрицательных бактерий, IgA- в противовирусном иммунитете (нейтрализация вирусов), IgAs- в местном иммунитете слизистых оболочек, IgE- в реакциях гиперчувствительности немедленного типа.
ИММУННЫЙ ОТВЕТ
Иммунные реакции принято подразделять на два типа: гуморальный и клеточный. Первый основан на наличии АТ, второй - на действии активированных Т-лимфоцитов.
Иммунный ответ гуморального типа - это ответная на определённый АГ реакция системы иммунитета, которая характеризуется пролиферацией клона В-лимфоцитов и дифференцировкой их в плазматические клетки, секретирующие иммуноглобулины. Краткая схема иммунного ответа гуморального типа представлена на рисунке.
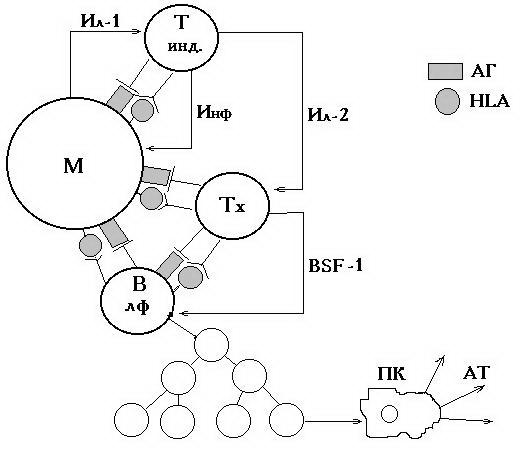
Рис. Схема иммунного ответа гуморального типа.
(М-макрофаг; Т-инд. - Т индуктор; Тх - Т-хелпер; В лф.- В-лимфоцит; ПК - плазматическая клетка; Ил-1 и Ил-2- интерлейкин 1 и 2; Инф- интерферон; BSF-1 - фактор стимуляции В-клеток; АГ-антиген; HLA - молекулы главного комплекса гистосовместимости).
Иммунный ответ клеточного типа характеризуется выработкой большого количества антигенспецифических активированных Т лимфоцитов, часть которых непосредственно выполняет функцию эффекторов, а другие клетки синтезируют особые медиаторы, или лимфокины (рис.).
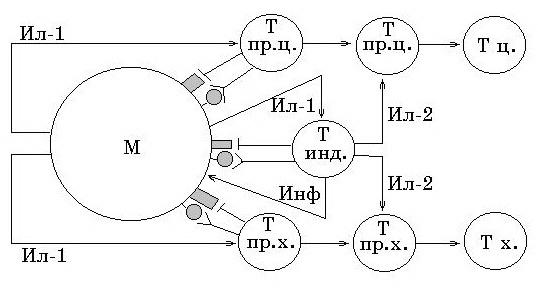
Рис. Схема иммунного ответа клеточного типа.
(Т пр.ц. - предшественник Т цитотоксической клетки; Т ц. - цитотокси-
ческий Т лимфоцит; Т пр.х. - предшественник Т хелпера).
Цитокины
В развитии иммунного ответа важную роль играют цитокины. Они действуют как на малых, так и больших расстояниях, обеспечивают взаимодействие между разными категориями иммунокомпетентных клеток, а также выполняют роль эффекторных молекул иммунных реакций. Они являются теми посредниками, которые обеспечивают связь иммунной системы с гемопоэзом (стволовыми кроветворными клетками), с эндокринной и нервной системами. Через них иммунная система оказывает регуляторное влияние на различные органы и ткани, может активировать или подавлять их функции, регулировать метаболизм, процессы физиологической и репаративной регенерации. К группе цитокинов относятся: интерлейкины – макромолекулы, продуцируемые лимфоцитами; монокины, продуцируемые моноцитами/ макрофагами; интерфероны; факторы некроза опухоли; хемокины, которые способны регулировать хемотаксис и активность лейкоцитов, а также воспалительные реакции. Многие цитокины принадлежат к семейтсву гемопоэтинов: ГМ-КСФ, Г-КСФ, ИЛ-2, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-7, ИЛ-11, ИЛ-12, ИЛ-13, ИЛ-15.