Материал: t1_struktura_immunnoy_sistemy
-
Собственно В-клетки (ещё называемые «наивными» В-лимфоцитами) — неактивированные В-лимфоциты, не контактировавшие с антигеном. Не содержат тельца Голла, в цитоплазме рассеяны монорибосомы. Полиспецифичны и имеют слабое сродство к многим антигенам.
-
В-клетки памяти — активированые В-лимфоциты, вновь перешедшие в стадию малых лимфоцитов в результате кооперации с Т-клетками. Являются долгоживущим клоном В-клеток, обеспечивают быстрый иммунный ответ и выработку большого количества иммуноглобулинов при повторном введении того же антигена. Названы клетками памяти, так как позволяют иммунной системе «помнить» антиген на протяжении многих лет после прекращения его действия. В-клетки памяти обеспечивают долговременный иммунитет.
-
Плазматические клетки — являются последним этапом дифференцировки активированных антигеном В-клеток. В отличие от остальных В-клеток несут мало мембранных антител и способны секретировать растворимые антитела. Являются большими клетками с эксцентрично расположенным ядром и развитым синтетическим аппаратом - шероховатый эндоплазматический ретикулум занимает почти всю цитоплазму, также развит и аппарат Гольджи. Являются короткоживущими клетками (2-3 дня) и быстро элиминируются при отсутствии антигена, вызвавшего иммунный ответ.
Характерной особенностью В-клеток является наличие поверхностных мембраносвязанных антител, относящихся к классам IgM и IgD. В комплексе с другими поверхностными молекулами иммуноглобулины формируют антигенраспознающий рецептивный комплекс, ответственный за узнавание антигена. Также на поверхности В-лимфоцитов расположены антигены МНС класса II, важные для взаимодействия с Т-клетками, также на некоторых клонах В-лимфоцитов присутствует маркер CD5, общий с Т-клетками. Рецепторы компонентов комплемента C3b (Cr1, CD35) и C3d (Cr2, CD21) играют определённую роль в активации В-клеток. Следует отметить, что маркеры CD19, CD20 и CD22 используются для идентификации В-лимфоцитов. Также на поверхности В-лимфоцитов обнаружены Fc рецепторы.
НК-клетки
Эта категория клеток имеет морфологию больших гранулярных лимфоцитов. Присутствуют в крови и во всех лимфоидных органах в количестве от 5% до 10%. Развиваются в костном мозге и тимусе из стволовой лимфоидной клетки. Фенотипически маркером НК-клеток являются молекулы CD56, CD16. Клетки не имеют ни ТКР, ни sIg. Их рецепторы, обеспечивающие активацию клеток и адгезию к мишени, принадлежат к семейству С-лектинов. На НК-клетках экспрессированы рецепторы к ИЛ-2, ИЛ-12, ИЛ-15, через которые возможна их стимуляция. Натуральные киллеры способны оказывать прямое цитотоксическое действие на клетки-мишени как путем контактного лизиса, так и через факторы, секретируемые либо в виде гранул, либо в свободном состоянии. Эти факторы способны разрушатьДНК клеток – мишеней, внутриклеточную вирусную ДНК, супрессировать репликацию вирусов, а также обладают бактерицидной, фунгистатической и антипротозойной активностью. Их мишенями являются инфицированные клетки, чужеродные клетки, измененные свои и опухолевые клетки. НК-клетки обладают способностью продуцировать гамма-интерферон.
Отдельная субпопуляция НК-клеток и цитотоксических Т-лимфоцитов, обладающая способностью разрушать клетки-мишени в реакции АЗКЦ (антителозависимой клеточной цитотоксичности), названа К-лимфоцитами. Эти лимфоциты не несут собственного специфического маркера. К-лимфоциты присутствуют в крови и во всех лимфоидных органах. Их количество в крови составяет около 9% от всех лимфоцитов. К категории К-клеток (что не идентично понятию К-лимфоцитов) относятся, помимо К-лимфоцитов, макрофаги, гранулоциты, проявляющие цитотоксичность в АЗКЦ.
Развитие мононуклеарных фагоцитов в костном мозге и тканях
К мононуклеарным фагоцитам относятся моноциты периферической крови и тканевые макрофаги (макрофаги соединительной ткани, макрофаги печени, альвеолярные макрофаги легких, свободные и фиксированные макрофаги селезёнки и лимфатических узлов, макрофаги серозных полостей, клетки микроглии ЦНС, остеокласты костной ткани). Мононуклеарные фагоциты (М.Ф.) генерируются в костном мозге из кроветворной полипотентной клетки и в форме моноцита покидают орган и поступают в кровоток. Часть тканевых макрофагов образуется из моноцитов крови и часть – в результате пролиферации тканевых макрофагов.
Мононуклеарные фагоциты обладают следующими свойствами:
1) высокой фагоцитарной способностью и бактерицидностью. (Мононуклеарные фагоциты способны поглощать микроорганизмы, повреждённые и погибшие клетки, разрушать их и метаболизировать);
2) участвуют в индукции гуморального и клеточного иммунитета (представляют антиген лимфоцитам в иммуногенной форме);
3) оказывают регуляторное влияние на развитие иммунных реакций и гемопоэз (продуцируемые клетками ИЛ-1, ИЛ-6, ИЛ-12, ИЛ-8 оказывают активирующее действие на Т-хелперы, Т-цитотоксические клетки, В-лимфоциты, а гемопоэтины (ГМ-КСФ,Г-КСФ) – повышают функциональную активность кроветворных клеток);
4) являются эффекторами иммунных реакций. (Активированные макрофаги способны уничтожать чужеродные и опухолевые клетки через развитие реакции АЗКЦ или экзопродукцию гидролитических энзимов, цитотоксических форм кислорода и ФНОa).
На мембране макрофагов экспрессированы различные рецепторы для захвата микроорганизмов: макрофагальный маннозный рецептор (ММР), Scavenger-рецептор (рецептор-мусорщик, МРМ), рецепторы для бактериального ЛПС. Благодаря ММР, осуществляется захват Mycobacteria, Leishmania, Legionella, Pseudomonas aeraginosa и других. Через МРМ происходит эндоцитоз липопротеинов при превращении макрофага в пенистую клетку, а также фагоцитоз большинства бактерий. Помимо этих рецепторов, на поверхностной мембране макрофагов выявлены многочисленные рецепторы для цитокинов, гормонов, компонентов комплемента (С3, С4) и Fc-фрагмента иммуноглобулинов. Повышенная экспрессия рецепторов для Fc-фрагмента иммуноглобулинов и С3 ассоциируется с увеличением функциональной активности макрофагов и может модулироваться биологически активными субстанциями, например, усиливаться цитокинами, ингибироваться кортикостероидами.
Кроме рецепторов, на поверхности макрофагов идентифицировано большое число антигенов, но ни один из них не является строго специфичным для этих клеток. Наиболее характерным считается антиген СD14, функционирующий как рецептор для ЛПС клеточной стенки грамотрицательных бактерий. Связывание молекулой CD14 комплекса бактериальных ЛПС вызывает немедленную активацию макрофагов, включение синтеза провоспалительных цитокинов и стимуляцию моноцитопоэза. В соответствии с этим молекула CD14 рассматривается как рецептор для фактора роста макрофагов. Экспрессия этого рецептора на макрофагах повышается при воспалении и иммунном ответе.
Наиболее мощным и специфическим индуктором активности макрофагов является интерферон-γ. Активация макрофагов включает комплекс структурно-функциональных сдвигов, направленных на повышение защитной способности клеток. В процессе активации резко увеличивается интенсивность метаболических процессов, повышаются синтез и секреция биологически активных продуктов, активность лизосомных ферментов, экспрессия поверхностных рецепторов и антигенов, что проявляется усилением фагоцитарной активности макрофагов.
Макрофаги содержат и продуцируют целую гамму биологически активных веществ, которые оказывают регуляторное влияние на многие клетки и системы организма
Мононуклеарные фагоциты, в отличие от Т-лимфоцитов и В-лимфоцитов, не имеют клонально-заданных свойств и не обладают антигенной специфичностью, в иммунных реакциях они выступают как неспецифические клетки.
Эозинофильные и базофильные гранулоциты
Эозинофильные гранулоциты имеют диаметр в капле крови 9-10 мкм. Количество их в периферической крови 1-5% общего числа лейкоцитов.
Эозинофилы способны к фагоцитозу, эмиграции в ткани. Они принимают участие в защитных реакциях организма на чужеродный белок, в аллергических и анафилактических реакциях, участвуют в метаболизме гистамина. Не обладая способностью синтезировать гистамин, они могут накапливать его, фагоцитируя гистаминсодержащие гранулы, выделяемые базофилами и тучными клетками, а также абсорбировать его на цитоплазме, содержащей специфические рецепторы к гистамину. Кроме того, они вырабатывают специфический фактор, тормозящий освобождение гистамина из базофилов и тучных клеток. Эозинофилы способны к цитолизу чужеродных клеток, играют ключевую роль в противогельминтной защите организма.
Базофильные гранулоциты имеют диаметр около 9 мкм в капле крови. В крови человека составляют 0,5-1% общего числа лейкоцитов.
Базофилы не обладают фагоцитарной активностью. Они участвуют в метаболизме гистамина и гепарина, являются активными участниками аллергических реакций 1 типа. На их мембране экспрессированы Fс-рецепторы для IgЕ. На каждой клетке экспрессировано более 200000 таких рецепторов, обладающих высокой аффинностью.
Морфология и клеточный состав лимфоидных образований слизистых
В слизистых, где нет постоянного и длительного воздействия антигенов, лимфоциты располагаются разрозненно, на некотором расстоянии друг от друга, формируя диффузную лимфоидную ткань. В участках, где наблюдается частое соприкосновение с антигенами и аллергенами, лимфоциты собираются в мелкие и крупные плотные скопления, получившие название лимфоидных узелков. Лимфоидные узелки, не имеющие центров размножения, содержатся в большом количестве в слизистой оболочке пищевода, дыхательных путей (гортани, трахеи, крупных бронхов). В местах постоянного и сильного воздействия антигенов, где требуется участие в защитных реакциях все новых и новых лимфоцитов, располагаются лимфоидные узелки с центрами размножения. В этих герминативных центрах клетки располагаются рыхло, и на микропрепаратах эти центры выглядят более светлыми, чем окружающая (периферическая, мантийная) зона лимфоидного узелка. Центры размножения в лимфоидных узелках являются местами размножения лимфоцитов, потребность в которых в местах постоянного антигенного вторжения велика. Лимфоидные узелки с центрами размножения в большом количестве имеются в слизистой оболочке желудка, тонкой и толстой кишки, в аппендиксе. У детей в стенках аппендикса, имеющем длину в среднем 7-10 см и диаметр 0,5-1 см, насчитывается до 700-800 лимфоидных узелков.
Лимфоидные бляшки представляют собой достаточно крупные скопления лимфоидной ткани в стенке тонкой кишки. По сути они являются собранными вместе, плотно прилежащими лимфоидными узелками. В составе отдельных бляшек может быть до 900 лимфоидных узелков. Безусловно, такие объединения лимфоидных узелков повышают их функциональную значимость. Следует учесть, что все лимфоидные узелки в составе лимфоидных бляшек имеют центры размножения. В этих центрах происходит образование новых лимфоцитов и их дифференцировка. Это явление можно рассматривать как местное воспроизводство лимфоцитов в стенках кишечника, где постоянно происходит всасывание продуктов переваривания. Вероятно, объединение лимфоидных узелков с центрами размножения в единую структуру в лимфоидных бляшках является морфологическим механизмом, обеспечивающим высокую степень иммунной защиты в условиях интенсивного антигенного воздействия перевариваемой пищи на слизистую оболочку тонкой и толстой кишки.
Миндалины лимфоидного кольца Пирогова расположены в стенках верхних отделов глотки. Они являются первым защитным барьером от патогенов, способных проникать в организм с воздухом и пищей. Лимфоидная паренхима миндалин представлена многочисленными лимфоидными узелками с центрами размножения и окружающей их диффузной лимфоидной тканью. Здесь же находятся свободно перемещающиеся лимфоциты и макрофаги.
В стенках слизистых покровов (кишечника, желудка и других органов) имеются многочисленные свободные лимфоциты и плазматические клетки. Некоторые из этих клеток проникают в эпителиальный пласт и располагаются между эпителиоцитами. Они первыми взаимодействуют с антигенным раздражителем. Известно, что в области желудка на 1000 эпителиоцитов приходится около 50 лимфоцитов, в пилорическом отделе желудка этот показатель составляет 59 лимфоцитов. Между энтероцитами ворсинок тонкой кишки располагается от 100 до 300 лимфоцитов на 1000 эпителиальных клеток.
Лимфоидные образования слизистых покровов – лимфоидные узелки с герминативными центрами, лимфоидные бляшки, глоточные миндалины, как и регионарные лимфатические узлы, состоят из Т- и В-зон с наличием зародышевых центров в В-зоне. Лимфоидные узелки без центров размножения не содержат таких зон. В клеточном составе лимфоидных образований насчитывается 40-50% Т-лимфоцитов (СD3+-клеток) и 40-45% В-лимфоцитов (CD19+-клеток). Среди Т-лимфоцитов субпопуляция Т-хелперов (CD4+, -клeтoк) составляет около 60%, субпопуляция цитотоксических клеток (СD8+-лимфоцитов) – около 25%. sIgA+-В-лимфоциты в общем пуле В-лимфоцитов составляют около 10-15%.
Уникальную морфологическую структуру имеют пейеровы бляшки. Они содержат 3 анатомические зоны: купол, В-клеточную и Т-клеточную зоны. Зона купола представлена лимфоцитами, макрофагами и небольшим числом плазматических клеток. Эта зона выстлана уникальным эпителием – микроскладчатыми клетками (М-клетками). М-клетки имеют короткие микровилли, небольшие цитоплазматические отростки и небольшое число лизосом. М-клетки ответственны за транспорт антигена внутрь пейеровых бляшек. В-клеточная (фолликулярная) зона, располагающаяся под куполом, содержит большое число IgA+-B-лимфоцитов. Фолликулярная зона включает зародышевый центр, в котором происходит пролиферация В-клеток и их дифференцировка в плазматические клетки – продуценты IgA. Т-клеточная зона содержит две основные Т-клеточные субпопуляции: Т-хелперы и Т-цитотоксичекие лимфоциты.
Функционально в иммунной системе слизистых покровов выделяют два участка: индуктивный (лимфатические узлы, миндалины, лимфоидные бляшки, лимфоидные узелки) и эффекторный (lamina propria и межэпителиальные лимфоциты). В индуктивном участке происходит распознавание антигена, его презентация в иммуногенной форме и формирование популяции антигенспецифических лимфоцитов. В этом процессе принимают участие дендритные клетки, макрофаги, ГКГ II+-клетки, CD4+, -лимфoциты, СD8+-лимфоциты, sIgA+-B-лимфоциты.
В эффекторном участке продуцируется секреторный IgA и накапливаются эффекторные Т-лимфоциты, которые обеспечивают клеточную защиту слизистых поверхностей. В lamina propria от общего количества лимфоидных клеток Т-лимфоциты составляют 40-60%, В-лимфоциты – 20-40%, НК-клетки – 2-3%; межэпителиальные лимфоциты на 80-90% представлены Т-клетками, среди которых основной процент принадлежит СD8+-лимфоцитам, обладающих цитотоксичностью и способностью усиливать продукцию sIgA.
Закономерности развития иммунных реакций в слизистых оболочках
Проникновение патогена в слизистую оболочку приводит к его захвату макрофагами и презентации Т- и В-лимфоцитам. Из просвета кишечника антигены доставляются в индуктивный отдел иммунной системы слизистой с помощью М-клеток, где в дальнейшем представляются иммунокомпетентным клеткам.
Под влиянием антигена происходит отбор клоноспецифических Т- и В-лимфоцитов , их активация и пролиферация. Большая часть активированных Т- и В-лимфоцитов проходит своё развитие до зрелых эффекторных клеток (плазматических или цитотоксических клеток) в индуктивном отделе иммунной системы слизистых (лимфоидных узелках, лимфоидных бляшках, регионарных лимфатических узлах), после чего эти клетки мигрируют в эффекторную зону иммунной системы слизистых, где и реализуют свои свойства (продуцируют IgA или вызывают цитолиз чужеродных клеток).
Основную роль в регуляции дифференцировки IgA+ В-клеток в антитело-секретирующие клетки играют ТН2-хелперы (CD4+, ), и продуцируемые ими ИЛ-5, ИЛ-6.
Часть антигенактивированных в слизистых покровах Т- и В-лимфоцитов через лимфатические сосуды и грудной лимфатический проток попадает в системную циркуляцию, откуда они диссеминируют в селезенку, отдаленные лимфатические узлы и индуктивные участки лимфоидных образований слизистых других систем организма. Такая высокая миграционная активность лимфоидных клеток слизистых обеспечивает непрерывное пополнение всех участков слизистых покровов (желудочно-кишечного тракта, респираторной системы, мочеполовой системы и железистых органов) антигенреактивными Т- и В-лимфоцитами, что в итоге служит постоянному поддержанию высокой общей иммунореактивности организма.
Особую роль в этом процессе играет иммунная система желудочно-кишечного тракта, которая, как известно, находится в постоянном контакте с громадным потоком микробного и аллергенного материала. Установлено, что пейеровы бляшки тонкой кишки являются важным (но не единственным) источником плазмоцитов, секретирующих IgA, практически для всех слизистых оболочек и железистых органов, а стимуляция иммунокомпетентных клеток пейеровых бляшек ведет к активации иммунной системы не только ЖКТ, но и дыхательного и урогенитального трактов. Известно, что секреторный IgA обеспечивает эффективную защиту слизистых покровов от инвазии микробов, вирусов, от проникновения токсинов и аллергенов, усиливает антибактериальную активность фагоцитов. Селективный дефицит IgA, развивающийся по разным причинам, в том числе и вследствие мутации в структурных генах Нa-цепи, способен приводить к аллергическим, инфекционным и аутоиммунным заболеваниям кишечника и других слизистых структур организма. Установлено, что повышенный поток микробных антигенов и токсинов может вести к активации «дремлющих» клонов аутоиммунных лимфоцитов и при наличии соответствующих условий может служить пусковым механизмом в развитии патологического процесса. Отсюда следует, что нормализация работы иммунной системы слизистых покровов и поддержание нормальной продукции IgA является обязательным условием лечения и профилактики инфекционных, аллергических и аутоиммунных заболеваний.
Антитела.
Антитела — специфические белки гамма- глобулиновой природы, образующиеся в организме в ответ на антигенную стимуляцию и способные специфически взаимодействовать с антигеном (in vivo, in vitro). В соответствии с международной классификацией совокупность сывороточных белков, обладающих свойствами антител, называют иммуноглобулинами.
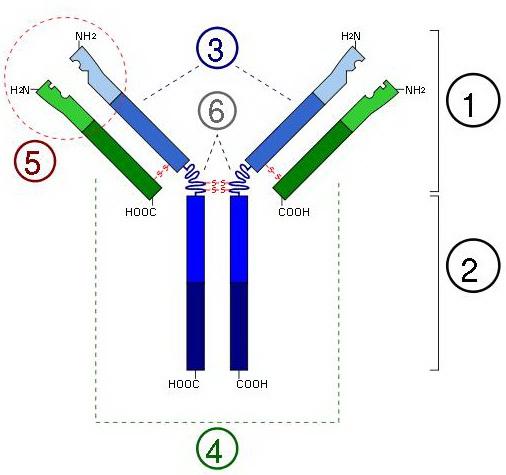
Общий план строения иммуноглобулинов:
1) Fab (Участок связывания антигена (Fab, fragment antigen binding) — это участок молекулы иммуноглобулина, который связывает антиген. Fab состоит из одного константного и одного вариабельного домена легкой и тяжелой цепей. Эти домены образуют паратоп — сайт связывания антигена на N-конце. Вариабельные домены связывают эпитоп специфических антигенов). Fc и Fab могут быть получены разрезанием молекулы иммуноглобулина ферментом папаином, при этом из одной молекулы мономерного иммуноглобулина образуются два Fab и один Fc. Фермент пепсин разрезает иммуноглобулины ниже шарнирного участка и при этом образуется один мономер Fc и один F(ab)2);