Материал: t1_struktura_immunnoy_sistemy
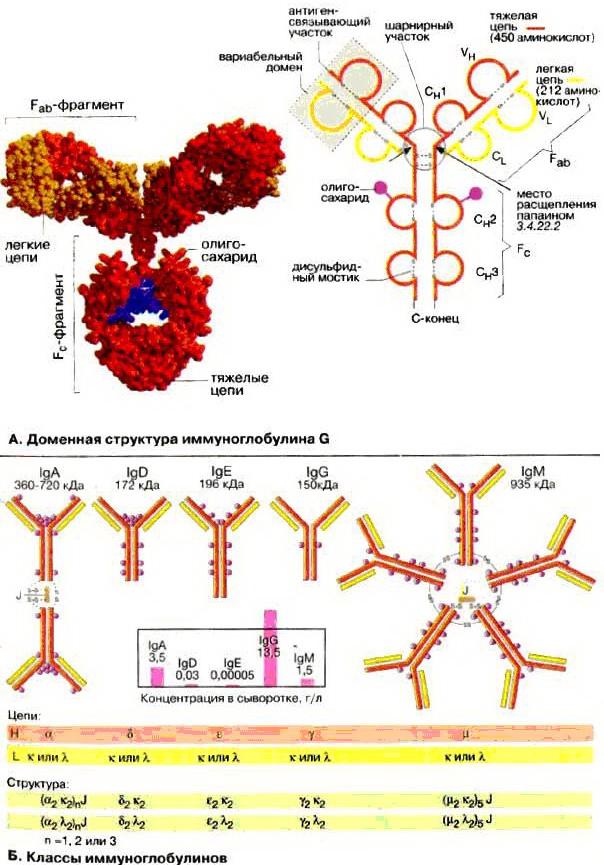
2) Fc (Кристаллизующийся фрагмент иммуноглобулина (Fc, fragment crystallizable region, Fc region) — это концевая часть молекулы иммуноглобулина, которая взаимодействует с Fc рецептором на поверхности клетки и с некоторыми белками системы комплемента. Данное свойство позволяет антителам активировать иммунную систему. Fc участок IgG, IgA и IgD изотипов состоит из двух одинаковых белковых фрагментов, соответственно, второго и третьего константных доменов двух тяжелых цепей; в случае изотипов IgM и IgE Fc содержит три константных домена тяжелых цепей (домены CH 2-4) в каждой полипептидной цепочке. Другая часть антитела называется Fab (от англ. Fragment antigen binding), и состоит из вариабельных участков, которые определяют специфичность мишени, которую связывает антитело. Напротив, Fc всех антител одного класса одинаковы и константны. Отсюда происходит неправильное объяснение происхождения термина Fc как «fragment constant region»);
3) тяжелая цепь;
4) легкая цепь;
5) антиген-связывающийся участок;
6) шарнирный участок.
Уникальность антител заключается в том, что они способны специфически взаимодействовать только с тем антигеном, который вызвал их образование.
Иммуноглобулины ( Ig ) разделены в зависимости от локализации на три группы:
- сывороточные (в крови);
- секреторные ( в секретах- содержимом желудочно- кишечного тракта, слезном секрете, слюне, особенно- в грудном молоке) обеспечивают местный иммунитет (иммунитет слизистых);
- поверхностные ( на поверхности иммунокомпетентных клеток, особенно В- лимфоцитов).
Любая молекула антител имеет сходное строение ( Y- образную форму) и состоит из двух тяжелых ( Н ) и двух легких ( L ) цепей, связанных дисульфидными мостиками. Каждая молекула антител имеет два одинаковых антигенсвязывающих фрагмента Fab ( fragment antigen binding ), определяющих антительную специфичность, и один Fc ( fragment constant ) фрагмент, который не связывает антиген, но обладает эффекторными биологическими функциями. Он взаимодействует со “своим” рецептором в мембране различных типов клеток ( макрофаг, тучная клетка, нейтрофил).
Концевые участки легких и тяжелых цепей молекулы иммуноглобулина вариабельны по составу ( аминокислотным последовательностям ) и обозначаются как VL и VH области. В их составе выделяют гипервариабельные участки, которые определяют структуру активного центра антител (антигенсвязывающий центр или паратоп). Именно с ним взаимодействует антигенная детерминанта (эпитоп) антигена. Антигенсвязывающий центр антител комплементарен эпитопу антигена по принципу “ключ — замок” и образован гипервариабельными областями L- и Н- цепей. Антитело свяжется антигеном (ключ попадет в замок) только в том случае, если детерминантная группа антигена полностью вместится в щель активного центра антител.
Легкие и тяжелые цепи состоят из отдельных блоков- доменов. В легких ( L ) цепях — два домена- один вариабельный ( V ) и один константный ( C ), в тяжелых ( H ) цепях- один V и 3 или 4 ( в зависимости от класса иммуноглобулина ) C домена.
Существуют легкие цепи двух типов- каппа и лямбда, они встречаются в различных пропорциях в составе различных (всех) классов иммуноглобулинов.
Выявлено пять классов тяжелых цепей- альфа ( с двумя подклассами), гамма ( с четырьмя подклассами), эксилон, мю и дельта. Соответственно обозначению тяжелой цепи обозначается и класс молекул иммуноглобулинов- А, G, E, M и D.
Именно константные области тяжелых цепей, различаясь по аминокислотному составу у различных классов иммуноглобулинов, в конечном результате и определяют специфические свойства иммуноглобулинов каждого класса.
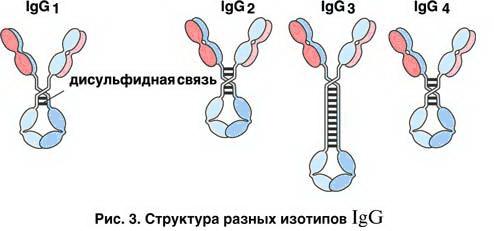
Известно пять классов иммуноглобулинов, отличающихся по строению тяжелых цепей, молекулярной массе, физико- химическим и биологическим характеристикам: IgG, IgM, IgA, IgE, IgD. В составе IgG выделяют 4 подкласса ( IgG1, IgG2, IgG3, IgG4 ), в составе IgA- два подкласса (IgA1, IgA2 ).
Структурной единицей антител является мономер, состоящий из двух легких и двух тяжелых цепей. Мономерами являются IgG, IgA ( сывороточный), IgD и IgE. IgM- пентамер (полимерный Ig). У полимерных иммуноглобулинов имеется дополнительная j ( joint) полипептидная цепь, которая объединяет ( полимеризует) отдельные субъединицы (в составе пентамера IgM, ди- и тримера секреторного IgA).
Основные биологические характеристики антител.
1. Специфичность — способность взаимодействия с определенным (своим) антигеном (соответствие эпитопа антигена и активного центра антител).
2. Валентность- количество способных реагировать с антигеном активных центров ( это связано с молекулярной организацией- моно- или полимер). Иммуноглобулины могут быть двухвалентными ( IgG ) или поливалентными (пентамер IgM имеет 10 активных центров). Двух- и более валентные антитела называют полными антителами. Неполные антитела имеют только один участвующий во взаимодействии с антигеном активный центр ( блокирующий эффект на иммунологические реакции, например, на агглютинационные тесты). Их выявляют в антиглобулиновой пробе Кумбса, реакции угнетения связывания комплемента.
3. Афинность — прочность связи между эпитопом антигена и активным центром антител, зависит от их пространственного соответствия.
4. Авидность — интегральная характеристика силы связи между антигеном и антителами, с учетом взаимодействия всех активных центров антител с эпитопами. Поскольку антигены часто поливалентны, связь между отдельными молекулами антигена осуществляется с помощью нескольких антител.
5. Гетерогенность — обусловлена антигенными свойствами антител, наличием у них трех видов антигенных детерминант:
- изотипические — принадлежность антител к определенному классу иммуноглобулинов;
- аллотипические- обусловлены аллельными различиями иммуноглобулинов, кодируемых соответствующими аллелями Ig гена;
- идиотипические- отражают индивидуальные особенности иммуноглобулина, определяемые характеристиками активных центров молекул антител. Даже тогда, когда антитела к конкретному антигену относятся к одному классу, субклассу и даже аллотипу, они характеризуются специфическими отличиями друг от друга (идиотипом). Это зависит от особенностей строения V- участков H- и L- цепей, множества различных вариантов их аминокислотных последовательностей.
Классификация по антигенам
-
антиинфекционные или антипаразитарные антитела, вызывающие непосредственную гибель или нарушение жизнедеятельности возбудителя инфекции либо паразита
-
антитоксические антитела, не вызывающие гибели самого возбудителя или паразита, но обезвреживающие вырабатываемые им токсины.
-
так называемые «антитела-свидетели заболевания», наличие которых в организме сигнализирует о знакомстве иммунной системы с данным возбудителем в прошлом или о текущем инфицировании этим возбудителем, но которые не играют существенной роли в борьбе организма с возбудителем (не обезвреживают ни самого возбудителя, ни его токсины, а связываются со второстепенными белками возбудителя).
-
аутоагрессивные антитела, или аутологичные антитела, аутоантитела — антитела, вызывающие разрушение или повреждение нормальных, здоровых тканей самого организма хозяина и запускающие механизм развития аутоиммунных заболеваний.
-
аллореактивные антитела, или гомологичные антитела, аллоантитела — антитела против антигенов тканей или клеток других организмов того же биологического вида. Аллоантитела играют важную роль в процессах отторжения аллотрансплантантов, например, при пересадке почки, печени, костного мозга, и в реакциях на переливание несовместимой крови.
-
гетерологичные антитела, или изоантитела — антитела против антигенов тканей или клеток организмов других биологических видов. Изоантитела являются причиной невозможности осуществления ксенотрансплантации даже между эволюционно близкими видами (например, невозможна пересадка печени шимпанзе человеку) или видами, имеющими близкие иммунологические и антигенные характеристики (невозможна пересадка органов свиньи человеку).
-
антиидиотипические антитела — антитела против антител, вырабатываемых самим же организмом. Причём это антитела не «вообще» против молекулы данного антитела, а именно против рабочего, «распознающего» участка антитела, так называемого идиотипа. Антиидиотипические антитела играют важную роль в связывании и обезвреживании избытка антител, в иммунной регуляции выработки антител. Кроме того, антиидиотипическое «антитело против антитела» зеркально повторяет пространственную конфигурацию исходного антигена, против которого было выработано исходное антитело. И тем самым антиидиотипическое антитело служит для организма фактором иммунологической памяти, аналогом исходного антигена, который остаётся в организме и после уничтожения исходных антигенов. В свою очередь, против антиидиотипических антител могут вырабатываться анти-антиидиотипические антитела и т. д.
Характеристика основных классов иммуноглобулинов.
IgG.
Обладая молекулярной массой 1,5 • 105 D, иммуноглобулин G способен защищать от инфекций организм новорожденного в течение первых месяцев жизни, поскольку легко проникает сквозь плаценту. Другие иммуноглобулины такого свойства лишены. IgG составляет около 70% сывороточных иммуноглобулинов, IgG – основное антитело вторичного иммунного ответа.
Иммуноглобулин G обладает самым продолжительным периодом полураспада, который составляет 21 день. Основной биологической функцией иммуноглобулинов данного класса является защита человеческого организма и его органов от возбудителей инфекционных заболеваний и от продуктов жизнедеятельности таких возбудителей путем опсонизации, активации фагоцитоза и комплемента.
Тимусзависимый иммуноглобулин G вырабатывается только при участии Т-лимфоцитов. Вследствие этого, как влияние разнообразных иммунодепрессантов, так и облучение способно не только нарушить синтез иммуноглобулина G, но и полностью его подавить.
Максимальный уровень синтеза IgG происходит вследствие вторичного введения антигена при соблюдении обусловленного интервала, который может длиться до 30-35 дн. Особенности происходящих на всех этапах выработки иммунитета процессов влияют на конечные результаты иммунизации, то есть на полноценность и завершенность иммунного ответа, на образование элементов иммунологической памяти. Именно этими обстоятельствами обосновываются схемы иммунизации – дозы и интервалы введения антигенов, их характер и свойства процессов, которые они вызывают.
Изменения обоснованных и разработанных схем иммунизации непременно должны иметь иммунологическое оправдание, в противном случае возможны нарушения в формировании клеток иммунологической памяти и в синтезе Ig, вследствие чего нарушится весь эффект иммунизации, иногда – с полным его «извращением» – сенсибилизацией.
Уровень иммуноглобулина G в организме регулируется по двум направлениям: путем разрушения Ig и вызывающей синтез IgG антигенной стимуляцией. Уровень конечной концентрации иммуноглобулина G находится в прямой зависимости между его синтезом и деструкцией.
Опираясь на высокую специфичность, иммуноглобулины G принимают активное участие в иммунном ответе, регулируя его при этом и оказывая влияние на активность прочих процессов иммунного ответа – гуморальных и клеточных, что в конечном итоге приводит к полноценности иммунного ответа. Можно сказать, что в большой степени иммуноглобулин G призван контролировать образование Ig методом обратной связи.
Как самый распространенный иммуноглобулин, Ig G обеспечивает защиту от токсинов и микроорганизмов. Есть предположение, что в процессе вторичного иммунного ответа преимущественно синтезируется именно IgG. Обладая способностью к преодолению плацентарного барьера, иммуноглобулин G выполняет ведущую роль в процессах защиты от инфекций в первые недели жизни новорожденного. Поступая через слизистую оболочку в кровоток, содержащийся в молозиве IgG усиливает защищенность новорожденного гораздо легче, чем другие иммуноглобулины. При этом, доминируя в среде прочих изотипов, иммуноглобулин G активно распространяется в тканевых жидкостях, способствует связыванию микроорганизмов с дальнейшей их опсонизацией, а также нейтрализует бактериальные токсины.
Находясь в тесном контакте (комплексе) с бактериями, иммуноглобулин G способен активировать комплемент и способствовать хемотаксису полиморфноядерных лейкоцитов. Обогащенная комплементом и антителами бактерия прилипает к лейкоциту, поскольку последний обладает рецепторами для Fс-участков и комплемента.