Материал: Сыровая А.О. и др Аминокислоты глазами химиков, фармацевтов, биологов. Т. 2

Орнитин также является предшественником в биосинтезе некоторых алкалоидов, в частности, пирролидинов, пирролизидинов, а также алкалоидов тропанового ряда, например, кокаина [13].
Орнитин входит в состав антибиотиков – бацитрацина, продуцируемого бактерией Bacillus licheniformis [85] и грамицидина – циклического пептида,
выделяемого живущей в почве бактерией Bacillus brevis [86].
Производные дикарбоновых аминокислот
L-α-Аминоадипиновая кислота является промежуточным продуктом в биосинтезе лизина, осуществляемом в клетках высших грибов и некоторых бактерий [87].
HOOC 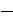 CH2 CH2 CH2 CH COOH NH2
CH2 CH2 CH2 CH COOH NH2
L-α-Аминоадипиновая кислота
Метаболический путь образования лизина в клетках грибов с участием
L-α-аминоадипиновой кислоты является уникальным для грибов и, таким образом, может служить потенциальной мишенью для разработки новых фунгицидных препаратов [88]. Эта аминокислота также найдена в составе водорастворимого белка зерна кукурузы [89].
L,L-α,ε-Диаминопимелиновая кислота представляет собой
ε-карбоксипроизводное лизина.
HOOC |
|
|
|
CH |
|
CH2 |
CH2 |
CH |
|
|
CH |
|
COOH |
|
|
|
2 |
|
|
||||||||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
NH2 |
|
|
|
|
NH2 |
|||||||
L,L-α,ε-Диаминопимелиновая кислота
246

Эта аминокислота найдена в составе белкового компонента пептидогликанов, участвующих в построении клеточных стенок практически всех бактерий [90], например, кишечной палочки (Escherichia coli) [91], дифтерийной бактерии и ряда других микроорганизмов [5].
γ-Карбоксиглутаминовая кислота (Gla) является производным глутаминовой кислоты.
HOOC
 CH CH2 CH COOH
CH CH2 CH COOH
COOH NH2
γ-Карбоксиглутаминовая кислота
Она обнаружена в протромбине и минерализованных белках тканей позвоночных. Эта аминокислота образуется из остатка глутаминовой кислоты в посттрансляционной ферментативной реакции, для которой необходим витамин К и бикарбонат. За счет остатков Gla белки, содержащие их, способны связывать ионы кальция [92–95].
Иминокислоты Пипеколиновая кислота – природная непротеиногенная α-
аминокислота, встречающаяся, главным образом, в растениях.
N COOH
H
Пипеколиновая кислота
Эта аминокислота является гомологом пролина и биосинтезируется из лизина [96]. Пипеколиновая кислота входит в состав рапамицина – макроциклического антибиотика, выделенного из продуктов жизнедеятельности почвенной бактерии Streptomyces hygroscopicus. Рамапицин проявляет
247
фунгицидную активность, а также является мощным иммуносупрессором и используется в клинической практике при пересадке органов для предотвращения отторжения [97]. Современные исследования также показывают, что рамапицин влияет на пролиферацию клеток и, таким образом, может быть использован для лечения некоторых видов рака [98]. Многочисленные природные и синтетические аналоги пипеколиновой кислоты проявляют разнообразные интересные биологические свойства – являются анестетиками, антикоагулянтами,
ингибиторами гликозидазы, а также интермедиатами в синтезе алкалоидов [99].
Азетидин-2-карбоновая кислота встречается в тканях лилейных (ландыш) и
агавах и составляет значительную часть растворимых азотсодержащих веществ в данных группах растений [100].
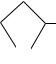
COOH
N
H
Азетидин-2-карбоновая кислота
Эта аминокислота обнаружена также в сахарной свекле и столовой свекле.
Азетидин-2-карбоновая кислота токсична для растений и животных. Будучи гомологом и антагонистом пролина, она легко встраивается в белки вместо пролина у многих видов, включая человека, и вызывает многочисленные токсические эффекты, а также врожденные пороки развития [101]. Действие еѐ как токсина основано на том, что аппарат биосинтеза белка не может отличить пролин от азетидинкарбоновой кислоты. Многие лилейные защищены от неконтролируемого встраивания этой кислоты в собственные белки благодаря наличию высокоспецифичной пролил-тРНК-синтетазы [102].
L-транс-2,3-дикарбоксиазиридин является метаболитом, выделенным из культуры Streptomyces [103].
248

H COOH
HOOC H
N
H
L-транс-2,3-дикарбоксиазиридин
Это соединение обладает антибактериальным действием. Мощная биологическая активность соединений, содержащих азиридиновое кольцо, тесно связана с высокой реакционной способностью напряженного трехчленного гетероцикла [104].
Большое внимание уделяется синтезу пептидов, содержащих 2,3-
дикарбоксиазиридин в качестве электрофильного фрагмента, поскольку они являются ингибиторами цистеиновых протеиназ – соединений необходимых для жизненного цикла паразитического микроорганизма рода Leishmaniа,
вызывающего лейшманиоз – заболевание, входящее в число 13 наиболее важных тропических болезней списка Всемирной Организации Здравоохранения. В мире от лейшманиоза страдает около 12 миллионов человек и 350 миллионов находится в группе риска, в то же время количество препаратов для лечения этого заболевания весьма ограничено. Таким образом, разработка новых пептидных селективных ингибиторов цистеиновых протеиназ на основе 2,3-
дикарбоксиазиридина является перспективным направлением в разработке новых лекарственных средств для лечения лейшманиоза [105–107].
Kаинова кислота была выделена из морских водорослей под названием
"Kainin-sou" или "Makuri" (Digenea simplex).
C |
CH3 |
COOH |
||
|
CH |
|
||
CH2 |
|
2 |
||
|
|
|
|
|
|
|
|
|
|
N COOH
H
Kаинова кислота
249
Первоначально эта кислота применялась в качестве антигельминтного средства для удаления червей из кишечника. Последующие исследования показали, что она является неразрушающимся аналогом глутамата и мощным нейротоксином. Каинова кислота проявляет нейротоксические и эпилептогенные свойства, воздействуя на каинатные рецепторы центральной нервной системы.
При связывании с соответствующими рецепторами, каинова кислота вызывает ряд клеточных ответов, в том числе приток ионов Ca2+, производство активных форм кислорода, а также митохондриальную дисфункцию, что в конечном итоге приводит к нейронному апоптозу и некрозу. Таким образом, каинова кислота используется в нейронаучных экспериментах на животных для индуцирования судорог, эксайтотоксической гибели нейронов, моделирования эпилепсии с целью исследования разнообразных нейродегенеративных процессов [108, 109].
Количество описанных в литературе непротеиногенных аминокислот все увеличивается, вероятно, в ближайшем будущем будет обнаружено множество новых аминокислот, продуцируемых микроорганизмами и морскими организмами, химический состав и метаболизм которых интенсивно изучается в последнее время и интерес к которым неуклонно возрастает.
ЛИТЕРАТУРА
1. Ambrogelly A. Natural expansion of the genetic code / A. Ambrogelly,
S. Palioura, D. Söll // Nature Chemical Biology. – 2007. Vol. 3. – N 1. – P. 29–35.
2.Lu Y. On the evolution of the standard amino-acid alphabet / Y. Lu, S. Freeland // Genome Biology. – 2006. – Vol. 7. – P. 102.
3.Uy R. Posttranslational covalent modification of proteins / R. Uy, F. Wold // Science. - 1977 . – Vol. 198. – P. 890–896.
4. Fowden L. Plant amino acid research in retrospect: from Chinball to Singh / L. Fowden // Amino Acids. – 2001. – Vol. 20. P. 217–224.
250