Материал: Сыровая А.О. и др Аминокислоты глазами химиков, фармацевтов, биологов. Т. 2
и печенью продуктов метаболизма. Он способствует улучшению секреторной функции поджелудочной железы и печени.
Вряд ли найдѐтся в человеческом организме белок, не содержащий в своѐм составе фенилаланин, который выполняет функцию строительного блока белков и является важным «кирпичиком» в «строительстве» организма. Это важно и необходимо помнить людям, желающим набрать мышечную массу. В
первую очередь это касается бодибилдеров. Фенилаланин входит в состав белков организма, которые составляют мышцы, сухожилия, связки и другие органы.
Кроме того, он входит в состав жиросжигателей. При недостатке фенилаланина невозможно добиться хороших результатов в бодибилдинге. Поэтому многие пищевые добавки в спортивном питании, созданные для увеличения интенсивности и максимального подъема энергии, содержат фенилаланин.
Человек, живущий в большом городе, так или иначе испытывает на себе влияние его суматошного ритма. Зачастую необходимо набраться сил и восстановить душевное равновесие. В отличие от искусственных стимуляторов
(кофе, алкоголя), которые истощают запас энергии и впоследствии приводят человека в состояние опустошенности и раздражения, эта аминокислота позволяет успешно справляться с раздражением и чувством тревоги. Также он снижает тягу к алкоголю и опиатам в профилактике, лечении и реабилитации опиатной и алкогольной зависимости
Фенилаланин способствует регуляции природного цвета кожи путем образования пигмента меланина. Он является необходимым при витилиго, когда происходит частичная потеря пигментации кожи. Фенилаланин помогает восстановить цвет кожи на месте бледных пятен.
Фенилаланин полезен при болезни Паркинсона (снижает тяжесть симптомов – депрессия, расстройства речи, ригидность конечностей)
В организме фенилаланин может превращаться в другую аминокислоту – тирозин, из которого синтезируются два основных нейромедиатора: дофамин и
11
норадреналин, которые непосредственно участвуют в передаче нервного импульса. Поэтому эта аминокислота влияет на настроение, уменьшает боль,
улучшает память и способность к обучению, усиливает половое влечение.
При синтезе адреналина фенилаланин стимулирует производство холецистокинина и таким образом действует как активатор аппетита, а также способствует восстановлению нормальной пигментации кожи.
L-Фенилаланин стимулирует выработку меланина, поэтому принимает участие в регуляции цвета кожных покровов.
Клинические проявления и влияние на структуры организма. Нарушение этого процесса вследствие генетически обусловленного приводит к накоплению фенилаланина в клетках и жидкостях организма. Нарушение нормального пути превращения фенилаланина вызывает вторичные биохимические реакции,
приводящие к образованию в организме фенилпировиноградной, фенилмолочной и фенилуксусной кислот и развитию заболевания – так называемой фенилкетонурии. При отсутствии или резком снижении активности фермента возникает заболевание фенилкетонурия, которое проявляется, главным образом,
выраженной олигофренией [1, 21].
Метаболизм фенилаланина в организме человека В организме фенилаланин используется только в синтезе белков. Весь
неиспользованный запас аминокислоты превращается в тирозин [2224]. В этом процессе непосредственно участвует фермент фенилаланин-4-монооксигеназа,
которая обеспечивает окисление ароматического кольца. Реакция необратима.
Активность фермента зависит от наличия Fe2+. Кофермент тетрагидробиоптерин
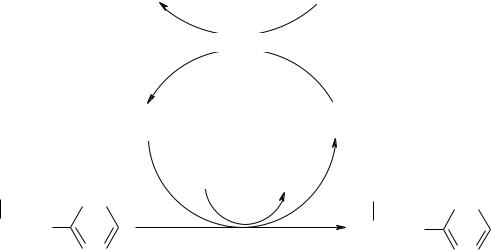
(Н4БП) в реакции окисляется до дигидроформы (Н2БП). Восстановление кофермента осуществляет дигидробиоптерин-редуктаза со своим коферементом НАДФН (NADPH + H+) (рис.3) [5,10, 21, 24].
12
НАДФ |
НАДФН |
|
Дигидробиоптеринредуктаза
|
|
|
|
|
|
|
|
|
Тетрагидро- |
|
Дигидро- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
биоптерин |
|
биоптерин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
O2 |
H2 |
O |
+ |
|
|
|
|
|
|
|
|
|||
NH3 |
|
|
|
|
|
NH3 |
|
|
|
||||||||||||
HC |
|
|
CH2 |
|
|
|
|
|
|
HC |
|
|
CH2 |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
Фенилаланин-4-монооксигеназа |
|
|
|
|
|
|
|
|||||||
|
_ |
|
|
|
|
|
|
_ |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
COO |
|
|
|
|
|
COO |
|
|
|
||||||||||||
Фенилаланин |
|
|
|
|
|
|
|
|
Тирозин |
|
|
|
|||||||||
Рис. 3. Превращение фенилаланина в тирозин Превращение фенилаланина в тирозин прежде всего необходимо для
удаления избытка фенилаланина, так как высокие концентрации его токсичны для клеток. Образование тирозина не имеет большого значения, так как недостатка его в клетках практически не бывает. Основной путь метаболизма фенилаланина начинается с его гидроксилирования, представленный на рис.4.
Фенилаланин относится к незаменимым аминокислотам, поскольку ткани животных не обладают способностью синтезировать его бензольное кольцо. В то же время тирозин полностью заменим при достаточном поступлении фенилаланина с пищей. Объясняется это тем, что основной путь превращения фенилаланина начинается с его окисления (точнее, гидроксилирования) в тирозин
(рис.4). Реакция гидроксилирования катализируется специфической фенилаланин- 4-монооксигеназой, которая в качестве кофермента содержит, как все другие гидроксилазы, тетрагидробиоптерин. Блокирование этой реакции, наблюдаемое при нарушении синтеза фенилаланин-4-монооксигеназы в печени, приводит к развитию тяжелой наследственной болезни – фенилкетонурии
(фенилпировиноградная олигофрения).
13
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
|
N N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H N |
|
|
|
|
|
|
|
|
CH |
|
|
CH |
|
|
|
CH |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
CH |
|
|
COOH |
|||||||||
NADP+ |
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|||||||||
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
5,6,7,8-тетрагидробиоптерин (Н |
4 |
БП) |
O2 |
|
|
|
|
|
|
|
|
|
|
Фенилаланин |
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Дигидроптеридин- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Фенилаланингидроксилаза, Fe 2+ |
|||||||||||||||||||||||||||||
редуктаза |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
HN |
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
N |
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
NADPH+H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
CH |
|
|
COOH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
H N |
|
|
|
|
|
|
N |
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Тирозин |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
7,8-дигидробиоптерин (Н 2БП) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
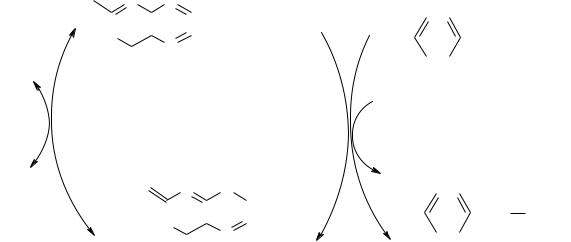
Рис. 4. Реакции гидроксилирования фенилаланина (1) и регенерации Н4БП (2)
Впроцессе трансаминирования тирозин превращается в n-
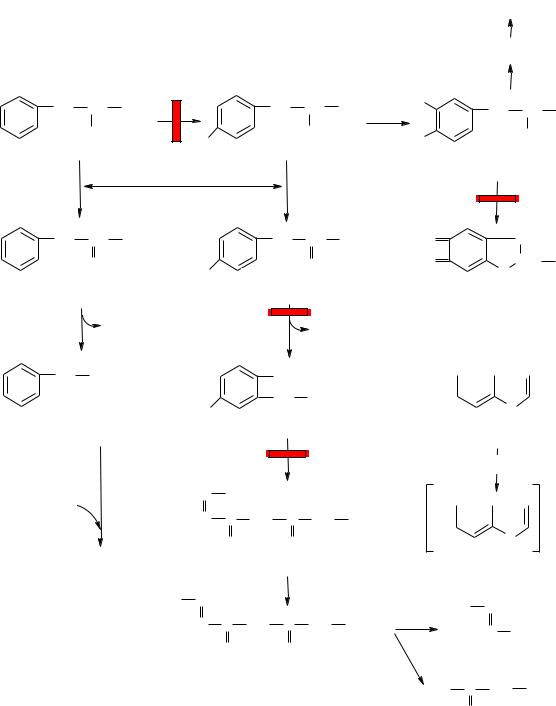
оксифенилпировиноградную кислоту, которая под действием специфической оксидазы подвергается окислению, декарбоксилированию, гидроксилированию и внутримолекулярному перемещению боковой цепи с образованием гомогентизиновой кислоты; эта реакция требует присутствия аскорбиновой кислоты, роль которой пока не выяснена. Основные метаболические превращения фенилаланина и тирозина в организме человека приведены на рис.5.
Дальнейшее превращение гомогентизиновой кислоты в малеилацето-
уксусную кислоту катализируется оксидазой гомогентизиновой кислоты.
Малеилацетоуксусная кислота под действием специфической изомеразы в присутствии глутатиона превращается в фумарилацетоуксусную кислоту,
подвергающуюся гидролизу с образованием фумаровой и ацетоуксусной кислот,
дальнейшие превращения которых уже известны.
Заболевания, связанные с нарушением метаболизма фенилаланина Депрессия. Аминокислота фенилаланин – важнейший «стройматериал» для
нейромедиаторов, способствующих бодрости, хорошему настроению,
позитивному мировосприятию и даже избавлению от боли, депрессии.
14
|
|
|
1 |
|
|
|
|
|
|
CH2 |
CH |
COOH |
|
|
CH2 |
CH |
|
COOH |
|
|
NH2 |
|
НО |
|
|
|
NH2 |
|
|
Фенилаланин |
|
|
Тирозин |
|
|
||||
|
|
|
|
|
|||||
|
|
Трансаминирование |
|
|
|
|
|
||
CH2 |
CH |
COOH |
|
|
CH2 |
CH |
|
COOH |
|
|
O |
|
НО |
|
|
|
O |
|
|
Фенилпировиноградная |
|
n-Оксифенилпировино- |
|||||||
|
|
||||||||
кислота |
|
|
|
граднаякислота |
|||||
|
|
|
|
|
|
|
3 |
|
|
|
CО2 |
|
|
|
|
CО |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
COOH |
|
|
|
OH |
|
|
|
|
|
|
|
НО |
|
|
CH2 |
COOH |
||
Фенилуксусная |
|
Гомогентизиноваякислота |
|||||||
|
|
||||||||
кислота |
|
|
|||||||
|
|
|
|
|
|
|
|
||
|
|
|
|
Fe2+ |
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
L-глутамин |
|
|
HC |
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HC |
C |
CH2 |
C |
CH2 |
COOH |
|
|
|
|
|
O |
|
O |
|
|
|
Фенилацетглутамин |
Малеилацетоуксуснаякислота |
||||||||
|
|
|
|
|
|
|
|||
|
|
НООС СН |
|
|
|
|
|
|
|
|
|
|
HC |
C |
CH2 |
C |
CH2 |
COOH |
|
|
|
|
|
O |
|
O |
|
|
|
|
|
|
Фумарилацетоуксуснаякислота |
||||||
|
Катехоламины |
|
|
|
Дофамин |
|
|
НО |
CH2 |
CH |
COOH |
|
|||
НО |
|
NH2 |
|
|
Диоксифенилаланин |
||
|
(ДОФА) |
|
|
|
|
2 |
|
|
|
H2 |
|
|
О |
C |
|
|
О |
CH2 |
COOH |
|
N |
|
|
|
H |
|
|
|
Дофахром |
|
|

 CО2
CО2
О

О
N
H
Индол-5,6-хинон
Полимеризация
О

О
N
H n
Меланин
НООС СН
HC COOH
Фумароваякислота
CH3 C CH2 COOH
O
Ацетоуксуснаякислота
Рис. 5. Основные метаболические превращения фенилаланина и тирозина Цифры – участки блокирования реакций при фенилкетонурии (1),
тирозинозе (2), альбинизме (3) и алкаптонурии (4).
15